近日,西安交通大学第一附属医院脑科学团队王强教授课题组在《自噬(Autophagy)》杂志(2022 IF: 13.391)发表题为「Impaired lipophagy induced-microglial lipid droplets accumulation contributes to the buildup of TREM1 in diabetes-associated cognitive impairment」的研究论文,揭示了高糖环境下小胶质细胞脂滴自噬受损诱导脂滴大量蓄积,通过包裹炎症放大因子 TREM1 使其在细胞内堆积,持续加重海马内神经炎症,为糖尿病认知功能损害的发生提供了新的理解。

我国糖尿病患者高达 1.47 亿,易感人群约为 1.97 亿,高居世界首位。糖尿病认知功能障碍(DACI)已超越心脑血管并发症,成为糖尿病患者第二大死因,尚无有效的诊断和指导治疗的早期生物标记物,给患者个人和社会带来沉重的医疗负担。小胶质细胞活化引起的神经炎症以及随后的神经认知功能受损是糖尿病认知功能障碍的主要发病机制。脂滴自噬是是自噬的一种,参与维持细胞内脂质及炎症稳态。近年来的研究已经表明,小胶质细胞内脂滴蓄积的老龄化大脑的一个重要特征,然而,小胶质细胞脂滴自噬是如何参与 DACI 的以及具体的分子机制知之甚少。
针对上述科学问题,研究团队构建了 2 型糖尿病喂养模型 HFD/STZ 以及基因敲除模型 db/db 小鼠,以及体外高糖培养鼠源性小胶质细胞 BV2、人源性小胶质细胞 HMC3 以及原代小胶质细胞,确认了高糖损害的脂滴自噬作用是小胶质细胞中脂滴蓄积的重要原因。从机制上创新性的发现,蓄积的脂滴与小胶质细胞特异性炎症放大因子 TREM1 共定位,并多成包裹形式,导致小胶质细胞中 TREM1 的异常堆积,这反过来又加重了高糖诱导的脂滴自噬损伤,随后通过 NLRP3 炎性小体促进高糖诱导的神经炎症级联反应。此外,本研究确定了 LP17 对 db/db 小鼠和 HFD/STZ 小鼠的 TREM1 进行药物阻断可抑制脂滴和 TREM1 的蓄积,减少海马神经元炎症损伤,从而改善认知功能。综上所述,我们的发现揭示了一个以前未被重视的机制,既高糖诱导的脂滴自噬受损与老年糖尿病患者脑内持续加重的神经炎症之间的分子机制关系,表明 TREM1 可作为一个延迟糖尿病相关认知衰退具有临床转化潜力的治疗靶点。
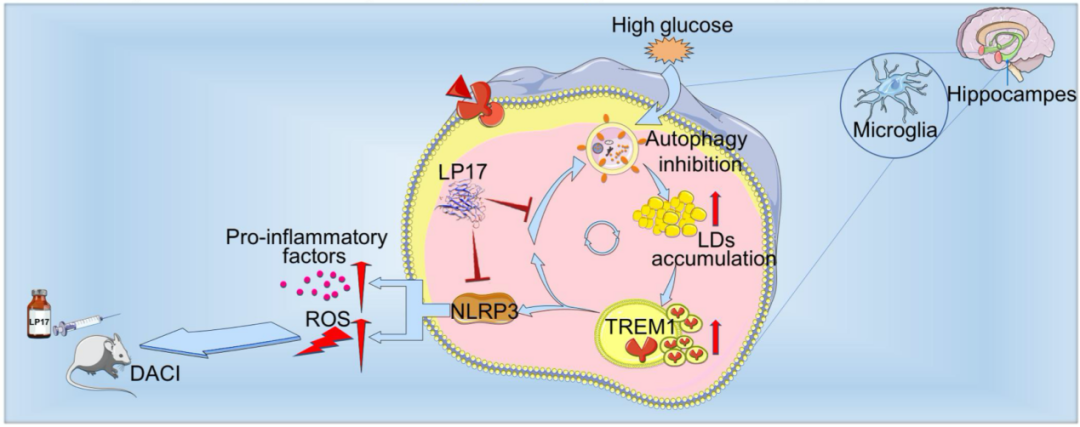
综上所述,该研究集中揭示了 DACI 中蓄积的脂滴和神经炎症的分子基础。脂质代谢和神经炎症的发生机制是非常复杂的,炎症放大因子 TREM1 蛋白水平的增加在这一过程中发挥了重要的作用,本研究中严格的数据证明了这一点。该研究也为衰老过程中的认知障碍发生机制提供了一种更深层次的理解。从临床转化潜力来讲,该研究证实了 TREM1 是糖尿病小鼠认知能力下降的潜在靶点。未来的研究方向需要进一步探索脂滴如何与 TREM1 共定位,并且是如何将炎症信号释放。
西安交通大学第一附属医院助理研究员李青博士为本文的第一作者,王强教授为论文通讯作者,西安交通大学第一附院医院为第一完成单位。本研究得到了国家自然科学基金(81974540、82274290、82203826)、陕西省重点研究与发展计划(2022ZDLSF02-09)、陕西省科技创新团队(20201TD-58)、陕西省自然科学基金(2021JQ-398)中央高校基本科研业务费(xzy012020108)和交大一附院科学基金(2020QN-11)等项目资助。
好文章,需要你的鼓励
















