来源:《临床儿科杂志》
赵琳朝, 王英洁, 景沼贺, 买钰淼, 孙盼, 邱思敏, 牛宏运, 陈志伟, 董芃芃, 刘健. 造血干细胞移植治疗儿童遗传性骨髓衰竭综合征疗效及预后分析 [J]. 临床儿科杂志, 2025, 43(7): 505-510 DOI:10.12372/jcp.2025.24e0699
ZHAO Linchao, WANG Yingjie, JING Zhaohe, MAI Yumiao, SUN Pan, QIU Simin, NIU Hongyun, CHEN Zhiwei, DONG Pengpeng, LIU Jian. Analysis of the efficacy and prognosis of hematopoietic stem cell transplantation for inherited bone marrow failure syndrome in children[J]. Journal of Clinical Pediatrics, 2025, 43(7): 505-510 DOI:10.12372/jcp.2025.24e0699
本文作者: 赵琳朝 1 王英洁 1 景沼贺 1 买钰淼 1 孙 盼 1 邱思敏 1 牛宏运 1 陈志伟 2 董芃芃 1 刘 健 1
作者单位:1. 郑州大学第一附属医院儿科(河南郑州 450052);2. 河南省儿童医院儿内科(河南郑州 450052)
摘要:目的 观察造血干细胞移植(HSCT)治疗儿童遗传性骨髓衰竭综合征(IBMFs)的疗效和预后。方法 收集 2019 年 1 月至 2023 年 11 月在郑州大学第一附属医院行 HSCT 的 IBMFs 患儿的临床资料,分析其临床特征、移植预处理方案、造血重建情况以及预后。结果 纳入 IBMFs 患儿 18 例,包括范可尼贫血(FA)7 例、先天性角化不良(DKC)5 例、先天性纯红细胞再生障碍性贫血(DBA)3 例、先天性无巨核细胞性血小板减少症(CAMT)2 例和重症先天性中性粒细胞减少症(SCN)1 例,男 10 例、女 8 例,中位移植年龄为 8.2(1.2~14.0)岁。移植后患儿中性粒细胞植入中位时间为 11(9~21)天,血小板植入中位时间为 13(10~30)天,18 例患儿在中位随访 10.6(1.0 ~ 62.9)个月时骨髓均为供者细胞完全嵌合状态。共 8 例患儿出现了急性移植物抗宿主病(GVHD),其中Ⅳ度 2 例、Ⅲ度 2 例、Ⅱ度 1 例、Ⅰ度 3 例;2 例发生慢性 GVHD,均为轻度。存活 15 例;死亡 3 例,2 例 FA 患儿出现移植相关血栓性微血管病,应用血浆置换或去纤维蛋白多核苷酸治疗,效果欠佳,此 2 例患儿均死于多脏器衰竭;1 例 CAMT 患儿移植后+28 天出现严重肺部感染,病情进展迅速,死于呼吸衰竭。结论 HSCT 是治疗儿童 IBMFs 的有效方法,根据 IBMFs 患儿所患疾病选择相适应的预处理方案可使患儿获得更好的疗效及预后。
关键词: 造血干细胞移植; 遗传性骨髓衰竭综合征; 预处理方案; 儿童
遗传性骨髓衰竭综合征(inherited bone marrow failure syndromes,IBMFs)是一组罕见的血液病,其特征是造血功能受损,具有特定的临床表现和致病机制,其中一部分患儿可进展为骨髓增生异常综合征(MDS)和急性髓系白血病(AML)。该组疾病主要包括:范可尼贫血(Fanconi anemia,FA)、先天性角化不良(dyskeratosis congenita,DKC)、先天性纯红细胞再生障碍性贫血(Diamond-Blackfan anemia,DBA)、先天性中性粒细胞减少伴胰腺功能不全综合征(Shwachman-Diamond syndrome,SDS)、先天性无巨核细胞性血小板减少症(congenital amegakaryocytic thrombocytopenia,CAMT)、重症先天性中性粒细胞减少症(severe congenital neutropenia,SCN)等。考虑到骨髓衰竭通常是患者发病和死亡的主要原因,选择造血干细胞移植(HSCT)对该组疾病的治疗具有重要意义 [1],可治愈骨髓衰竭的问题,但它可能会对患者造成一些远期影响,包括急性或慢性移植物抗宿主病(GVHD)、免疫缺陷、铁过载、肺部并发症、肾功能不全、内分泌功能不全和心理障碍等 [2-5]。国内仍缺乏大样本 HSCT 治疗儿童 IBMFs 的临床研究,多为病例个案报道,因此,本研究回顾性分析了本院行 HSCT 的 IBMFs 患儿的临床资料,包括预处理方案、供者选择、GVHD 的发生情况、预后,拟为该疾病的临床诊疗提供参考。
1 对象与方法
1.1 研究对象
回顾性分析 2019 年 1 月至 2023 年 11 月在郑州大学第一附属医院行 HSCT 的 IBMFs 患儿的临床资料。纳入标准:①年龄 0~18 岁;②IBMFs 诊断明确 [6];③移植前对患儿进行评估,均达到各疾病的移植指征 [7]。排除标准:①随访资料不全;②有移植禁忌证,包括心、肝、肾、肺等重要器官功能障碍。
本研究最终纳入分析 IBMFs 患儿 18 例,包括 FA 7 例、DKC 5 例、DBA 3 例、CAMT 2 例和 SCN 1 例,其中男 10 例、女 8 例。
1.2 方法
1.2.1 供者干细胞动员、采集和回输 供体类型包括全相合亲缘供者(MSD)3 例,不全相合亲缘供者(MMSD)2 例,全相合非亲缘供者 4 例(MUD),不全相合非亲缘供者(MMUD)6 例,以及不全相合非亲缘脐带血(UCB)3 例,其中 6 例 MMUD 均来源于中华骨髓库,人类白细胞抗原(HLA)配型均为 9/10。移植所需干细胞来源有外周血干细胞(PBSC,n= 15)和脐带血干细胞(CBSC,n= 3)。行 HSCT 患儿,供者采用粒细胞集落刺激因子(G-CSF)5~10 μg/(kg·d) 动员干细胞 5 天,后采集 PBSC。移植过程中回输 PBSC 单核细胞(MNC)中位数 11.20(4.90~27.26)×108/kg,CD34+细胞中位数 8.22(2.20~13.84)×106/kg;CBSC 的 MNC 中位计数 0.67(0.56~1.29)×108/kg,CD34+细胞中位数 0.15(0.15~0.38)×106/kg。见表 1。
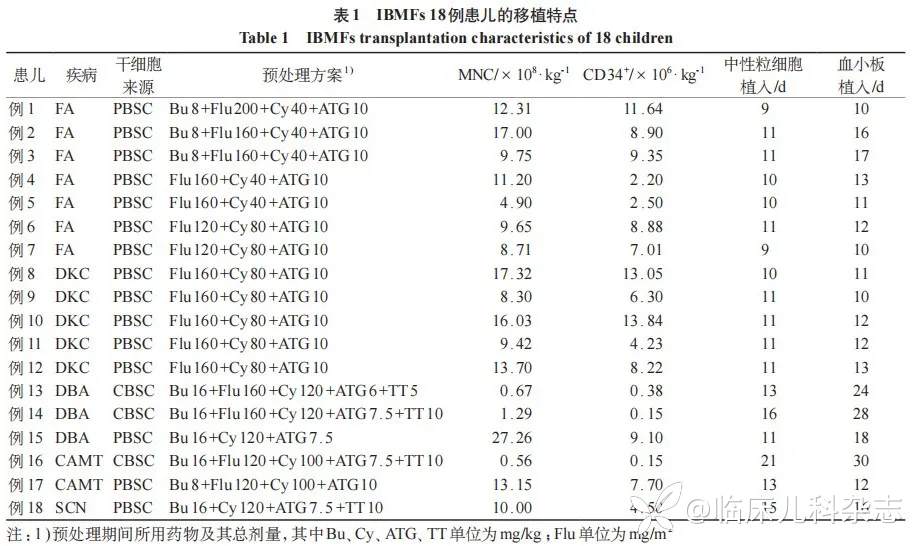
1.2.2 预处理方案 根据国际标准 [7-8],患儿移植前采用以下两种预处理方案 :减低剂量预处理(reduced-intensity conditioning,RIC)和清髓性预处理(myeloablative conditioning,MAC)。
7 例 FA 接受以氟达拉滨(fludarabine,Flu)为主的 RIC,总剂量为 Flu 120~200 mg/m2+ 环磷酰胺(cyclophosphamide,Cy)40~ 80 mg/kg+抗人胸腺免疫球蛋白(anti-human thymocyte globulin,ATG)10 mg/kg,根据骨髓衰竭程度考虑是否加用白消安(busulfan,Bu)4.0 mg/(kg·d)×2d。5 例 DKC 接受 RIC,总剂量为 Flu 160 mg/m2+Cy 80 mg/kg+ATG 10 mg/kg。3 例 DBA 患儿中,1 例 PBSC 患儿接受 MAC,总剂量为 Bu 16.0 mg/kg+Cy 120 mg/kg+ATG 7.5 mg/kg;2 例 CBSC 患儿接受 MAC,总剂量为 Bu 16.0 mg/kg+Flu 160 mg/m2+Cy 120 mg/kg +ATG 6~7.5 mg/kg+塞替派(thiotepa,TT)5~10 mg/kg。2 例 CAMT 患儿中,1 例 PBSC 患儿接受 RIC,总剂量为 Bu 8.0 mg/kg+Flu 120 mg/m2+Cy 100 mg/kg+ ATG 10 mg/kg;1 例 CBSC 患儿接受 MAC,总剂量为 Bu 16.0 mg/kg+Flu 120 mg/m2+Cy 100 mg/kg+ATG 7.5 mg/kg+TT 10 mg/kg。1 例 SCN 患儿接受 MAC,总剂量为 Bu 16.0 mg/kg+Cy 120 mg/kg+ATG 7.5 mg/kg+ TT 10 mg/kg。
1.2.3 移植物抗宿主病预防 急性 GVHD 按 Glucksberg 标准 [9] 进行分级 ;慢性 GVHD 按美国国立卫生研究所(NIH)2005 年发布的诊疗共识 [10] 进行诊断和评估。本研究中预防 GVHD 主要使用环孢素(cyclosporin A,CsA)和小剂量甲氨蝶呤(methotrexate,MTX),根据患儿供者不同加减吗替麦考酚酯(mycophenlate mofetil,MMF)。从-7d 开始静脉滴注 CsA 3~5 mg/(kg·d),待肠道功能恢复后改为口服,用药期间调整血药浓度达到 150~250ng/mL;MMF 使用时从-7d 按照 30 mg/(kg·d) 开始口服,连用 30d 停用;移植后短程应用小剂量 MTX,在+1d、+3d、+6d 分别予 15 mg/m2、10 mg/m2 和 10 mg/m2。
1.2.4 随访 随访方法为住院、门诊或电话随访,以移植当天为患儿随访的时间起点,以月为单位计算随访时间,当患儿出现移植后复发、严重并发症等所导致的死亡,失访或截止时间时停止随访,本研究随访至 2024 年 3 月。
1.3 统计学分析
采用 SPSS 26.0 统计软件处理数据。非正态分布计量资料以中位数(全距)表示,计数资料以 n(%)表示;采用 Kaplan-Meier 生存曲线分析移植后急性 GVHD 累积发生率以及无失败生存率。
2 结果
2.1 造血重建
18 例行 HSCT 的 IBMFs 患儿的中位移植年龄 8.2(1.2~14.0)岁,发病至移植前中位病程为 33.0(2.0~112.0)个月。移植后患儿中性粒细胞植入中位时间为 11(9~21)天,血小板植入中位时间为 13(10~30)天。见表 1。
2.2 GVHD 发生情况
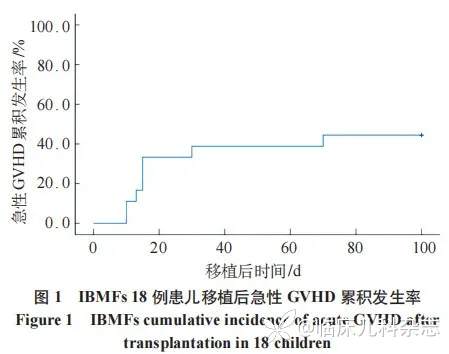
8 例 IBMFs 患儿在 HSCT 后发生急性 GVHD,其中Ⅳ度 2 例、Ⅲ度 2 例、Ⅱ度 1 例、Ⅰ度 3 例,包括 4 例 FA,2 例 DKC,以及 DBA、SCN 患儿各 1 例;急性 GVHD 发生的中位时间为移植后 15(10~70)天,急性 GVHD 累积发生率为(44.4±11.7)%(图 1)。1 例 FA 患儿及 1 例 DKC 患儿后续出现轻度慢性 GVHD,慢性 GVHD 累积发生率为(11.1±7.4)%。
2.3 其他并发症
2 例 FA 患儿出现了移植相关的血栓性微血管病,应用血浆置换或去纤维蛋白多核苷酸治疗,效果欠佳,后 2 例患儿均死于多脏器衰竭。3 例患儿(2 例 DKC 和 1 例 FA)住院期间发生可逆性后部白质脑病综合征,均出现继发性高血压、头痛等不适,予降压药物应用、免疫抑制剂适当减量后症状逐渐好转。6 例患儿(包括 3 例 DKC、1 例 FA、1 例 DBA 和 1 例 SCN)出现出血性膀胱炎,1 例 FA 患儿并发移植相关的血栓性微血管病等并发症,后对症治疗无效后死亡,余患儿经水化碱化以及免疫抑制剂适当减量后逐渐好转。
此外,1 例 DBA 患儿移植+53 天出现肺部感染、胸腔积液、空洞形成,病原学检查示嗜肺军团菌感染、肺炎克雷伯杆菌感染,药物治疗效果欠佳,后行肺叶切除术;另 1 例 DBA 患儿移植+38 天出现侵袭性黑曲霉菌感染,治疗后逐渐进展为闭塞性细支气管炎、支气管扩张,生存质量欠佳;1 例 CAMT 患儿移植后+28 天出现严重肺部感染,病情进展迅速,后死于呼吸衰竭。
2.4 随访结果
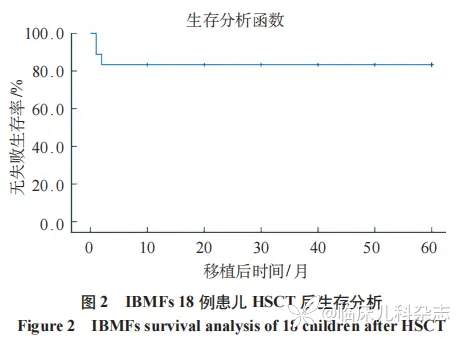
HSCT 后获得成功植入的 18 例患儿中无失访病例。中位随访时间为 10.6(1.0~62.9)个月,截至随访日期,本组患儿骨髓均为供者细胞完全嵌合状态,HSCT 治疗无失败生存率为(83.3±8.8)%(15/18),见图 2。
3 讨论
IBMFs 是一组异质性的罕见血液系统疾病。HSCT 仍然是 IBMFs 造血障碍的唯一根治性治疗选择。本研究中行 HSCT 的 IBMFS 主要有 FA、DKC、DBA、CAMT 等。
随着移植技术的进步,HSCT 的供者来源较前更为广泛,PBSC 是目前同种异体 HSCT 的主要干细胞来源,在供者选择时,HLA 配型是主要考虑因素,其他因素包括供者年龄、性别等 [11]。本研究患儿主要应用 PBSC 移植,仅 3 例行 CBSC 移植,考虑到输注干细胞数量较少,造血重建时间较 PBSC 组延迟,因此对于脐血移植患儿,输注足够的干细胞对造血重建至关重要。
IBMFs 患儿因疾病各异,应选择不同的预处理方案。FA 和 DKC 患儿对化学毒性药物如 Cy、Bu 或电离辐射非常敏感,大剂量放化疗会增加患儿移植相关毒性和死亡概率 [3,12],本研究中 7 例 FA 患儿,其中 2 例预处理方案 Cy 总剂量为 80 mg/kg,均发生急性 GVHD,预后明显较 Cy 总剂量为 40 mg/kg 的另外 5 例 FA 患儿差。Flu 是一种抗代谢药物和免疫抑制剂,对 FA 和 DKC 患儿而言相对安全且具有足够免疫抑制作用,因此本研究主要应用高剂量的 Flu 以保证移植的顺利进行及低剂量的 Cy 减少移植相关不良反应。印度近期一项研究表明 [12],FA 患儿接受以 Flu 为基础的 RIC 预处理方案后行 HSCT,5 年总生存率(OS)为 80%。Bhoopalan 等 [13] 报道了 9 例 DKC 患儿接受以 Flu 为基础的 RIC 预处理方案后行 HSCT,OS 为 66.7%,且在随访期间未观察到明显的移植并发症,这些研究均证实了该方案的安全性及可行性。因此,尽管 FA 和 DKC 的预处理方案并没有达成共识,目前本中心大多采用以 Flu 为基础的 RIC 预处理方案。相较于 MAC 方案,接受 RIC 预处理方案的患儿容易在移植后出现供体的混合嵌合 [14],本研究中 7 例 FA 和 6 例 DKC 患儿均采用以 Flu 为基础的 RIC 方案,且随访期间均植入成功,在移植后 30 天内实现了 ≥ 95% 的供体嵌合,当然本研究样本量较小,还需进一步累积病例。此外,有研究表明 HSCT 可增加 DKC 患儿肺部疾病的风险,移植后中位发病时间为 4.7 年 [15]。本组 6 例 DKC 患儿随访期间均存活,短期效果较好,均未发生严重的肺部疾病,长期疗效仍有待研究,后期应注意随访患儿肺功能等相关指标。
目前 DBA 移植更多使用 MAC 方案 [16],RIC 方案虽降低了患儿移植相关毒性,但增加了 DBA 患儿移植失败的风险。本研究中 3 例 DBA 患儿均接受了基于 Bu 的 MAC 方案,所有患儿随访期间均为供体完全嵌合,存活且不依赖输血。近期研究表明,DBA 患儿中激素无效或因生长迟缓等不能耐受激素治疗者,都可考虑在 10 岁之前进行移植 [17-18],本组 DBA 患儿接受 HSCT 的年龄相对较小,均在此范围内。对于 CAMT 和 SCN 来说,欧洲血液和骨髓移植学会(EBMT)专家小组建议将基于 Flu 和 Bu 的 MAC 用于孤立血小板减少症或进展为 MDS、白血病的 CAMT 患儿,RIC 用于全血细胞减少症 CAMT 患儿,基于 Bu 和 Cy 的 MAC 用于 SCN 患儿 [7]。
GVHD 是影响 IBMFs 患儿 HSCT 结局的重要因素,本研究中 8 例患儿出现了急性 GVHD,包括 4 例 FA,2 例 DKC,以及 DBA、SCN 患儿各 1 例,急性 GVHD 的危险因素包括 HLA 配型、供受体性别差异、预处理方案强度、患儿年龄、移植物来源等 [19],本研究 18 例行 HSCT 的患儿移植后 100 天内急性 GVHD 累积发生率为 44.4%,其中 2 例进展为轻度慢性 GVHD,主要表现为局限性皮肤红疹及口腔溃疡、黏膜苔藓样变,但局限性口腔慢性 GVHD 可能增加口腔鳞状细胞癌的发生风险,所以即使程度较轻,仍应积极处理;予患儿口服免疫抑制剂并局部应用地塞米松含漱液以控制症状,并定期进行致癌监测。有研究表明非亲缘脐血移植与慢性 GVHD 累积发生率较高相关 [1],本研究非亲缘脐血移植患儿较少,均未发生慢性 GVHD。
综上所述,HSCT 为 IBMFs 患儿的有效治疗方法。尽管异基因 HSCT 具有一定风险,但其仍然是维持生命和改善生活质量的重要手段。预处理方案的选择是 HSCT 能否成功的关键,因此需依据患儿所患疾病来选择合适强度的预处理方案。本研究旨在评估 IBMFs 患儿行 HSCT 的疗效及预后,结果显示移植后 1 年内的累积无失败生存率为 83.3%,肯定了 HSCT 对于儿童 IBMFs 的治疗效果。然而,本研究病例数有限,随访时间较短,所得结论还需更多研究进一步验证。
好文章,需要你的鼓励
















