


湖州市中心医院胃肠外科团队胃食管反流病遗传学研究成果获权威期刊《Communications Biology》发表
近日,湖州市中心医院胃肠外科魏云海主任团队与山东第一医科大学常啸教授团队合作,在胃食管反流病(GERD)遗传机制研究领域取得重要进展。相关成果发表于 Springer Nature 旗下国际权威期刊《Communications Biology》(中科院双一区 TOP 期刊,影响因子 5.1),魏云海主任为论文第一作者,湖州市中心医院为第一完成单位。

该研究通过创新人工智能模型,系统揭示了 GERD 的遗传基础,为深入理解其发病机制与开发新型治疗策略提供了关键线索。
研究背景
AI 赋能
破解复杂疾病遗传密码
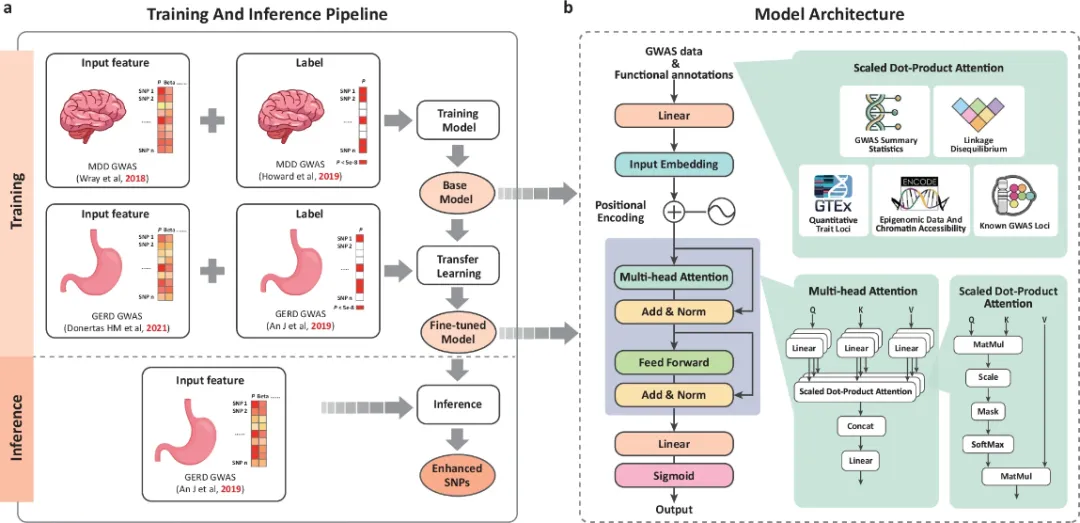
GERD 是临床常见的慢性胃肠道疾病,传统抑酸治疗虽可缓解症状,但难以从根本上应对其复发倾向与癌变风险。研究表明,GERD 与抑郁症等多种精神障碍存在显著的遗传重叠,提示其发病涉及多基因、多通路的复杂交互,尤其与神经调控及上皮屏障功能密切相关。然而,传统遗传学研究方法受限于统计学阈值,难以系统捕捉其中微效而广泛的遗传信号。
为此,研究团队独辟蹊径,引入前沿人工智能技术,开发了名为 InsightGWAS 的 Transformer 深度学习模型。该模型的核心创新在于采用了 「跨疾病迁移学习」 策略——首先利用与 GERD 遗传高度相关(遗传相关系数 rg = 0.52)的重度抑郁症大规模遗传数据进行预训练,使其习得复杂神经精神性状的遗传模式,再针对 GERD 特有数据进行精调。这一设计显著增强了对微弱但真实遗传信号的探测能力,突破了传统分析方法的瓶颈。
核心成果
发现 209 个新型风险位点
揭示「神经-上皮」交互框架
通过这一创新分析方法,研究不仅全面验证了已知的 GERD 风险位点,更全新发现了 209 个此前未被报道的候选基因座。深入的功能富集分析表明,这些新位点显著聚集于化学突触传递、神经元发育以及上皮钙粘蛋白介导的信号通路。这从遗传学层面首次系统勾勒出 GERD 「神经-上皮」双重通路交互作用的发病框架,即疾病发生同时涉及神经系统调控异常与食管上皮屏障功能受损。
学术价值
提供遗传解析新范式
深化疾病机制认知
本研究的学术价值突出体现在两方面:一是在方法学上,成功验证了「迁移学习+深度学习」整合多组学数据解析复杂疾病遗传架构的可行性,为同类研究提供了新范式;二是在生物学认知上,将 GERD 的遗传基础从传统的胃肠局部范畴,拓展至与中枢神经系统功能密切关联的跨系统调控网络,极大地深化了对该疾病本质的理解。
临床意义
超越抑酸治疗
指明精准医学新方向
该研究成果具有明确的临床转化前景。所发现的数百个新位点及其关联的神经与上皮通路,为未来开发超越单纯抑酸的新型疗法指明了方向。例如,针对神经调控通路的药物可能改善食管感觉与动力障碍,而增强上皮屏障功能的策略或许能从根本上减少反流损伤。这为 GERD 的精准分型、个体化治疗及预防策略的制定奠定了重要的理论基石,有望最终提升临床疗效,改善患者远期预后。
论文信息
标题:
Transformer-based InsightGWAS improves GERD genetic discovery via pretraining on GWAS for major depressive disorder
期刊:Communications Biology
链接:https://www.nature.com/articles/s42003-025-09177-3
魏云海

主任医师 / 教授 / 硕导
湖州市中心医院大外科副主任、胃肠疝外科主任
好文章,需要你的鼓励
推荐阅读













