
细胞外基质(ECM)是肿瘤转移的首要物理屏障。西安交大一附院杨谨教授课题组、仿生工程与生物力学研究所(BEBC)徐峰团队围绕「癌细胞如何突破 ECM 屏障」展开深入研究。发现癌细胞群能协同重塑 ECM,在致密基质中构筑四通八达的微通道网络结构,作为肿瘤细胞跨越屏障、畅通无阻的「高速公路」。基于原子力显微镜–光镊–共聚焦一体化系统,团队实现了微通道网络形成过程中微结构与力学性能的全面表征,并结合单细胞测序、分子干预、数理模型等多学科手段,系统解析了转移微通道网络形成的力学生物学机制,鉴定出关键力敏感细胞亚群及调控分子,从力医学视角提出了肿瘤转移的全新力学生物学理论框架及潜在干预新靶点。
临床难题与关键发现:首次揭示「微通道网络」这一肿瘤转移新结构
肿瘤远处转移是临床治疗中最具挑战性的科学问题之一,癌细胞如何突破 ECM 这一核心物理屏障仍缺乏系统理论框架。既往研究表明乳腺癌细胞能通过 ECM 力学重塑形成微通道结构作为阻力最小的迁移路径。然而,既往研究仅仅在单细胞水平上聚焦于单个微通道的形成过程,多细胞水平微通道的延伸规律及机制仍不清楚。本研究团队将研究焦点从独立的细胞个体升级为相互协作的群体,首次观察到癌细胞在群体尺度下能够协同自组装 ECM 微结构,逐步构建出由多条微通道相互连接、具有拓扑特征的微通道网络。该网络作为细胞群体转移过程中畅通无阻的「高速公路」,使群体迁移效率显著提高,揭示了肿瘤细胞在复杂力学微环境中实现高效转移的新模式。
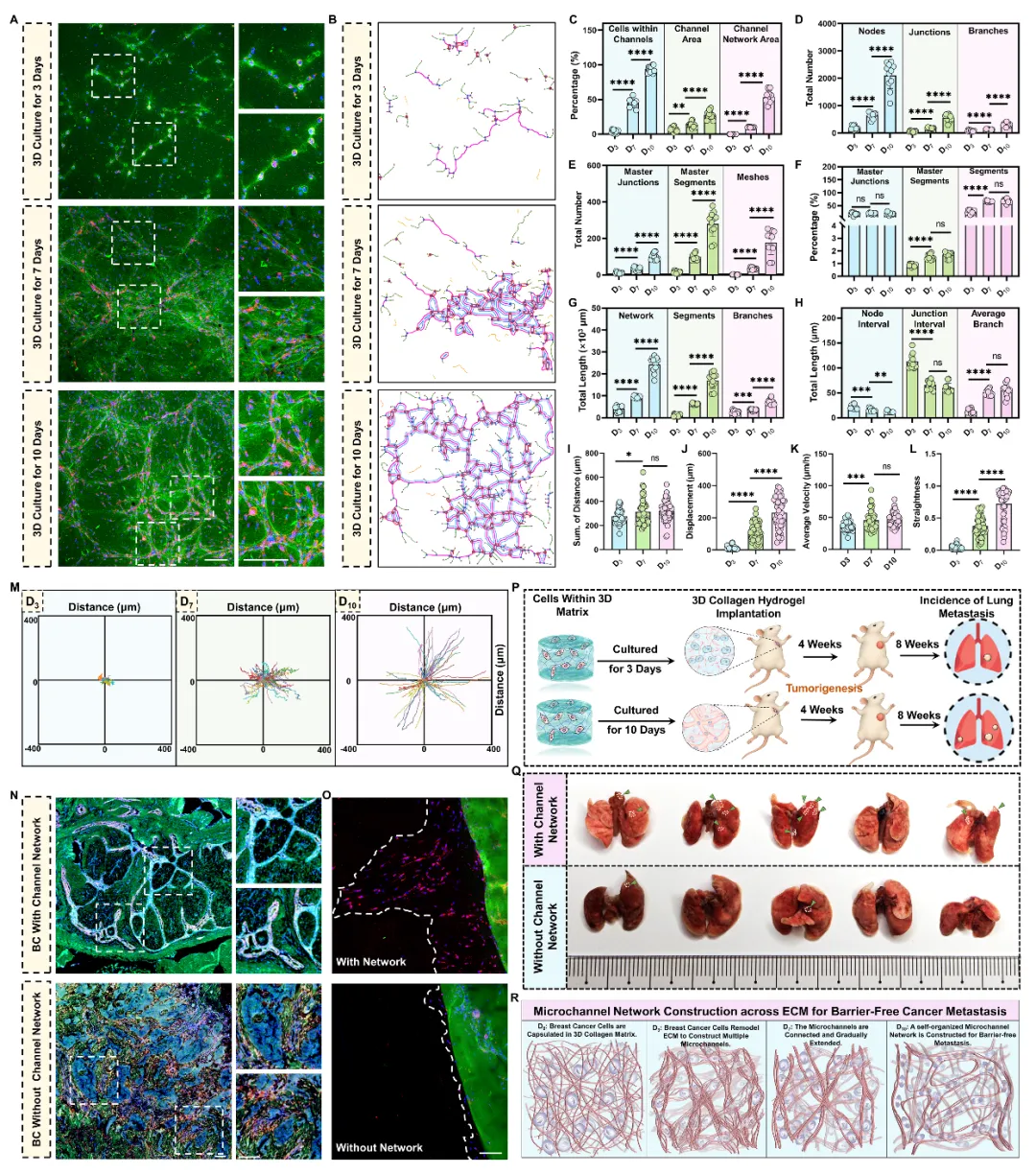
多学科交叉研究手段解析微通道网络构建过程的力学生物学特征机制
为揭示微通道网络构建得力学生物学机制,本研究基于团队自主搭建的原子力显微镜–光镊–共聚焦成像一体化平台,对网络构筑过程中的 ECM 力学性能、组织微结构及细胞牵引行为进行了全程原位力学生物学表征。结果显示,微通道之间的连接并非随机,而是在癌细胞群体协调施力下沿特定方向延伸并精准汇合,其方向性由细胞重塑 ECM 后形成的「机械桥」所引导。机械桥由高度对齐的胶原纤维组成,可跨尺度传递力学信号,促使相邻通道实现有序交汇。
进一步结合单细胞测序、分子干预及无格点 agent-based 数理模拟,鉴定出一类富集 Integrin–RhoA/YAP 信号轴与 MMP14 的力敏感型领导细胞(leader cells),其具备更强的机械响应能力与 ECM 改造能力,主导微通道的延伸与交汇。本研究基于 ECM 力学重塑的新型促转移生物网络及其形成的机制,从力医学视角为乳腺癌转移提供全新力学生物学理论框架及潜在干预靶标。
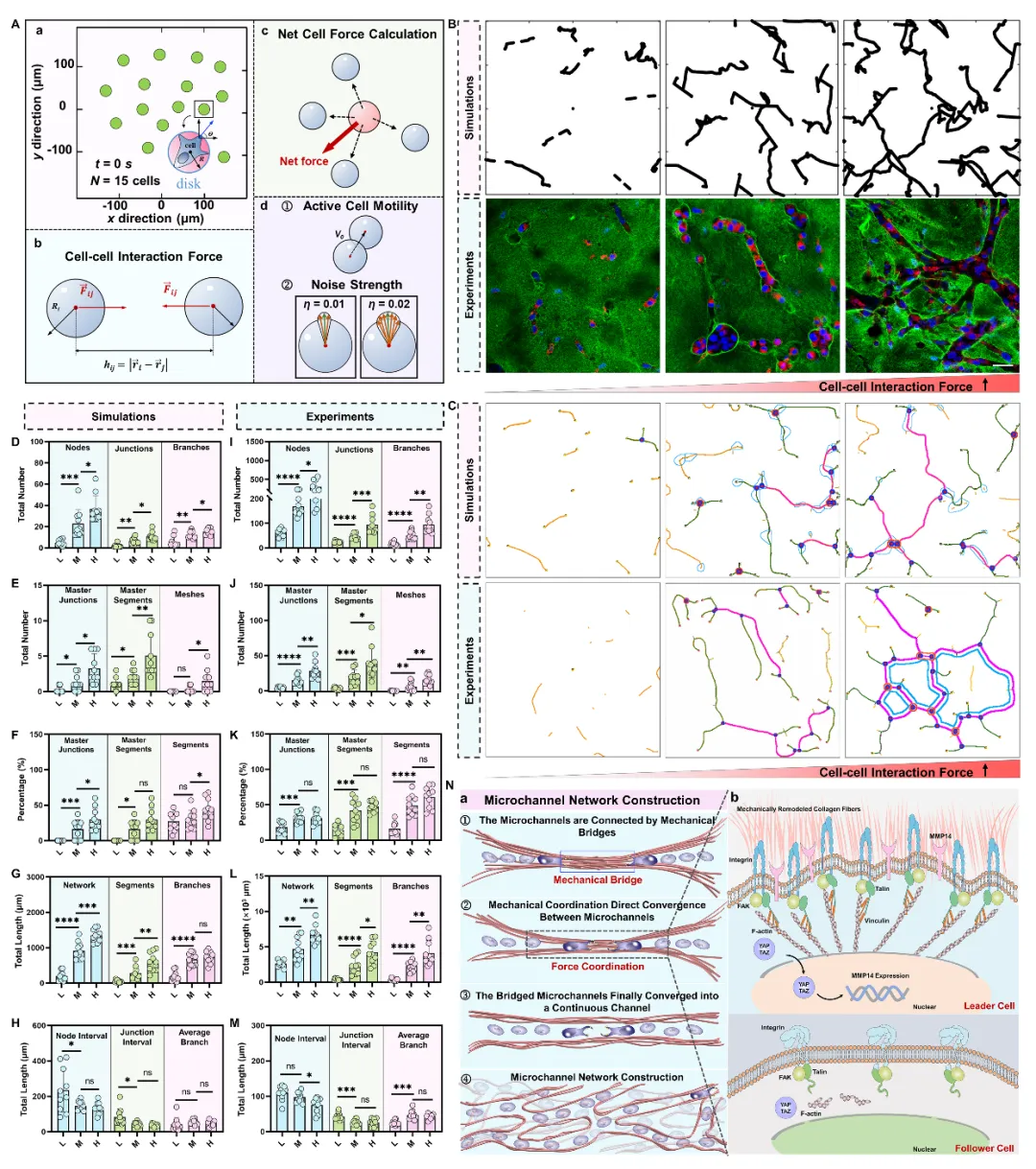
该研究成果以 Multicellular Force Coordination Constructs Microchannel Networks for Barrier-Free Metastasis across Extracellular Matrix 《力学信号交流驱动癌细胞群协同构筑高效转移微通道网络》为题近日在 Science Advances《科学进展》在线发表,西安交大一附院 I 期临床试验研究中心(第一作者单位)杨谨教授与西安交通大学 BEBC 徐峰教授共同指导的研究医生高欢作为第一作者,西安交通大学程波教授与靳国瑞教授为共同第一作者。杨谨教授、徐峰教授,以及西安交大一附院癌症中心名誉主任徐兵河院士、BEBC 靳国瑞教授、林敏教授、西安交大二附院郭卉教授为共同通讯作者。本研究依托西安交大仿生工程与生物力学研究所、西安交大一附院精准医学研究中心开展,获得国家自然科学基金重点/面上项目/青年项目、国家医学攻关产教融合创新平台等基地的支持。
好文章,需要你的鼓励
















