来源:高博医疗集团
3 月 4 日,我国自主研发的新型人类表皮生长因子受体 2(HER2)抗体偶联物(ADC)——瑞康曲妥珠单抗,治疗晚期胃/胃食管结合部腺癌(GC/GEJ)和结直肠癌(CRC)患者的Ⅰ期临床数据已发布,并刊登在肿瘤学领域的顶级期刊《Journal Of Clinical Oncology》(JCO,IF:43.4)杂志上,本项研究由中国药科大学上海高博肿瘤医院李进教授担任通讯作者。研究初步展示了瑞康曲妥珠单抗在 HER2 表达的 GC/GEJ 和 CRC 患者中有良好的抗肿瘤活性和安全性 [1]。

研究发表于 JCO
研究背景
根据 GLOBOCAN 2022 数据报道,GC/GEJ 的发病率和死亡率位居第五,CRC 的发病率和死亡率分别为第三和第二,两大瘤种已成为全球人群的健康负担 [2]。HER2 的异常改变与多种肿瘤的发生发展相关,其也是目前包括消化系统肿瘤在内多种肿瘤治疗的关键靶点 [3,4];在 GC/GEJ 患者中,HER2 在约 40% 的患者中表达 [5],在约 3%-11% 的 CRC 患者中过表达。
瑞康曲妥珠单抗(研发代号 SHR-A1811)是新一代以 HER2 为靶点的 ADC 药物,其通过可裂解的连接子将曲妥珠单抗与 DNA 拓扑异构酶 I 抑制剂(SHR169265)偶联而成,具有载荷 SHR169265 强效,药物-抗体比(DAR)较低的特点,可以兼顾疗效和安全性。
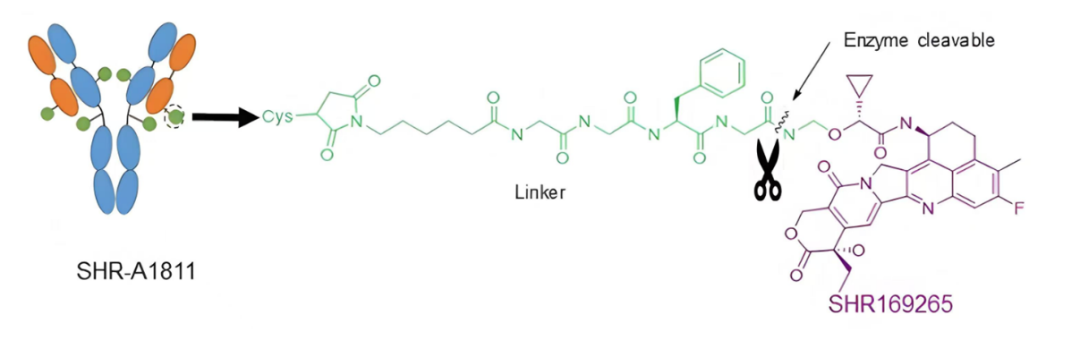
研究方法
此项Ⅰ期临床试验包括剂量递增、药代动力学扩展和临床扩展三个部分,纳入经标准治疗失败、对标准治疗不耐受或无可用标准治疗且具有 HER2 表达(IHC 1+,2+或 3+或 ISH+)的 GC/GEJ 和 CRC 患者。瑞康曲妥珠单抗剂量递增阶段采用 i3+3 方案,递增剂量依次为 3.2 mg/kg、4.8 mg/kg、6.4 mg/kg 和 8.0 mg/kg;选择 2-3 个剂量组进行药代动力学扩展。在临床扩展阶段,将进一步收集安全性和有效性数据。主要终点为剂量限制性毒性(DLT)和安全性,次要终点为药代动力学特征和客观缓解率(ORR),疾病控制率(DCR),缓解持续时间(DoR),无进展生存率(PFS)以及总生存率(OS)。
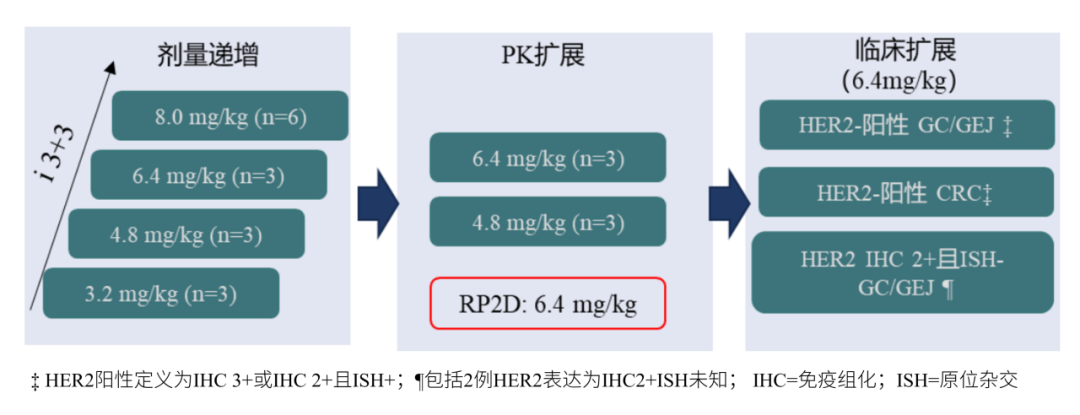
研究结果
1、患者基线数据
试验共纳入 100 例患者(剂量递增 15 例,剂量拓展 18 例,临床拓展 67 例);GC/GEJ 患者 57 例(胃癌患者 52 例,胃食管结合部癌 5 例),96.5% 的患者 ECOG 评分为 1,50.9% 的患者既往接受过抗 HER2 治疗;CRC 患者 43 例(左半结肠 11 例,右半结肠 12 例,直肠 20 例),90.7% 的患者 ECOG 评分为 1,27.9% 的患者既往接受过抗 HER2 治疗。截至 2024 年 2 月 29 日,11 例患者仍在治疗中,89 例患者停止治疗,主要原因是疾病进展。
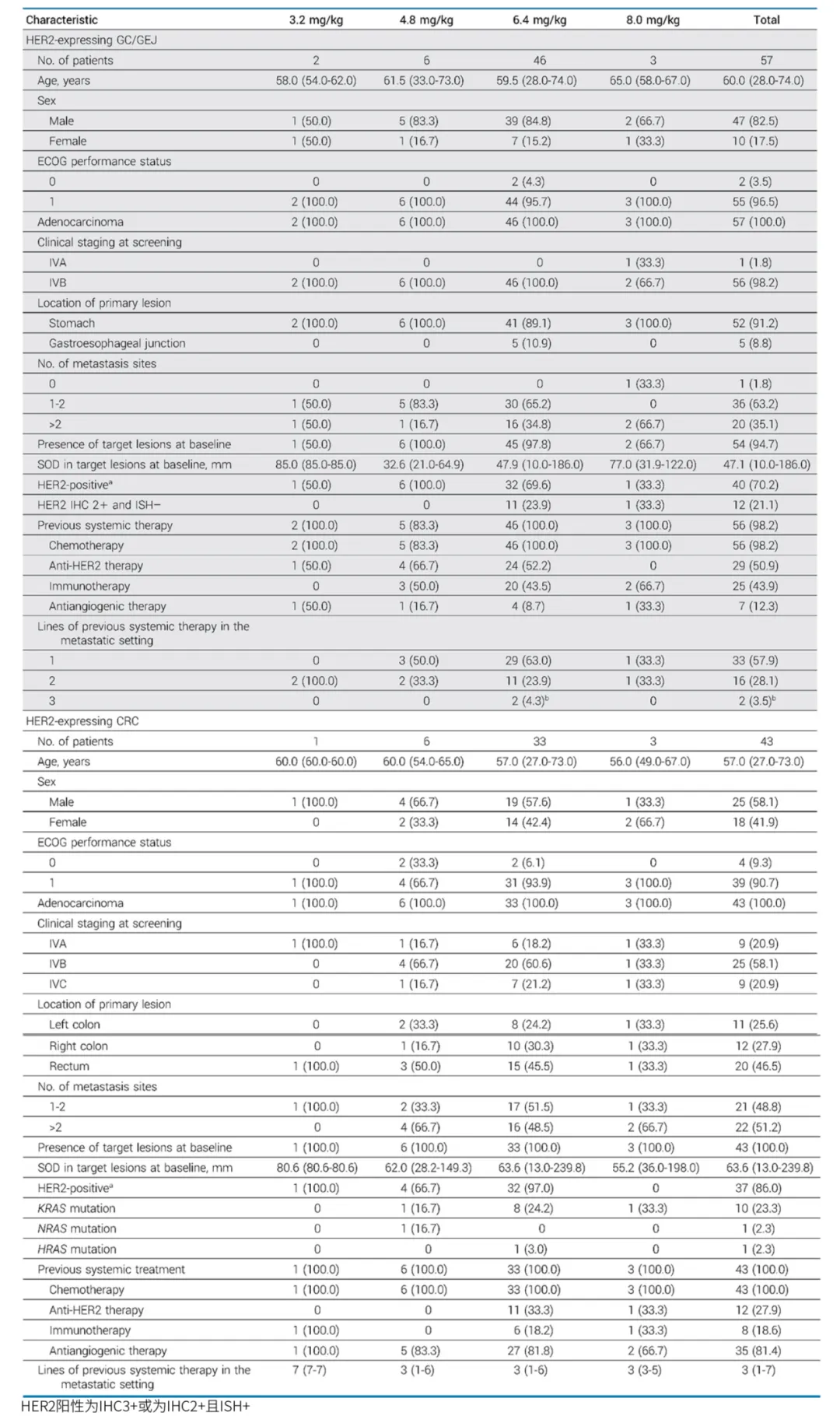
2、临床疗效
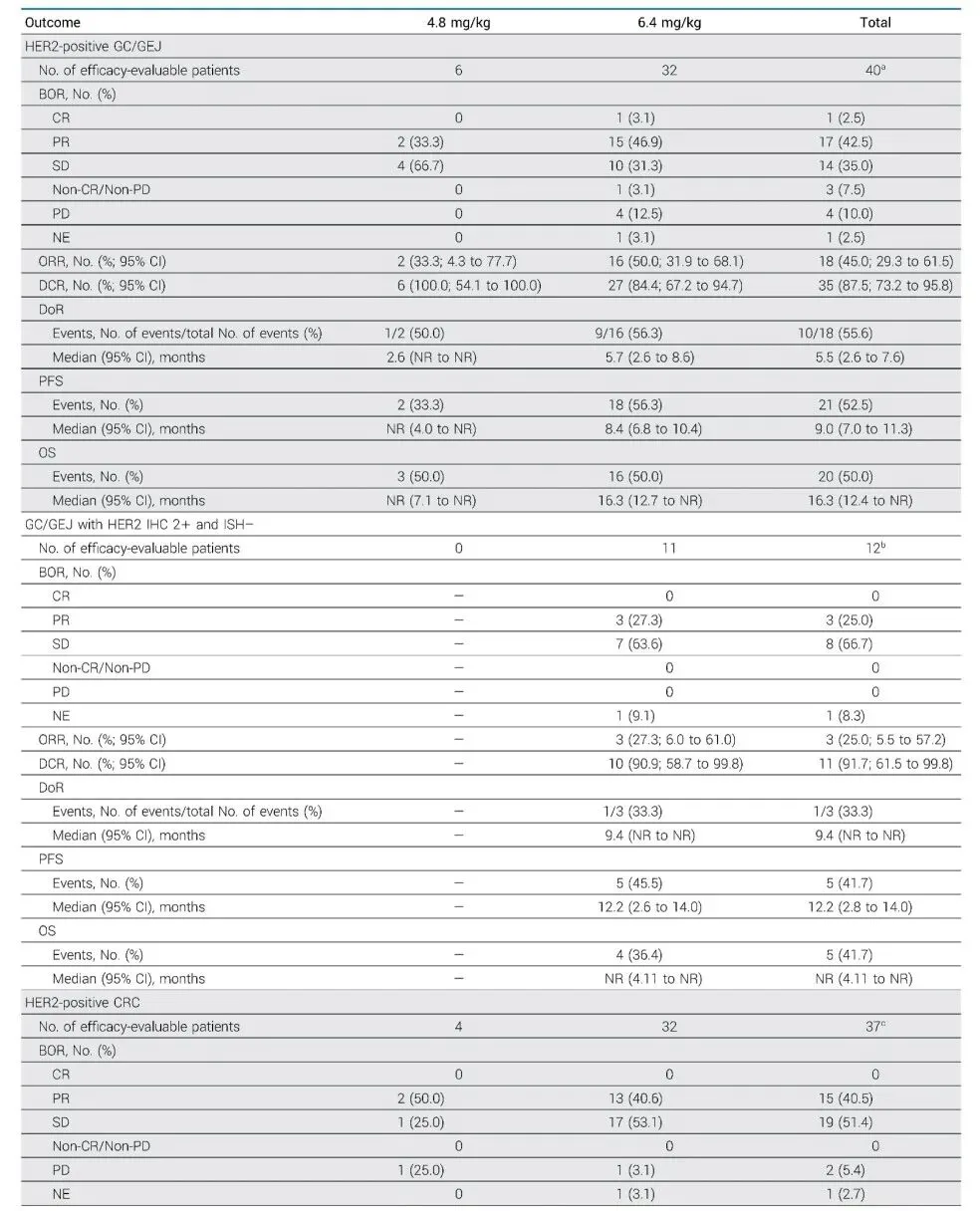
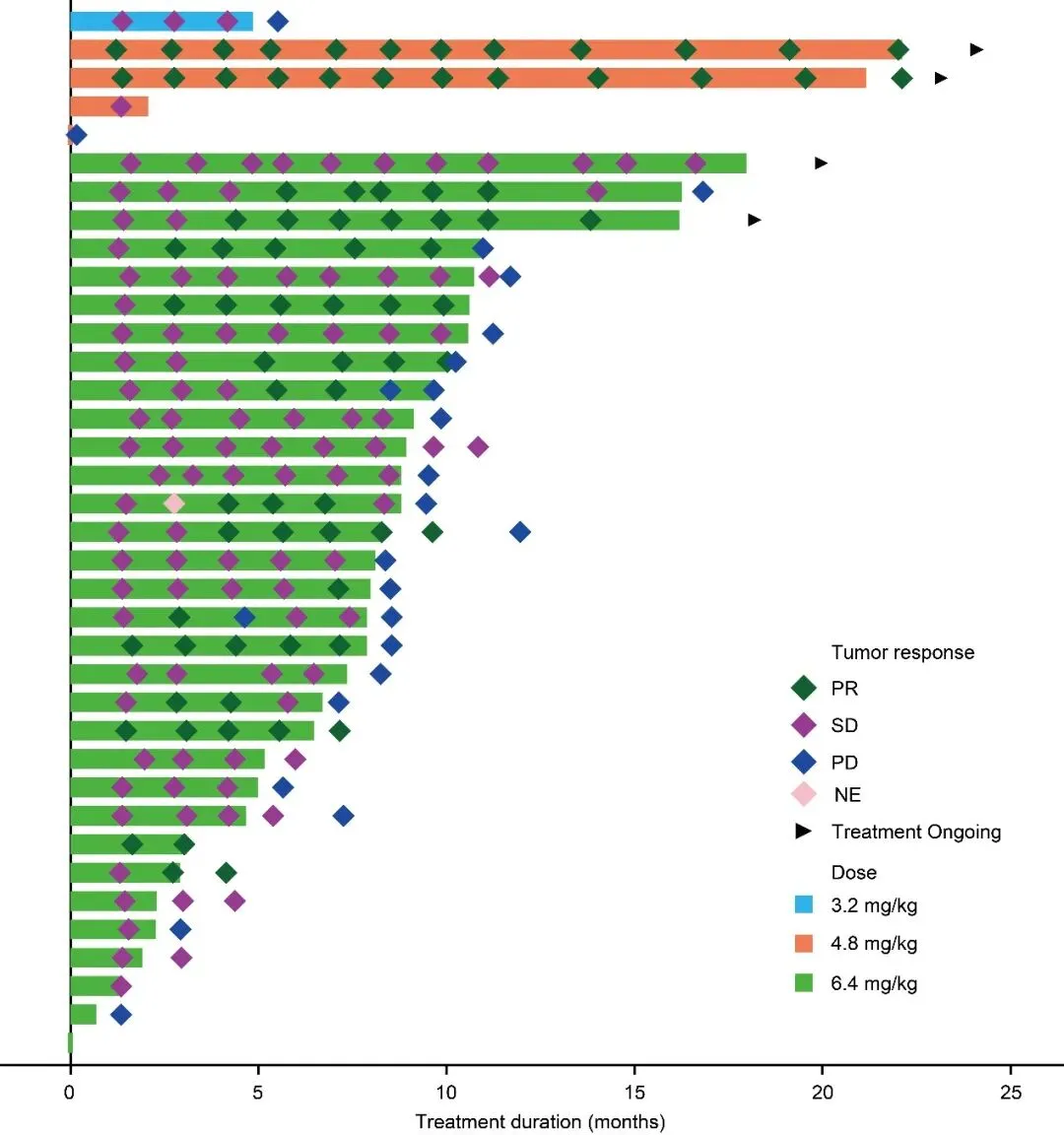
100 例患者接受了至少一次瑞康曲妥珠单抗治疗(57 例 HER2 表达的 GC/GEJ 患者,43 例 HER2 表达的 CRC 患者),截止 2024 年 2 月 29 日,GC/GEJ 患者和 CRC 患者的中位随访时间分别为 11.4 个月和 13.8 个月。
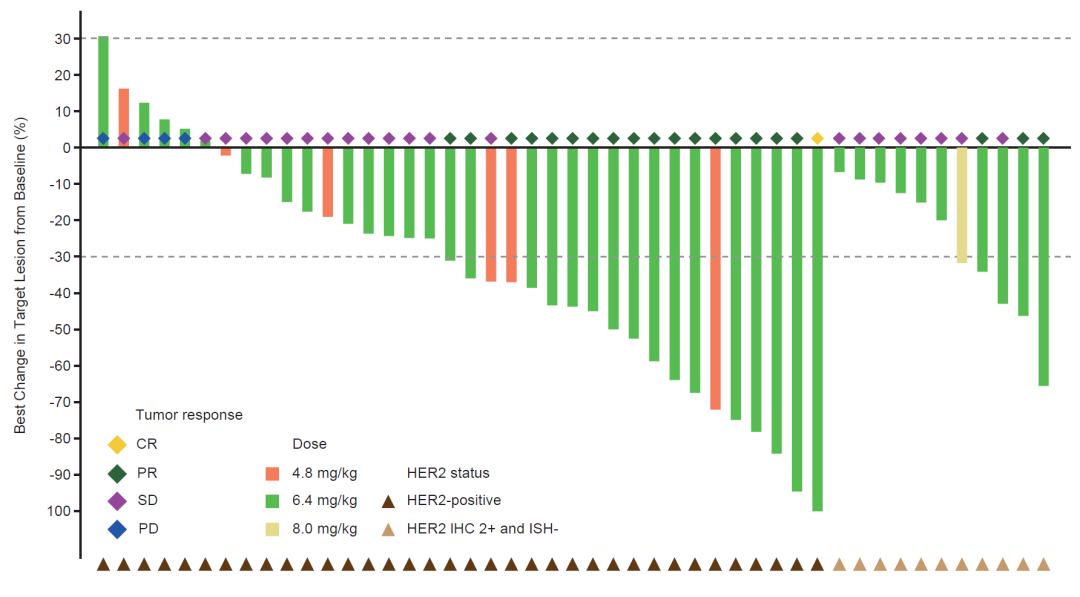
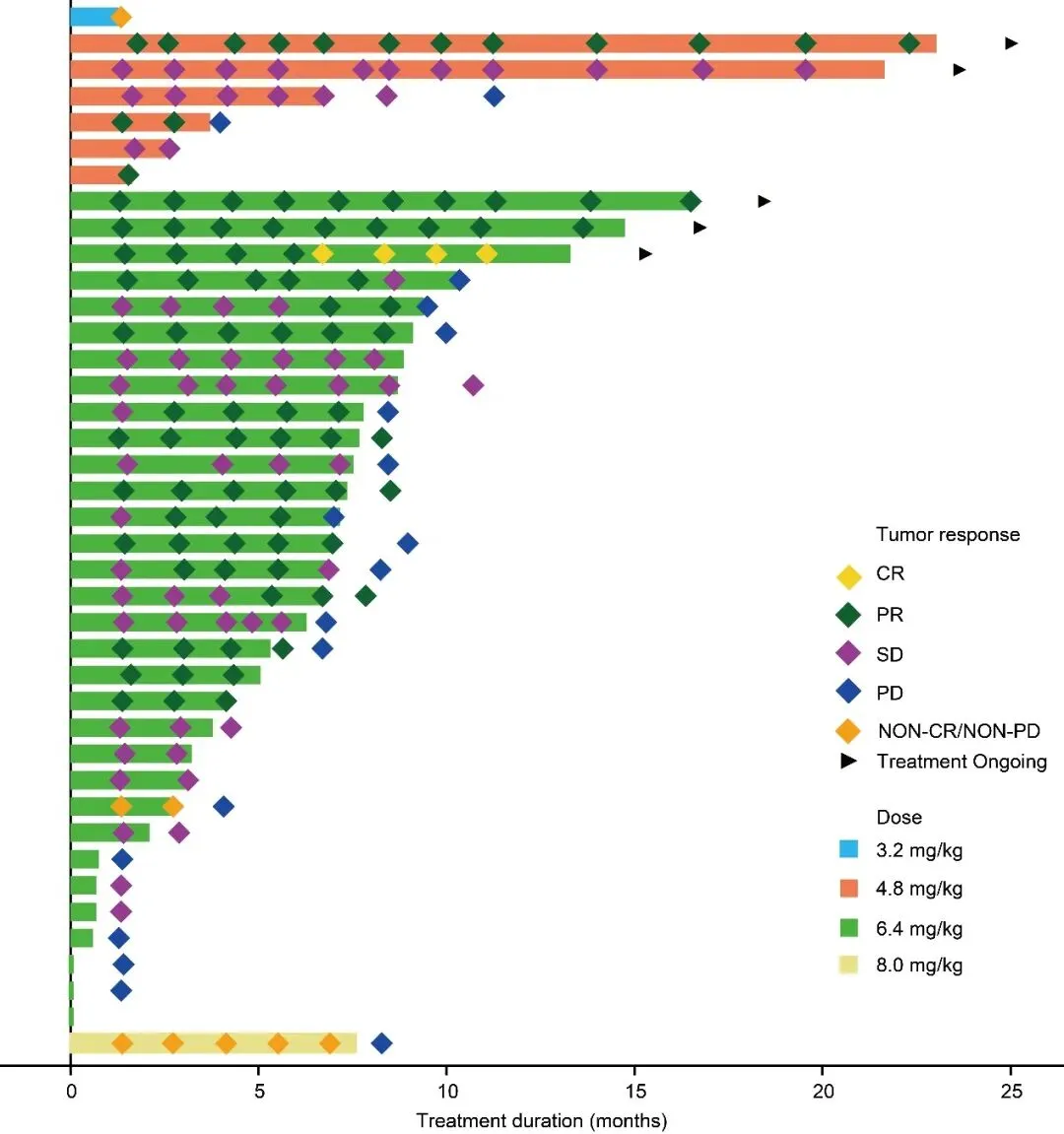
40 例 HER2 阳性 GC/GEJ 患者的 ORR 为 45.0%,DCR 为 87.5%,DoR 为 5.5 个月,中位 PFS 为 9.0 个月,中位 OS 为 16.3 个月,28 例既往接受过 HER2 治疗的患者中,14 例患者病灶得到缓解,ORR 为 50.0%;在 12 例 HER2 2+且 ISH-的 GC/GEJ 患者中,ORR 为 25.0%,DCR 为 91.7%,中位 PFS 为 12.2 个月,中位 OS 尚未成熟。
32 例接受 6.4 mg/kg GC/GEJ 患者 ORR 为 50.0%,DCR 为 84.4%,DoR 为 5.7 个月,中位 PFS 和中位 OS 分别为 8.4 个月和 16.3 个月。
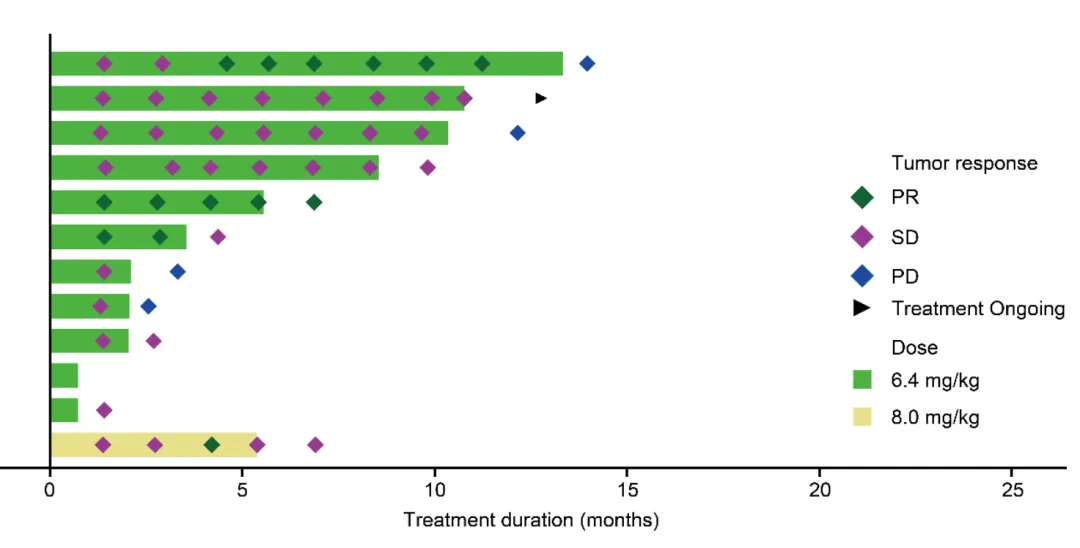
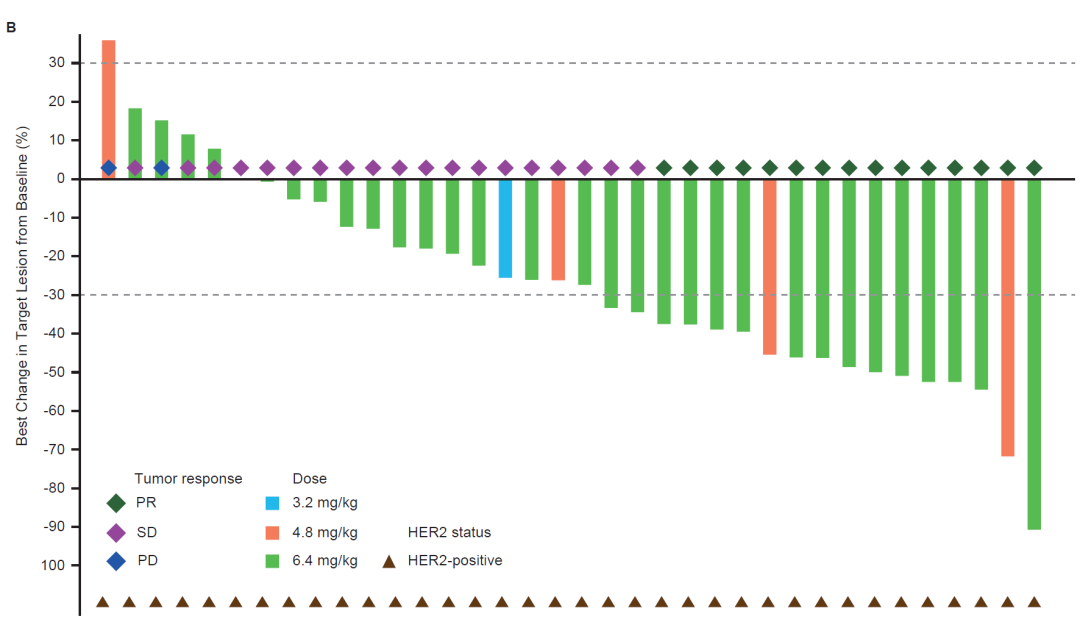
在 37 例 HER2 阳性 CRC 患者中,ORR 为 40.5%,DCR 为 91.9%,DoR 为 6.1 个月,中位 PFS 为 9.5 个月,中位 OS 为 22.7 个月,11 例既往接受过 HER2 治疗的患者中,4 例患者病灶得到缓解,ORR 为 36.4%。
32 例接受 6.4 mg/kg 剂量瑞康曲妥珠单抗治疗的 HER2 阳性 CRC 患者中,ORR 和 DCR 分别为 40.6% 和 93.8%,中位 PFS 为 9.5 个月,中位 OS 为 22.7 个月。
3、安全性
100 例患者中有 96 例(96%)发生了任何级别的治疗相关不良事件(TRAEs),66 例(66%)患者报告了 3 级或 4 级 TRAE。包括中性粒细胞计数减少(49 例,49%)、白细胞计数减少(39 例,39%)以及贫血(29 例,29%)。
有 33 例(33.0%)患者出现了严重 TRAEs,包括血小板计数降低(10 例,10.0%)、贫血(8 例,8.0%)以及中性粒细胞计数降低(7 例,7.0%)。
总结
综上,瑞康曲妥珠单抗在晚期 GC/GEJ 和 CRC 患者中显示出了良好的抗肿瘤活性和安全性。瑞康曲妥珠单抗用于 GC/GEJ 二线治疗的Ⅲ期研究(NCT06123494)正在进行中;其用于结直肠癌患者的新适应症上市申请已获得国家药品监督管理局药品审评中心(CDE)受理,并已纳入优先审评程序!期待未来给患者带来更多治疗选择。
参考文献
[1] Liu T, Luo S, Yuan X, et al. Trastuzumab Rezetecan in Human Epidermal Growth Factor Receptor 2-Expressing Advanced Gastric Cancer or Gastroesophageal Junction Adenocarcinoma and Colorectal Cancer: A Multicenter, Open-Label, Phase I Trial. J Clin Oncol. Published online March 4, 2026.
[2] Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024 Apr 4.
[3] Zhu K, Yang X, Tai H, Zhong X, Luo T, Zheng H. HER2-targeted therapies in cancer: a systematic review. Biomark Res. 2024;12(1):16
[4] Ingold Heppner B, Behrens HM, Balschun K, et al: HER2/neu testing in primary colorectal carcinoma. Br J Cancer 111:1977-84, 2014
[5] Van Cutsem E, Bang YJ, Feng-Yi F, et al: HER2 screening data from ToGA: targeting HER2 in gastric and gastroesophageal junction cancer. Gastric Cancer 18:476-84, 2015
好文章,需要你的鼓励
















