来源:首都医学科学创新中心
2025 年 12 月,首都医学科学创新中心(简称创新中心)资深研究员、肿瘤研究所副所长尤忠胜教授在国际期刊 Cell Reports 上发表文章 「Dual roles of TRPV2 in the innate immune response to cytosolic DNA: Arresting dormant and boosting activated STING」。研究发现,细胞内离子通道蛋白 TRPV2 像一个「智能开关」,既能牢牢锁住免疫「警报」防止误伤自己,也能在侦测到真正威胁时果断「踩下油门」,快速启动免疫反应。这一发现为自身免疫疾病(「刹车失灵」)和免疫逃逸的「冷」肿瘤(「动力不足」)提供了崭新的治疗方案和药物靶点。

我们的细胞里有一套「警报系统」(cGAS/STING 通路),专门监测不该出现在细胞里的 DNA(比如来自病毒或癌细胞自身的 DNA)。一旦发现,就会「拉响警报」,启动免疫应激。但这个系统不能误报,否则会误伤自己,导致自身免疫疾病;也不能反应太迟钝,否则无法有效抵抗病毒感染和癌症。科学家们想知道,这个精准调控的分子机制是什么?尤忠胜团队发现,离子通道蛋白 TRPV2 在其中起到关键作用。
在此前的研究中,尤忠胜团队发现了 STING 和离子通道蛋白 TRPV2 的在内质网上的相互结合,该结合正常情况下抑制 TRPV2 离子通道的活性。但在有 DNA 复制压力存在情形下,胞质 DNA 的产生促进了 STING 和 TRPV2 的解离,造成 TRPV2 激活,导致钙离子释放。这些释放的钙离子促进复制叉的保护,对基因组稳定性维护起关键作用(Li et al., Mol Cell 2019; Li, Kong et al., Mol Cell 2023; Kong, Cheng et al., Nat Commun 2024)。在此次研究中,团队发现 TRPV2 也反向调控 STING 的静息和激活,从而控制先天免疫反应。非常有趣的是,研究发现,TRPV2 同时具有「刹车」和「油门」的双重角色。在没有胞质 DNA 时,TRPV2 抓住「警报器」STING,把它锁在原地,防止错误启动,引发不必要的炎症或自身免疫疾病。当监测到胞质 DNA,「警报」系统会产生信号,让 STING 和 TRPV2 解离。被释放的 TRPV2 打开其离子通道,释放钙信号。这个钙信号促进 STING 转移到高尔基体,激活 TBK1 蛋白激酶,导致下游 I 型干扰素和多种细胞因子的表达,从而启动先天免疫反应。
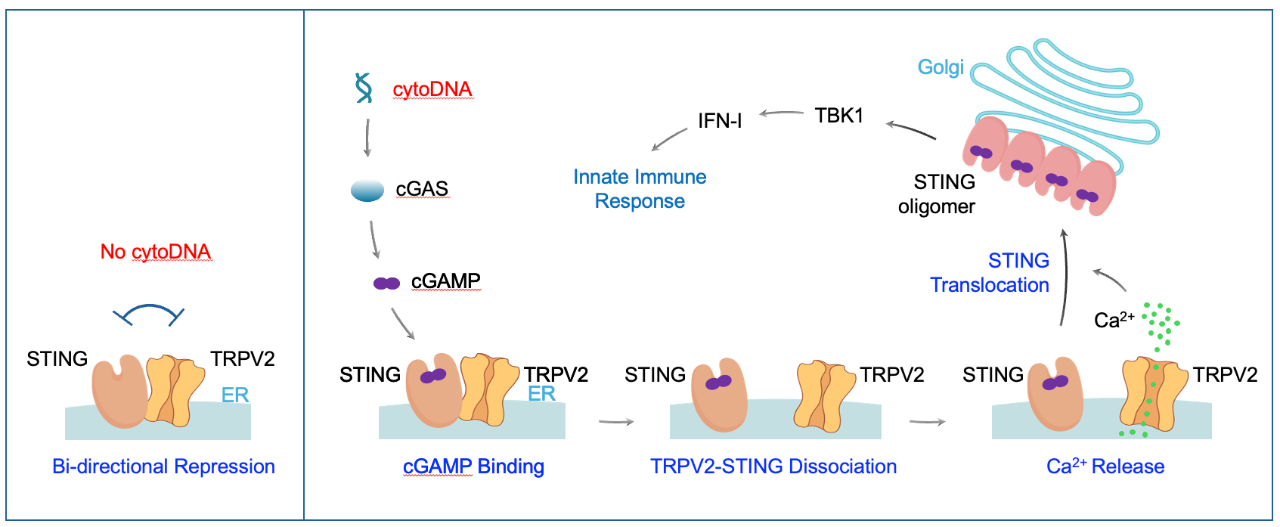
本研究首次发现 TRPV2 和钙离子信号直接参与 cGAS/STING 经典先天免疫通路的调控,通过蛋白之间的结合以及其离子通道的活性,TRPV2 既控制了 STING 的静息状态,防止误报,导致自身免疫疾病,也直接促进 STING 对胞质 DNA 信号的反应,确保「警报」迅速「拉响」。本研究中揭示的 TRPV2-STING 的互作,丰富了我们对免疫系统精巧调控和平衡机制的认识。
本研究对自身免疫疾病和癌症的治疗也具有重要意义:
治疗自身免疫病的新靶点:TRPV2 抑制剂可能能用于治疗因 cGAS/STING 持续错误激活造成的先天免疫疾病,比如 Aicardi-Goutieres 综合征、系统型红斑狼疮等。
提升癌症免疫治疗的新思路:通过破坏 STING-TRPV2 的结合,可以促进肿瘤微环境中 cGAS/STING 通路激活,让「冷」肿瘤变成「热肿瘤」,从而帮助现有的免疫疗法(如 PD-1 抗体和 PD-L1 抗体)更有效地清除癌细胞。
本研究的主要工作在华盛顿大学医学院完成,后续研究将在创新中心进一步开展。团队将通过动物模型研究,进一步深入验证 TRPV2-STING 互作对先天免疫系统的调控;解析 TRPV2-STING 复合物结构,进一步揭示其相互作用的分子机制;开发报告系统,筛选针对 TRPV2 及与 STING 互作的化学分子,进行药物开发和临床试验,用于治疗癌症和自免疾病。
专家介绍

尤忠胜
首都医学科学创新中心资深研究员、肿瘤研究所副所长
好文章,需要你的鼓励
















