让临床听懂科研,让科研看见临床
肾透明细胞癌(ccRCC)是泌尿系统最常见的恶性肿瘤之一,具有高侵袭性和易复发转移的特点。尽管手术是主要治疗手段,但约 20%-40% 的患者会出现复发。既往肾肿瘤研究多聚焦于单核苷酸变异,而对更大尺度的基因组结构变异(Structural variation, SV)和三维基因组结构的认知仍很有限。

1 月 6 日,浙江大学医学院附属第四医院泌尿外科张诚团队、肿瘤医学中心朱贵欣团队合作在国际权威期刊《npj Digital Medicine》(IF = 15.1,中科院 1 区)上发表题为 Structural variation drives enhancer hijacking via 3D genome disruption in ccRCC(肾癌结构变异破坏三维基因组结构驱动增强子劫持)的原创性研究成果。
这项工作首次在 ccRCC 中完整阐明了「结构变异破坏三维基因组-导致增强子劫持-激活癌基因」的连锁机制,为理解该疾病的发病根源提供了全新视角,并为未来的早期诊断、预后评估及靶向治疗开发奠定了关键的理论基础。
1、核心发现一:
绘制肾癌结构变异与三维基因组重塑图谱
研究团队利用前沿的纳米孔长读长测序技术,在肾癌细胞中鉴定出肾癌关键基因的新结构变异事件。同时,通过 Hi-C 技术发现,与正常细胞相比,肾癌细胞的三维基因组在区室(A/B compartment)、拓扑关联结构域(TAD)和染色质环(Loop)等多个层次发生了广泛的重构,这些三维结构的改变与致癌基因的异常激活显著相关。
2、核心发现二:
揭示「增强子劫持」致癌新机制
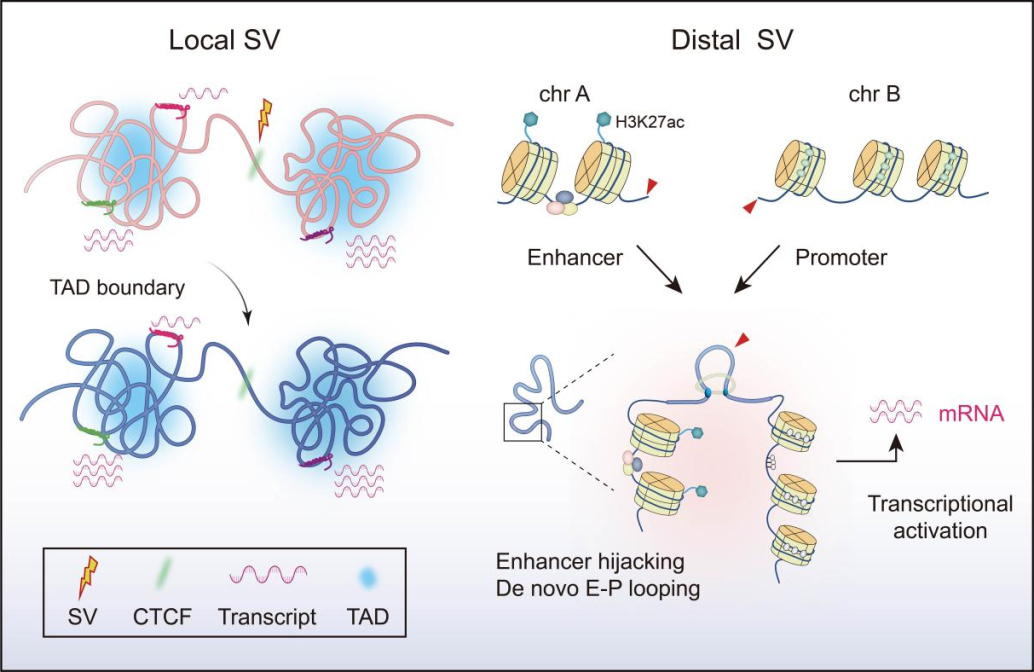
研究最具突破性的发现是阐释了结构变异导致「增强子劫持」的完整过程。团队发现,复杂的染色体重排(如倒位、易位)可以破坏原有的 TAD 边界,将远端增强子错误地置于原癌基因 SEMA5B 的启动子附近,形成全新的染色质互作环(neoloop),从而持续激活该基因。通过 DNA-FISH、PCR 及测序等多技术验证,证实了该结构变异及由此产生的新生染色质互作在癌细胞中特异性存在。
3、核心发现三:
验证 SEMA5B 为潜在治疗靶点
功能实验表明,SEMA5B 在 ccRCC 组织和细胞中特异性高表达。利用 CRISPRi 技术靶向抑制被「劫持」的增强子或 SEMA5B 启动子,可显著降低其表达,并有效抑制癌细胞的增殖、侵袭能力。动物实验进一步证实,干扰这一调控回路能够减缓肿瘤生长。这提示 SEMA5B 及其上游的异常调控机制可作为潜在的干预靶点。
基于上述机制发现,研究团队利用 TCGA 数据库,构建了一个基于增强子劫持相关基因特征的机器学习预后风险模型。该模型在预测 ccRCC 患者总生存期和无进展生存期方面表现出色,其预测效能超越了传统的 WHO 分级系统,为患者的精准风险分层和临床决策提供了新的工具。
通讯作者

张诚
浙江大学求是特聘医师 教授
主任医师 博士研究生导师
通讯作者

朱贵欣
浙江大学医学院「百人计划」研究员
第一作者

董宇
泌尿外科博士研究生
从事肾透明细胞癌的临床和基础研究
好文章,需要你的鼓励
















