来源:《临床儿科杂志》
作者:中国妇幼保健协会儿童变态反应专业委员会 中华医学会儿科学分会皮肤性病学组 《临床儿科杂志》编辑委员会
基金项目:浙江省「尖兵」「领雁」研发攻关计划项目
通信作者:李明,任韵清 电子信箱:mingli@fudan.edu.cn; yqren@zju.edu.cn
推荐引用格式:
中国妇幼保健协会儿童变态反应专业委员会,中华医学会儿科学分会皮肤性病学组,《临床儿科杂志》编辑委员会. 儿童特应性皮炎非药物干预管理专家共识 [J]. 临床儿科杂志, 2026, 44(5): 381-393 DOI:10.12372/jcp.2026.25e1596
Professional Committee of Child Allergology, China Maternal and Child Health Association, Dermatology and Venereology Group of Pediatric Branch Society, Chinese Medical Association, Editorial Board of the Journal of Clinical Pediatrics. Expert consensus on non-pharmacological interventions for atopic dermatitis in children[J].Journal of Clinical Pediatrics, 2026, 44(5):381-393 DOI:10.12372/jcp.2026.25e1596
摘要
特应性皮炎(AD)作为一种慢性、复发性的炎症性皮肤病,自 21 世纪以来,其在中国及国际范围内的发病率呈持续上升态势,已成为重要的公共卫生议题。AD 的综合管理体系主要涵盖药物治疗与非药物干预两大核心内容。尽管近年来 AD 的药物治疗方法不断丰富,但鉴于 AD 发病机制的高度复杂性以及显著的临床异质性,单纯依靠药物干预难以实现 AD 的最佳控制,非药物干预始终是 AD 防治的关键基础。目前,国内外已发表的 AD 治疗共识及指南中,干预策略多以药物治疗为核心架构,对非药物干预的系统性关注与整合明显欠缺。基于此背景,中国妇幼保健协会儿童变态反应专业委员会、中华医学会儿科学分会皮肤性病学组和《临床儿科杂志》编辑委员会,组织了来自 30 家医疗单位的 33 位皮肤科专家,依据当前国内外最新研究进展及临床实践经验,制定本项共识。本共识系统地阐述了 AD 的非药物干预管理策略,核心建议包括规避诱发因素、规范皮肤护理以维持皮肤屏障的稳定状态、落实健康教育与心理支持;强调了非药物干预作为 AD 管理基础措施的重要意义,旨在降低 AD 的复发率并提升患儿的生活质量;同时明确了各项措施的适用场景与实施要点,为临床工作者、患儿家属及健康管理人员提供了系统且实用的指导。
关键词
特应性皮炎;非药物干预;皮肤护理;皮肤屏障稳态;儿童
引言
特应性皮炎(atopic dermatitis,AD)是一种慢性复发性炎症性皮肤病,以剧烈瘙痒、湿疹样皮损及环境刺激高敏感性为特征,儿童多发,多数患者呈终身患病倾向。因常合并过敏性鼻炎、哮喘等其他特应性疾病,AD 被视为一种系统性疾病 [1]。AD 是全球最常见的皮肤病之一,其患病率高达约 10%~20%[2]。我国儿童 AD 患病率呈显著上升趋势,1~7 岁儿童患病率从 2002 年的 2.78% 增至 2014 年的 12.94%,婴儿期(1~12 月龄)高达 30.48%[3-5]。AD 使皮肤相关疾病负担沉重,据统计,AD 家庭年均总费用约 3 万元人民币 [6]。值得关注的是,AD 的皮肤表现常为特应性进程的起始,婴儿期 AD 会增加后续患儿哮喘(约 33%)[7]、过敏性鼻炎(约 45%)[8]、过敏性结膜炎(风险升高 8 倍)[9] 的发生风险,且常合并食物过敏 [10]。此外,AD 还与精神心理疾病、炎症性肠病、慢性阻塞性肺疾病、心血管疾病、代谢性疾病、肿瘤等非特应性疾病相关 [11]。
AD 的综合管理包含药物治疗与非药物干预两大核心。药物治疗虽为急性期及中重度病例的核心手段,但尚无任何药物可实现完全控制,且难以针对环境诱因、屏障修复及生活方式等上游环节进行干预。这些问题为探索更全面、更具针对性的 AD 管理策略(如非药物干预与药物治疗的协同整合)提出了需求与方向。AD 非药物干预通过规避诱发因素、修复受损皮肤屏障、调节皮肤微生态平衡等,贯穿 AD 治疗的始终,是 AD 长期管理中不可动摇的基石。AD 非药物干预可以减少药物依赖及相关副作用,降低疾病复发风险,具有重要意义。然而,现有指南多以药物治疗为核心框架,对非药物干预缺乏系统性阐述。虽有研究探索了 AD 的非药物干预措施,涉及皮肤屏障保护、规避诱发因素和改善菌群失衡,但尚未形成规范体系,也未阐明其适用场景、干预方法和效果评估。AD 发病机制复杂,包括遗传因素、环境因素、皮肤屏障功能障碍(包括物理结构屏障受损、化学酸性屏障异常、微生态屏障失调)等 [12-16],鉴于屏障功能障碍是 AD 发病的核心机制之一,本共识将系统阐述儿童 AD 非药物干预的适用情形、干预方法、作用机制及效果评估,为临床实践提供明确指导。
本共识运用改良德尔菲法 [17],组建核心撰写组,借助循证医学手段,以「特应性皮炎、非药物干预、皮肤屏障稳态、atopic dermatitis、skin care」等作为检索关键词,以 PubMed、EMBASE、Web of Science、万方数据库、中国知网数据库、全国团体标准信息平台等数据库为检索范畴,对 2000 年 1 月至 2025 年 9 月期间发表的 AD 患儿实践案例以及国际指南或共识展开调研,并参考相关领域专家意见,总结并初步拟定共识及推荐意见草案。同时,建立一个由皮肤病学、儿科学、妇产科学、流行病学等领域的 33 位专家组成的专家小组。经过三轮讨论达成最终意见:第一轮讨论,儿童皮肤科专家通过电子邮件等线上途径对每一条共识意见进行评估与反馈,撰写组收集专家反馈意见后,对《共识》进行调整与修改,完成《共识》初稿的撰写。第二轮讨论,专家小组采用电子问卷的方式,对每一条共识意见的同意程度进行评分(采用李克特量表,分为非常同意、同意、部分同意、不同意和非常不同意),以此确定是否达成「共识」。本共识规定,针对单条推荐意见,同意程度 ≥ 80% 即达成专家共识。第三轮讨论,汇总前一轮投票意见,依据专家意见对共识内容进行修改与补充,按需开展下一轮投票,直至达成共识。最后由专人对专家意见进行最终汇编,形成共识终稿。此外,经严格核查确认,所有参与本次共识制定的专家组成员,均不存在与本共识撰写内容相关的利益冲突。
1 儿童 AD 非药物干预管理的定义
特应性皮炎(AD)的非药物干预管理,指的是不依赖药物的干预举措,或作为药物治疗的辅助手段 [18]。AD 非药物干预管理的概念已逐渐受到关注。非药物干预管理以「减少刺激诱发因素、修复皮肤屏障」为核心措施,同时结合患儿教育、光疗、心理干预等手段,形成多维度干预体系。其目标是构建并维持皮肤结构完整和功能稳定的动态平衡状态,即皮肤屏障稳态,从而有效抵御外界刺激,减少 AD 的反复发作,提高患儿及家庭的生活质量 [19-24]。
推荐意见 1 对于 AD 患儿,无论疾病处于何种阶段(包括急性期、亚急性期及缓解期),均应将非药物干预管理作为基础手段。围绕「修复皮肤屏障」这一核心,综合运用减少诱发因素、强化患儿及家属教育、必要时采用光疗、配合心理干预等多维度措施,以实现皮肤屏障稳态为目标,从而有效减少 AD 的反复发作,持续提高患儿及家庭的生活质量。(同意率 100%)
2 非药物干预管理的效果评估
在 AD 的非药物干预管理中,疗效评估是验证干预措施有效性、判断儿童皮肤健康稳定状态的关键步骤,其核心在于对皮肤屏障稳态进行系统评价。依据应用场景,评估体系可划分为「临床评估」与「科研评估」两个层级。前者面向日常诊疗,进一步细分为临床医师的医学评估与患儿的主观评估;后者则适用于科学研究,强调客观、量化与可重复性。
2.1 临床评估
临床医师专业评估。皮肤屏障稳态的临床评估可关联 AD 严重程度的评价方法 [25],临床常用的有特应性皮炎评分(scoring atopic dermatitis index,SCORAD)、湿疹面积和严重程度指数评分(eczema area and severity index,EASI)、研究者整体评分法(investigator’s global assessment,IGA)、瘙痒程度视觉模拟尺评分(visual analogue scale,VAS)等 [26-28]。临床医师亦可采用简单易行的指标进行判断,如:轻度为皮损占体表面积<5%;中度为皮损占体表面积 5%~10%,或皮疹反复发作;重度为皮损占体表面积>10%,或皮炎呈持续性,瘙痒剧烈,影响睡眠 [29]。同时关注皮肤是否存在细菌、真菌、病毒等感染的临床表现,从临床角度判断其皮肤微生物屏障是否存在失调。
推荐意见 2 临床医师应将皮肤屏障稳态作为核心评价指标,结合 AD 严重程度评价方法开展医学评估。通过这些评估方式,全面、准确地掌握非药物干预措施的效果,为后续干预策略的调整提供依据。临床评估应以医师肉眼观察和问卷评分为基础。此外,还应关注皮肤微生物屏障状态,通过评估是否存在微生物(细菌、真菌、病毒)感染的临床表现,综合判断皮肤屏障稳态情况,为非药物干预措施的效果评价及方案调整提供依据。(同意率 100%)
患儿或照护者主观评价。家长作为患儿日常照护的核心参与者,其主观评价与记录手段不仅是临床医疗的重要补充,更是构建「医疗机构—家庭」协同管理体系的关键纽带。家长主观评价是儿童 AD 皮肤屏障稳态日常评估的重要手段,可从多维度辅助判断皮肤状态。常用的评估量表有患者湿疹自我检查评分表(patient-oriented eczema measure,POEM)、ADCT 评分(atopic dermatitis control tool,ADCT)、峰值瘙痒数字评定量表(peak pruritus numeric rating scale,Peak pruritus NRS)、皮肤病生活质量指数(children’s dermatology life quality index,CDLQI)等 [27-28]。家长的长期日常动态记录,如润肤剂用量记录、用药记录、饮食日记等也是重要的日常评估手段,可帮助医师追溯诱因、调整干预方案。
推荐意见 3 家长主观评价(如 POEM、ADCT、Peak pruritus NRS、CDLQI、润肤剂用量记录、饮食日记、用药日记等)是重要的日常评估手段。适用于所有医疗机构的诊断、分级与随访管理。(同意率 97%)
2.2 实验室评估
皮肤物理/化学屏障功能评估。经表皮水分丢失(trans-epidermal water loss,TEWL)是评估皮肤屏障功能的一项客观指标,其数值越高,提示皮肤屏障越弱,在临床研究中应用最为广泛 [30-31]。除 TEWL 外,还可测定皮肤角质层含水量 [32]、皮脂含量 [33],以综合评估皮肤的物理结构屏障。皮肤表面 pH 值测定用于评估皮肤酸性屏障功能 [31,34-35]。
皮肤微生态屏障功能评估。AD 的显著特征是皮肤微生物群落失衡加剧,表现为多样性降低,尤其是金黄色葡萄球菌显著增加 [36-38]。依据《皮肤微生态调节型化妆品功效评价团体标准》[39],评估分为:① 人体皮肤微生态评估方法。采用 16 S rRNA(细菌)或 ITS(真菌)扩增子测序及宏基因组测序。干预前后满足以下任一指标,且伴物理/化学屏障功能改善,即可支持微生态调节效应:a. 皮肤菌群多样性发生显著变化(P<0.05);b. 皮肤常驻菌群相对丰度发生显著变化(P<0.05);c. 皮肤机会致病菌相对丰度发生显著变化(P<0.05)。②特定皮肤微生物评价方法。包括体外抗菌测试、3D 皮肤模型和微生物共培养、其他皮肤微生态的相关体外实验评价等。最低抑菌浓度(MIC)测试和抑菌圈测试可用于评价刺激对特定微生物菌株的影响;3D 皮肤模型可在体外研究皮肤和微生物的相互作用。实验室与对照组差异显著(P<0.05)视为有效。
推荐意见 4 TEWL、皮肤角质层含水量、皮脂含量、皮肤表面 pH 值等仪器检测和微生态测序等技术,能提供客观、量化的数据,有助于更精准地评估,但对设备和专业知识要求高,适用于科研中心或有临床研究资质的机构。(同意率 94%)
3 非药物干预管理的措施及适用情形
非药物干预管理的措施包括核心措施和其他措施,不同措施的适用情形存在差异。
3.1 非药物干预管理的核心措施
3.1.1 规避诱发或加重因素 AD 的诱发因素繁多,可分为刺激因素和变应原因素,这些因素可通过受损的皮肤屏障入侵皮肤,引发炎症反应,从而诱发或加重 AD 症状。
①避免刺激因素。衣物面料是重要的刺激来源。100% 纯棉面料最为安全,部分标注「高棉含量」的混纺面料可能仍含有聚酯纤维等成分,建议在购买前查看成分标签以明确棉的实际占比。粗糙织物(如羊毛)及某些合成纤维衣物可刺激皮肤;传统大直径羊毛会引起瘙痒和刺激,超细或超超细美利奴羊毛因其纤维直径小、表面光滑,不易引起此类瘙痒反应,可作为普通羊毛制品的替代选项 [40-41]。此外,部分新型功能性面料,如纤维素基、壳聚糖涂层和银涂层织物,在减轻 AD 严重程度及减少金黄色葡萄球菌定植方面具有一定潜力,但是其长期效果和广泛适用性仍需更多证据支持 [42]。除衣物外,日常洗护用品也是不可忽视的刺激源。碱性的肥皂、洗涤剂等家用清洁产品会破坏皮肤天然油脂层,引发刺激;含色素、香料、防腐剂等个人护理产品也可能成为刺激源。
推荐意见 5 推荐选用柔软、透气、低刺激性的衣物面料,100% 纯棉最佳。个人护理产品应选择低刺激性产品。(同意率 100%)
②避免变应原因素。变应原因素包括吸入性变应原、食物变应原、接触性变应原。
吸入性变应原。常见的尘螨、宠物皮屑、霉菌及花粉等,经皮肤直接接触或吸入途径激活变应原特异性 IgE 与非 IgE 信号通路,可加剧炎症反应。室内最常见的吸入性变应原为尘螨、动物皮屑 [43]。若 AD 患儿合并哮喘和/或变应性鼻结膜炎,且皮炎季节性加重、环境改变后缓解,应考虑吸入性过敏 [44-48]。防控措施包括使用防螨床罩、高效过滤吸尘器,以及除螨剂 [49-51]。其他还包括减少室内毛绒玩具、厚重窗帘、地毯和羊皮制品,并定期清洗 [52]。当患儿接触宠物后症状加重,且患有鼻结膜炎和/或哮喘时,应怀疑存在宠物过敏原 [49,53]。可使用血清特异性检测 IgE 或过敏原提取物皮肤点刺试验(skin prick test,SPT)检测 [54]。确诊后根据严重程度决定是否回避。室外最常见的吸入性变应原为花粉 [43]。研究表明,接触草花粉会加剧 AD 的瘙痒和严重程度 [55-56]。症状春夏花粉季恶化,且随着花粉暴露减少而改善时,应怀疑花粉引起的过敏。建议采取关闭门窗、使用空气净化器、外出佩戴口罩和防护眼镜、返家后及时清洁皮肤和更换衣物的防护措施。
推荐意见 6 通过病史评估如接触后出现打喷嚏、咳嗽、喘息等症状,同时暴露部位皮肤出现皮损,提示可能存在吸入性过敏。皮肤点刺试验及特异性 IgE 抗体血液检测有助于识别致敏变应原。规避措施包括使用防尘床垫罩、移除地毯、高花粉浓度日减少外出。治疗措施可以使用润肤乳修复皮肤屏障,起到隔离过敏原接触刺激的作用。(同意率 100%)
食物变应原。在低龄儿童中常见鸡蛋、牛奶、花生等过敏,而年长儿童可能对茄科植物及食品添加剂等其他食物变应原敏感 [57]。食物通过经口、经皮两种途径诱发过敏,控制炎症、修复皮肤屏障可减少经皮致敏风险。同时建议家长通过饮食日记记录可疑食物与症状关联(包括食物种类、摄入量、症状出现时间及皮损照片)。若观察到症状加重(如进食后 24~48 小时内皮疹扩散、瘙痒加剧),不可自行长期回避,应提交完整记录由医师评估。必要时安排规范的食物激发试验,需在具备急救条件的医疗机构进行,以综合判断是否存在明确的食物过敏,以及该过敏与 AD 病情波动的直接关联。然而,通过双盲安慰剂对照口服食物激发试验(double-blind, placebo-controlled oral food challenges,DBPCFC)验证食物回避对 AD 症状改善轻微且可能无临床意义 [58]。不当的饮食回避可能导致儿童营养不良、生长发育迟缓,其危害甚至超过 AD 本身。在明确需要回避特定食物后,应根据患儿的年龄、营养需求及饮食偏好,选择营养价值相当的替代品,以保证营养均衡。研究表明,高风险婴儿早期(4~6 月龄)引入多种辅食有助于降低食物过敏风险 [59-61]。
推荐意见 7 AD 患儿盲目规避特定食物缺乏临床医学证据,对处于生长发育期的 AD 患儿具有重大的潜在不良影响。即使在具有明确特定食物过敏依据的前提下,也应综合考虑 AD 严重程度及其他相关临床问题,以决定是否需要饮食回避。(同意率 97%)
接触性变应原。指直接接触皮肤后引发过敏反应的物质。常见致敏物包括镍及多种生活常见用品成分(如芳香剂、消毒剂、防腐剂、新霉素、颜料、画笔、橡皮泥、黏土、沙土、特定的植物花草、软质玩具等)。特应性体质个体更易发生变应性接触性皮炎(allergic contact dermatitis,ACD)[62-63]。若患儿经规范的局部治疗无改善,或皮损范围超出常见部位持续扩散时,需警惕 ACD 的可能,必要时进行斑贴试验辅助诊断。
推荐意见 8 AD 应和 ACD 鉴别。若患儿经规范局部治疗无改善,或皮损范围异常扩散,应警惕合并 ACD,必要时通过斑贴试验明确诊断。临床应关注常见接触性致敏物,如镍、芳香剂、消毒剂等,降低变应性接触性皮炎风险。(同意率 97%)
微生物因素。AD 患儿由于表皮屏障功能障碍更易发生细菌、病毒及真菌感染。此类感染可作为并发症存在,在特定情形下也可能成为 AD 的诱发和加重因素。目前,细菌或真菌引发的变态反应在 AD 中的具体作用机制仍不明确。滥用抗生素会导致微生物群落失衡,诱导耐药菌产生,增加后续治疗难度。因此,在皮肤出现感染症状时,应首先到医院进行病原学检测,并严格依据医师指导及病原学检测结果合理选用抗生素。不推荐随意、长期或大面积使用外用及口服抗生素。对于轻度皮肤感染,可优先采取清洁、消毒等非药物干预措施进行处理,促进皮肤的自我修复 [64-66]。
推荐意见 9 鉴于 AD 患儿表皮屏障功能障碍易发生细菌、病毒及真菌感染,且感染可能诱发或加重病情,临床需重视感染的监测与干预。当皮肤出现感染症状时,应优先前往医院进行病原学检测,严格依据检测结果及医师指导合理选用抗生素,避免滥用导致微生物群落失衡及耐药菌产生。不推荐随意、长期或大面积使用外用及口服抗生素。(同意率 97%)
气候因素。季节更换时,特应性皮炎(AD)患儿常出现 AD 症状的反复或加重情况。寒冷且干燥的气候会致使皮肤干燥,进而引发皮肤屏障功能受损。而炎热潮湿的气候则会使出汗量增加,汗液直接刺激皮肤,加重 AD 症状。室内温度宜维持在 18~22℃,对于婴幼儿,可将颈部皱褶部位皮肤温热且无汗作为判断标准;对于大龄儿童,则以躯干核心部位皮肤处于温热无汗状态 [1] 为宜。室内湿度应保持在 40%~60%,可借助空调、加湿器等设备调节室内温湿度。需依据环境温度合理为孩子增减衣物,避免穿着过多、过厚,避免使用厚重被褥,睡眠环境应保持凉爽。运动时应让患儿穿着透气吸汗的衣物,运动出汗后,及时为患儿擦干汗液并更换干爽衣物 [67-68]。学龄期儿童活动量增大,汗液是常见的刺激诱发因素,及时擦拭汗液是避免诱发因素的关键。
推荐意见 10 季节变化易导致 AD 患儿症状反复或加重,寒冷干燥季节需要加强润肤,炎热潮湿天气则需要注意保持皮肤凉爽散热,但长时间空调环境仍会加剧皮肤水分丢失,也需要加强润肤。(同意率 100%)
环境污染物因素。空气污染物及香烟烟雾暴露也与 AD 症状恶化相关。烟草烟雾和交通尾气暴露被报道与 AD 相关 [69]。一项观察性研究表明,主动或被动吸烟均会增加儿童 AD 的患病率 [70]。应严格避免儿童接触烟草烟雾,并尽量减少高污染环境暴露。
推荐意见 11 应严格避免儿童接触烟草烟雾,同时尽量减少其在污染环境中的暴露,以降低 AD 症状加重的风险。(同意率 97%)
搔抓触发因素。搔抓通过破坏皮肤屏障、激活促炎因子形成「瘙痒-搔抓」恶性循环,是 AD 恶化的关键诱因。需积极运用药物治疗打断该循环,同时进行多种非药物手段管理。可采用分层管理策略:避免刺激因素,坚持保湿润肤;物理降温止痒。局部皮肤降温可经由 TRPM8 离子通道介导,缓解瘙痒症状 ;或用冷湿敷敷料外敷瘙痒处,或用冷水冲洗瘙痒处,临时缓解瘙痒。每次冷敷不超过 15~20 分钟,观察皮肤反应,不适即停。也可以按需涂抹冷藏后的润肤剂。行为干预包括剪短指甲、戴棉手套、识别搔抓前兆并用其他行为替代,如握拳、分散注意力 [71-73]。特别强调习惯逆转疗法 [74]。
推荐意见 12 药物治疗仍是控制「瘙痒–搔抓」恶性循环的核心手段,避免刺激诱发因素,加强润肤保湿、冷敷、行为干预等非药物干预管理措施不可或缺。(同意率 100%)
3.1.2 皮肤护理 皮肤屏障功能障碍是 AD 发病的关键病理生理学机制,在儿童主要表现为角质层屏障障碍、皮脂膜屏障障碍和微生态屏障障碍。科学的皮肤护理以皮肤清洁与润肤为核心,既是修复受损皮肤屏障的关键,也是非药物干预管理的核心措施 [75]。
(1)清洁。皮肤的清洁护理至关重要,但过度清洁会破坏皮肤屏障。应选择弱酸性、低刺激性、无香精且尽量不含皂基类清洁剂的产品(年龄 ≤ 12 岁的儿童选择清洁产品需认准「小金盾」儿童化妆品标识)[25,76]。洗浴频率为每日 1 次或隔日 1 次,每次 5~10 分钟为宜,水温以 32~37℃ 为宜,或参考患儿自觉不冷的最低温度 [1,25]。建议直接用手轻柔清洗皮肤,避免使用毛巾、海绵等粗糙物品用力摩擦。清洁时,要着重关注皮肤皱褶(如颈部、腋窝、腹股沟、股后部、肘窝、腘窝等)和尿布区等易藏污纳垢的部位,清洁后及时轻柔吹干或吸干。如皮损有感染倾向,可尝试稀释漂白浴以抑制细菌活性,临床常用方案为 0.005% 次氯酸钠(0.005%NaOCl,即 1∶1000 家用漂白水的典型做法)、每周 2 次,2023 年 AAAAI/ACAAI 指南将其定为「条件性推荐」,通常用于中重度 AD 且伴反复细菌感染患者 [77]。
推荐意见 13 AD 患儿的皮肤易受外界刺激物(如灰尘、汗液、污垢等)和病原体(如细菌、真菌)的侵袭。需要强调规范清洁可及时清除这些有害物质,降低皮肤受刺激引发的瘙痒、红肿等症状,并可减少感染风险,不可不清洁或过度清洁皮肤。(同意率 100%)
(2)润肤。润肤是 AD 患儿修复皮肤屏障的关键,具体方法为:①选择合适的润肤剂。建议选择无香精、低刺激性的润肤剂 [28],后生元作为皮肤微生态调节领域的重要研究方向,在皮肤保湿及屏障修护中表现出良好潜力。后生元是指对宿主健康有益的无生命微生物和/或其成分的制剂,常见类型包括短链脂肪酸、多肽、多糖、有机酸和脂质等 [78]。后生元能够介导微生物之间、微生物与皮肤之间的信息交流,为益生菌营造有利于定植的微环境,并激发和调节皮肤免疫应答 [79]。目前,部分保湿及护肤产品添加了乳酸菌发酵液、酵母菌发酵液等后生元成分,通过调节皮肤微生态,增强屏障功能 [80-81]。富含油酸的油脂(如橄榄油)因其会破坏皮肤屏障功能并增加 TEWL,不建议使用 [82]。在润肤剂剂型的选择上,皮肤轻度干燥者宜选用乳液,皮肤中重度干燥则建议使用霜剂。同时,还需结合患儿的偏好、季节特点及地域气候差异等因素,提供多种供患儿选用。②润肤剂应在清洁后 3~5 分钟内涂抹 [25],用手掌或手指均匀推开,以「轻拍」的方式,避免用力摩擦皮肤(尤其皮损处)。润肤剂需全身涂抹,以皮肤残留少量且不油腻为宜 [83-84],推荐 AD 患儿每周使用 150~200 g,每日至少涂抹 2 次;可根据皮肤干燥、脱屑程度,按需增加使用次数。除了常规涂抹,还可以进行湿包裹疗法。湿包裹疗法是指在使用润肤剂或外用糖皮质激素后,将湿绷带敷在皮损区域,以增强皮肤保湿、减轻瘙痒并促进药物渗透,虽然这可能会增加皮肤感染的可能 [85],但在儿童短期应用中这种风险并不显著,且在难治性 AD 中其疗效大于风险 [82]。为避免过度水合导致皮肤浸渍,湿包裹疗法连续使用不超过 7 天,同时需每日检查包裹部位是否有感染迹象(如脓疱、渗液)。③长期规范涂抹。润肤剂的使用需贯穿 AD 治疗的始终,症状改善后仍需继续长期全身涂抹。
润肤剂作为特应性皮炎(AD)非药物干预管理的关键措施,当皮肤出现瘙痒、红斑、丘疹等 AD 症状加剧的情况,或使用润肤剂无法改善病情时,应及时寻求专业医师重新评估 AD 诊断的准确性,同时避免陷入认为润肤剂可治疗所有 AD 的认知误区 [86]。针对皮肤出现糜烂、渗液等症状,需在专业医师指导下评估病情,并选择适宜的药物进行治疗。待皮肤糜烂、渗液得到控制后,需继续使用润肤剂;若合并感染(如出现红肿、脓疱),需在医生指导下先进行抗感染处理,待感染得到控制后再继续使用润肤剂。
推荐意见 14 科学润肤是修复受损皮肤屏障、减少疾病复发与症状加重的核心干预手段。临床实践中,润肤护理需严格遵循「温和、及时、足量、规律」四大核心原则,贯穿 AD 治疗的始终。(同意率 100%)
(3)防晒。AD 与日光照射有双重性,大多数患者能从紫外线辐射治疗、受控的自然环境中的日光照射中获益,据报道,约 10% 的患者会出现光敏感,需要光保护以降低 AD 症状反复的风险 [87]。应对 AD 患儿进行光防护教育,首选物理遮挡防晒,可结合使用防晒霜。物理遮挡防晒包括避开 10 点~16 点紫外线高峰,优先选择 9 点前或 16 点后外出,可通过「影子长度判断法」即影子短于身高时,紫外线过强需防晒;在紫外线温和时段,暴露背部、四肢伸侧等皮肤较厚区域,每次 10~15 分钟即可;佩戴帽檐宽度 ≥ 7 cm 的宽檐帽及太阳眼镜,遮挡面部、耳朵和后颈,穿着长袖透气防晒衣(优先选择 UPF50+的专业防晒面料,或纯棉、亚麻等紧密面料),覆盖手臂与腿部。按需选择物理型防晒霜,含氧化锌/二氧化钛,认准「小金盾」儿童化妆品标识)[88]。急性炎症期首选物理遮蔽,如需使用防晒霜,先在非皮损处小面积试用,确认无刺激后再全面部或曝光部位使用。
推荐意见 15 AD 患儿应该以物理遮蔽防晒为主。物理防晒霜相对温和,儿童需认准「小金盾」儿童化妆品标识。(同意率 97%)
(4)年龄及部位特异性皮肤护理要点。①婴儿期(0~2 岁)强调「无香精、低刺激性、霜剂优先」;头皮护理可采用「软化–轻柔清除」模式(如用润肤剂软化痂皮后,用弱酸性清洁用品温水轻擦,清洁后头皮皮肤使用轻薄的乳液剂型);尿布区选择 pH 值 5.5~6.0 的专用护臀膏,避免与躯干保湿剂混用;丙二醇和高浓度的尿素具有刺激性,避免应用于 2 岁以下婴儿 [87]。②儿童期(2~12 岁)针对活动量大、易出汗的特点,推荐「分层保湿」策略–躯干用乳液,关节褶皱处用霜剂;手部 AD 患儿需遵循「洗手–擦干–即时润肤」三步法,每次洗手后 30 秒内涂抹护手霜。③青少年(12~16 岁)关注面部护理与心理需求,推荐兼具保湿与轻度控油的舒缓类护肤产品,避免含酒精的清洁产品;针对痤疮合并 AD 的情况,明确「先修复屏障,再温和控油」的顺序。
推荐意见 16 目前尚无明确证据表明需对 AD 患儿的护理进行年龄特异性与部位特异性区分,但鉴于各年龄儿童 AD 皮肤护理的重点有所差异,各年龄儿童的护理要点也应进行区分。(同意率 100%)
3.1.3 非药物干预管理的核心措施贯穿 AD 治疗全周期 从预防阶段到急性发作期、缓解期均必不可少:①AD 的预防阶段。无论婴儿是否存在过敏性疾病家族史(如过敏性鼻炎、哮喘、过敏性结膜炎等),早期进行润肤护理均可降低发病风险 [89-91]。②轻度 AD。对于轻度 AD 患儿,可通过非药物干预管理的核心措施,修复皮肤的物理屏障、改善皮肤微生态屏障,进而减少复发、缓解病情 [19,89]。需对 AD 病情进行密切监测,若呈现加重趋势,应及时就医并向专业医师寻求诊疗建议。③中重度 AD。对于中重度 AD 患儿,必须在专业医师的指导下进行药物治疗,同时进行非药物皮肤干预管理。这种综合干预方式能够提高整体治疗效果,减少药物用量及其可能带来的潜在副作用,加速皮肤修复进程,有效降低疾病的复发风险 [89]。
推荐意见 17 非药物干预管理的核心措施应贯穿 AD 治疗全周期,从预防阶段、急性发作期到缓解期均必不可少,适用于不同严重程度的 AD。(同意率 100%)
3.2 非药物干预管理的其他措施
3.2.1 教育与心理干预 患儿教育在 AD 管理中占据关键地位。最新的 Cochrane 系统综述表明,个人和团体教育干预均可有效改善 AD 的症状。特别是团体教育计划更优。已有研究表明,专业、结构化的教育干预能使患儿及其照护者潜在获益 [92-93],包括帮助患儿认识疾病、规避诱发因素,规范基础护理、正确使用药物,关注饮食营养、进行随访和心理疏导等 [94-95]。可采用手册、讲座、在线课程或应用程序等形式,后者效果与传统面对面教育相当。AD 患儿合并 ADHD(9%)、抑郁(11%)、焦虑(14%)及自杀倾向(10%),其皮损表现还可能导致患儿面临社交孤立 [96-97]。推荐 AD 患儿家长加入互助小组,如微信患教群,分享经验,有助于解决共同顾虑、减少孤立感;并为 AD 患儿家庭提供支持,减轻照护者的心理负担,营造社区归属感与认同 [94]。放松技巧与身心整合干预亦可能改善 AD 症状并提升患儿生活质量。已有研究探讨了两类具体方法的应用:其一为渐进式肌肉放松法,即通过依次紧绷并放松身体各部位肌肉以实现放松效果;其二为身心精神干预法,该方法强调从身体、心理及精神层面进行综合照护。目前证据显示,上述心理学方法在缓解 AD 患儿压力、减轻焦虑情绪方面效果明确,但对 AD 症状的直接疗效待验证。当患儿出现显著焦虑抑郁情绪、严重睡眠障碍、社交功能受损、顽固性搔抓行为或家庭关系紧张等情况时,应在积极综合治疗的同时转诊至儿童心理科/精神科。
推荐意见 18 患儿教育与心理干预是 AD 非药物管理中不可或缺的措施,其中专业结构化患儿教育可使 AD 患儿显著获益。实践中可通过健康手册、专家讲座、在线课程及智能手机应用程序等多元形式,构建涵盖疾病知识科普、诱因规避方法、科学护肤要点、规范用药指导、合理饮食建议及定期随访要求的多维度教育体系;同时鼓励家长加入疾病互助小组,通过经验分享减轻患儿心理负担,并减轻个体与社会经济压力。(同意率 100%)
3.2.2 紫外线照射治疗 窄谱中波紫外线(NB-UVB)与长波紫外线 1(UVA 1)为临床常用的紫外线光疗手段,多作为 AD 的二线治疗方法,主要适用于局部慢性肥厚性或苔藓样变皮损。其中,12 岁以下儿童应避免采用全身紫外线疗法。光疗通常不适用于青春期前儿童,但并非绝对禁忌证 [1]。紫外线治疗不宜应用于急性皮损(尤其是渗液性皮损),否则可能致使病情恶化,应在实施标准治疗数日后再开展紫外线治疗 [33,98]。紫外线照射初期需进行最小红斑量测定,治疗频率为每周 2~3 次 [25]。
推荐意见 19 大多数临床试验和系统评价都以成人为研究对象;儿科数据稀少,且往往是从成人研究中外推而来的。尽管光疗已被证实有效,但由于存在光老化和潜在致癌性等长期不良反应的担忧,在儿童中应将其作为二线治疗方案保留。(同意率 97%)
3.2.3 臭氧水疗 一项临床研究纳入中度至重度双侧 AD 皮损患者,采用随机分侧干预设计:一侧采用臭氧水疗后外涂臭氧油方案,另一侧以自来水清洗后外涂基础油作为对照。结果表明,臭氧水疗组的 SCORAD 评分显著降低,AD 皮损区域的炎症细胞浸润明显减少,且皮肤微生物多样性显著增加 [99]。
推荐意见 20 臭氧水疗作为 AD 非药物干预管理措施之一,具有潜在应用价值,但目前相关研究较少,仍需更多循证医学证据支持。(同意率 82%)
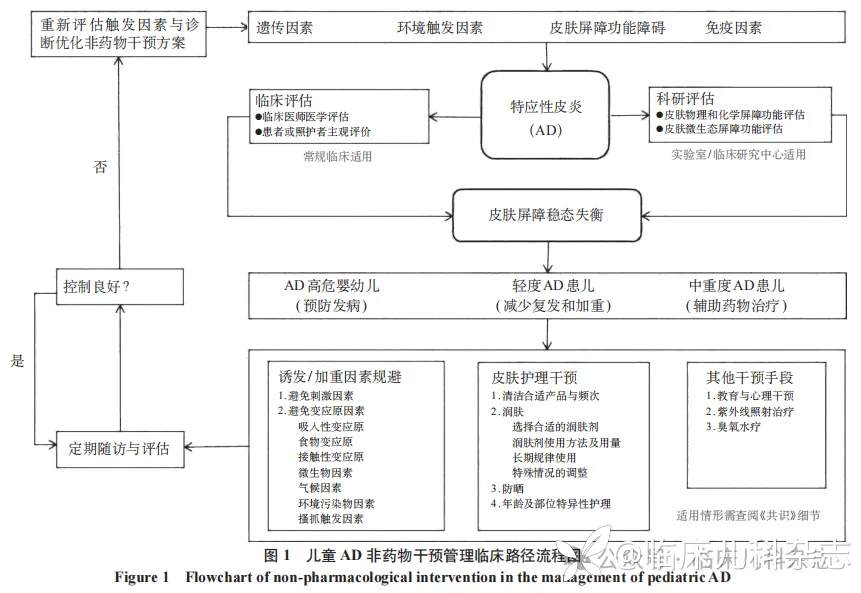
儿童 AD 非药物干预管理临床路径具体情况详见图 1。
4 总结与展望
儿童 AD 作为一种常见的慢性复发性皮肤疾病,严重影响患儿的身心健康与生活质量。本专家共识基于现有研究证据,系统阐述了儿童 AD 非药物干预管理的定义,构建了包含临床与科研双维度的效果评估体系,并明确了以规避诱发因素和科学皮肤护理为核心的干预策略及其适用场景。有效实施上述非药物干预管理措施,可显著改善患儿皮肤屏障稳态,降低 AD 发生率与复发率,切实改善患儿生活质量。展望未来,随着对 AD 发病机制研究的不断深化,以及皮肤微生态、免疫学等领域的突破性进展,非药物干预管理策略将向个性化精准医疗方向加速发展。基于个体皮肤微生态特征、遗传背景的个性化护理方案,以及新型功能性皮肤护理产品,如靶向调节皮肤微生态的后生元制剂、高效修复皮肤屏障的生物活性材料等有望成为 AD 综合管理的新方法。同时,强化家长与社会层面的健康教育,提高对 AD 非药物干预的认知与重视程度,积极构建「医–护–患–家庭」四方协同的管理模式,从而全面提升儿童 AD 的防治水平。
好文章,需要你的鼓励
推荐阅读
















