文章来源:高博医疗集团
肾细胞癌(RCC)诊疗领域在精准与联合的道路上大步前行,成果斐然:从改变局部晚期患者手术格局的围术期靶免新辅助治疗,到一线靶免联合方案的长期生存获益数据;从攻克耐药难题的后线创新疗法,到实现罕见非透明细胞癌亚型分子分型指导的精准诊疗策略,这些里程碑式进展共同推动肾癌治疗进入个体化、高效化的全新阶段。北京大学肿瘤医院/北京高博医院盛锡楠教授,立足国际学术前沿,对当前肾癌领域的关键突破与未来方向进行深度梳理与展望。
肾癌围术期治疗研究进展
1 新辅助治疗
2025 年肾癌新辅助治疗领域涌现出多项靶向联合免疫(靶免联合)及双免疫治疗的研究,旨在为高危局限期或局部晚期患者实现术前降期、优化手术方案并改善长期预后。既往开展的 NEOAVAX 研究 [1] 探索了高危局限性透明细胞肾细胞癌(ccRCC)术前使用阿维鲁单抗联合阿昔替尼的疗效。该研究纳入 40 例患者,结果显示 12 周新辅助治疗后,30%(12/40)的患者达到影像学部分缓解(PR),平均肿瘤缩小 20%。中位随访 52.9 个月后,中位无病生存期(DFS)为 25.1 个月。探索性分析 [2] 进一步发现,术后标本中 CD8+CD39+ T 细胞的高密度浸润与显著延长的 DFS 相关(P<0.0001),且达到主要病理缓解(MPR)的患者 DFS 更长,提示肿瘤微环境中的免疫应答与治疗获益密切相关。
对于瘤栓形成的局部晚期 ccRCC,国内学者开展了多项新辅助靶免联合治疗的探索 [3-5]。例如,II 期 NEOTAX 研究评估了特瑞普利单抗联合阿昔替尼用于伴有下腔静脉瘤栓患者的疗效。在 40 例患者中,治疗 12 周后 90%(36/40)的患者瘤栓长度缩短(中位缩短 1.9 cm),45% 的患者瘤栓分级降低,总体客观缓解率(ORR)为 37.5%。此外,54.3% 的患者因治疗有效而调整了手术方案,1 年 PFS 率达 87.5%,显示了新辅助治疗在实现肿瘤降期和创造手术机会方面的潜力。
在双免疫治疗方面,2025 年 ESMO 报道的 NESCIO 研究 [6] 评估了纳武利尤单抗单药、纳武利尤单抗联合伊匹木单抗、以及纳武利尤单抗联合 relatlimab 三种方案用于局部中高危 RCC 的新辅助治疗。初步结果显示,双免疫联合组(B 组和 C 组)达到了预设的主要终点(各有 14.3% 的患者达到近 pCR 或 pCR),而纳武利尤单抗单药组未达到。尽管第 6 周时大多数患者(40/42)表现为疾病稳定(SD),但双免疫方案在诱导病理缓解方面显示出优势,为优化新辅助免疫治疗策略提供了线索。
这些研究共同表明,新辅助靶免或双免疫治疗在高危或局部晚期肾癌中能够诱导显著的影像学和病理学缓解,改变肿瘤免疫微环境,并为部分患者带来手术可行性及生存获益。肿瘤微环境中的免疫细胞特征(如 CD8+CD39+ T 细胞密度)可能成为预测治疗反应的潜在生物标志物。
2 辅助治疗
对于术后复发风险较高的 RCC 患者,辅助免疫治疗已成为改善预后的重要策略。KEYNOTE-564 研究 [7] 的 5 年长期随访数据进一步巩固了帕博利珠单抗在此领域的标准地位。在中位随访 69.5 个月时,帕博利珠单抗辅助治疗组持续显示出显著的生存获益,与安慰剂组相比,其疾病死亡风险降低了 34%(OS HR 0.66,95% CI 0.48-0.90),无病生存期(DFS)持续改善(研究者评估:NR vs 68.3 个月,HR 0.71)。安全性特征与既往报告一致,未出现新的安全信号。
与此同时,III 期 RAMPART 研究 [8] 则探索了不同的辅助免疫方案。该研究比较了度伐利尤单抗单药(Arm B)、度伐利尤单抗联合替西木单抗(Arm C)与主动监测(Arm A)的疗效。在 ITT 人群中,经过 3 年中位随访,联合治疗组(Arm C)显示出 DFS 获益(HR 0.72; 3 年 DFS:75% vs 64%)。值得注意的是,预设的亚组分析表明,联合治疗对高危复发风险患者的获益尤为显著(交互作用 P = 0.019),对中危人群无显著获益。
综合 KEYNOTE-564、RAMPART 研究来看,两者基线人群特征相似,均以透明细胞癌为主,且包含中高危及 M1 NED(无疾病证据)患者。两项研究共同证实了辅助免疫治疗对降低术后复发风险的有效性,但方案与疗效存在差异:KEYNOTE-564 确立了帕博利珠单抗单药辅助治疗的标准地位,并拥有长达近 6 年的长期生存与安全性数据支持;而 RAMPART 研究则提示,对于特定高危人群,联合免疫治疗方案(度伐利尤单抗+替西木单抗)可能带来更深度的疾病控制,为个体化辅助治疗策略提供了新的选择。未来需要更长时间的随访数据来进一步明确联合方案的生存获益与长期安全性。

转移性肾癌系统治疗进展
1 晚期透明细胞癌一线治疗
晚期肾透明细胞癌(ccRCC)的一线治疗已形成免疫联合为主导的多元化格局,主要包括双免疫检查点抑制剂联合、免疫联合靶向(VEGF 抑制剂)以及新型三联方案等策略。
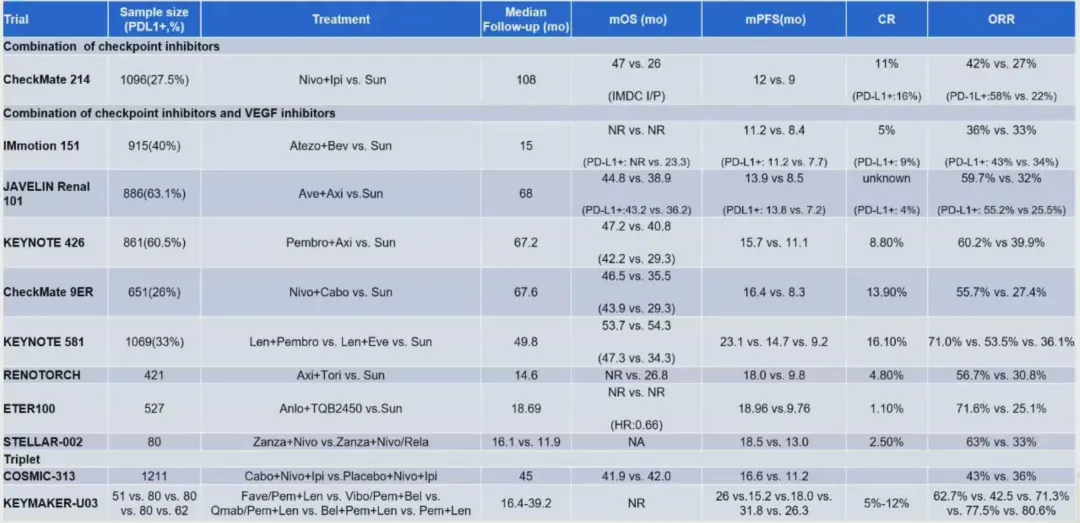
以双免疫联合为代表的 CheckMate 214 研究 [9-10] 长期随访(中位 108 个月)数据显示,纳武利尤单抗联合伊匹木单抗(NIVO+IPI)相比舒尼替尼(SUN)在 ITT 人群和中高危人群中持续显示出显著的生存获益,中位 OS 分别达 53 vs. 38 个月和 47 vs. 26 个月,8 年 OS 率分别为 31% vs. 20% 和 30% vs. 19%。该方案尤其在 PD-L1 阳性患者中客观缓解率(ORR)达 56%,完全缓解(CR)率为 12%,确立了其在特定人群中的长程疗效优势。如上表所示,既往报道的免疫联合靶向方案表现出较为广泛的适用性和突出的 PFS 获益。KEYNOTE-426(帕博利珠单抗+阿昔替尼)、CheckMate 9ER(纳武利尤单抗+卡博替尼)和 KEYNOTE-581/ CLEAR(帕博利珠单抗+仑伐替尼)等研究均显示出优于舒尼替尼的 PFS 与 OS 获益,其中仑伐替尼联合帕博利珠单抗的 PFS 长达 23.1 个月,ORR 达 71%。国产药物研究如 RENOTORCH(特瑞普利单抗+阿昔替尼)和 ETER100(TQB2450+安罗替尼)也显示出具有前景的疗效(mPFS 近 18.7 个月,ORR>56%),丰富了国内治疗选择。
为进一步提升疗效,多项研究探索了在双免疫或免疫靶向基础上联合第三种药物(TKI 或新型免疫制剂)的三联强化方案。然而,2025 年 ASCO-GU 报道的 COSMIC-313 研究 [11] 最终结果显示,在纳武利尤单抗联合伊匹木单抗的基础上增加卡博替尼,并未显著改善总生存(OS HR 1.02,P = 0.8366),且增加了毒性,提示单纯药物叠加未必能转化为生存获益。但探索性分析发现,肿瘤微环境中 M2 型巨噬细胞信号可能与三联方案疗效相关。与之相对,2025 年 ASCO 大会报道的 PDIGREE 研究 [12] 则采用了一种应答适应性设计(adaptive design),患者先接受 NIVO+IPI 诱导治疗,之后根据缓解情况分别接受纳武利尤单抗维持或联合卡博替尼,该策略旨在平衡疗效与毒性,其结果值得期待。
新型药物组合方面,2025 年 ESMO 报道 KEYMAKER-U03 子研究 03A[13-14] 探索了在帕博利珠单抗+仑伐替尼基础上联合抗 LAG-3(Fave)、抗 CTLA-4(Qmab)或 HIF-2α抑制剂(贝组替尼)的疗效。初步数据显示,联合贝组替尼组的 ORR 高达 77.5%,提示 HIF-2α抑制联合免疫靶向(贝组替尼+帕博利珠单抗+仑伐替尼)可能具有协同潜力。此外,贝组替尼在治疗 VHL 综合征相关肾细胞癌中也显示出卓越疗效(肾病灶 ORR 49%)[15-18],进一步印证了其靶向价值。
2 二线及后线治疗
随着一线免疫联合治疗的广泛应用,晚期肾透明细胞癌(ccRCC)的二线及后线治疗策略成为新的临床焦点。目前研究主要围绕免疫治疗进展后,如何通过新型靶向联合、不同抗血管生成药物组合或新型免疫靶点药物进行有效干预。
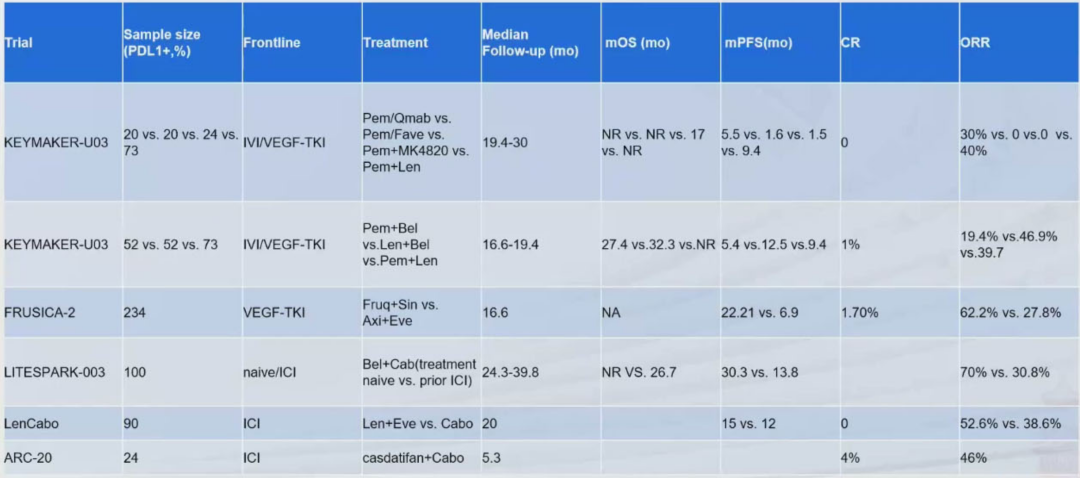
对于既往接受过 PD-1/PD-L1 抑制剂联合或不联合 VEGF-TKI 治疗后进展的患者,KEYMAKER-U03 子研究 03B[19] 探索了多种后续联合方案的疗效。其中,仑伐替尼联合新型 HIF-2α抑制剂贝组替尼显示出有前景的活性,客观缓解率(ORR)为 46.9%,中位 PFS 为 12.5 个月,中位 OS 达 32.3 个月。而帕博利珠单抗联合贝组替尼方案的 ORR 为 19.4%,mPFS 为 5.4 个月,提示在免疫治疗后继续使用 PD-1 抑制剂联合 HIF-2α抑制剂的增效作用可能有限。
在靶向治疗领域,2025 年 ESMO 报道的 III 期 FRUSICA-2 研究 [20] 评估了呋喹替尼联合信迪利单抗(FRUQ + SIN)对比阿昔替尼或依维莫司用于 VEGF-TKI 一线治疗失败的患者。结果显示,联合治疗组显著改善了 PFS(22.2 vs. 6.9 个月),疾病进展或死亡风险降低 63%,且 ORR 显著更高(60.5% vs. 24.3%),证实了免疫联合抗血管生成治疗在靶向治疗耐药后仍然有效。
针对免疫治疗(ICI)进展后的治疗选择,II 期 LenCabo 研究 [21-22] 首次进行了头对头比较。该研究显示,仑伐替尼联合依维莫司对比卡博替尼单药用于 ICI 治疗后进展的患者,能获得更高的 ORR(52.6% vs. 38.6%)和更长的 mPFS(15 vs. 12 个月),为临床序贯治疗提供了高级别证据。
此外,HIF-2α抑制剂贝组替尼与卡博替尼的联合方案在后续治疗中也显示出潜力。LITESPARK-003 研究的队列 2[23-25] 针对既往接受过免疫治疗的患者,贝组替尼联合卡博替尼的 ORR 为 31%,mPFS 为 13.8 个月,mOS 为 26.8 个月。值得注意的是,该联合方案在初治患者(队列 1)中疗效更为突出(ORR 70%,mPFS 30.3 个月),提示其前线应用价值。
3 转移性非透明细胞癌治疗
转移性非透明细胞肾癌(nccRCC)具有高度异质性,其治疗策略因不同亚型而异。近年来,多项临床研究探索了免疫联合、靶向治疗及基于特定分子特征的精准治疗,为该类患者带来了新的治疗希望。
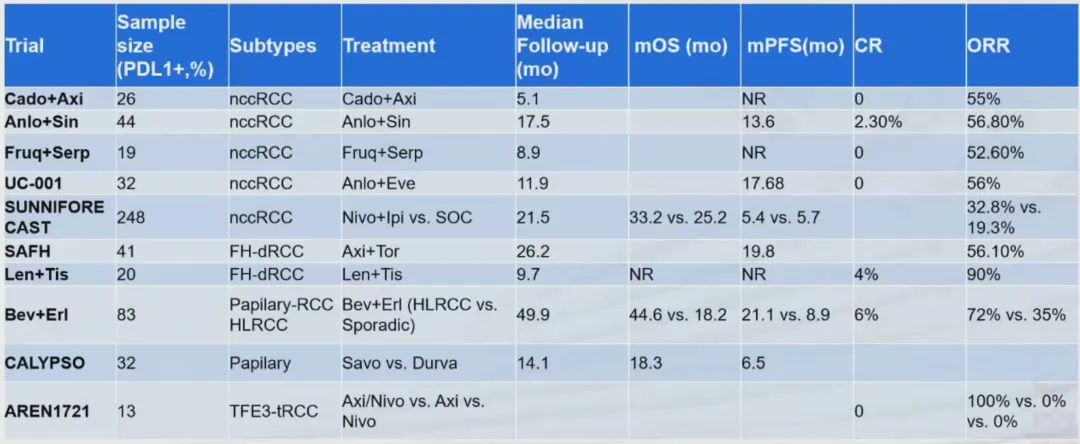
对于整体 nccRCC 人群,免疫联合治疗显示出一定疗效。II 期 SUNNIFORECAST 研究 [26] 对比了伊匹木单抗联合纳武利尤单抗(I/N)与研究者选择的标准化疗或靶向治疗(SOC)。结果显示,I/N 组在客观缓解率(ORR:32.8% vs. 19.3%)和 12 个月 OS 率(78% vs. 68%)方面均优于 SOC 组,中位 OS 也显示出延长趋势(33.2 个月 vs. 25.2 个月)。探索性分析提示,PD-L1 CPS ≥ 1 的患者可能从 I/N 治疗中获益更多 [27-28]。此外,如上表所示,多项小样本 II 期研究,如安罗替尼联合信迪利单抗(ORR 56.8%)、呋喹替尼联合斯鲁利单抗(ORR 52.6%)等,也初步证实了免疫联合抗血管生成治疗在 nccRCC 中的活性。
针对特定的 nccRCC 亚型,基于分子标志物的精准治疗取得了突破性进展。对于乳头状肾细胞癌(pRCC),II 期 CALYPSO 研究 [28-30] 评估了 MET 抑制剂赛沃替尼联合度伐利尤单抗的疗效。在总体人群中,该方案的 ORR 为 32%,中位 PFS 为 6.5 个月,中位 OS 为 18.3 个月。尤为重要的是,在 MET 驱动型患者中疗效显著提升(中位 PFS 和 OS 分别为 13.9 个月和 27.4 个月)。该研究还发现,循环肿瘤 DNA(ctDNA)状态与预后密切相关:基线 ctDNA 阳性患者中位 OS 更短(7.3 vs. 33.3 个月),而治疗中实现 ctDNA 清除的患者则获得了显著的 OS 延长(31.3 vs 7.2 个月)。
遗传性平滑肌瘤病和肾细胞癌(HLRCC)是一种由 FH 基因胚系突变导致的特殊类型 pRCC。一项 II 期研究 [31] 显示,厄洛替尼联合贝伐珠单抗在该类患者中取得了高达 72% 的 ORR,中位 PFS 和 OS 分别达到 21.1 个月和 44.6 个月,疗效优于散发性 pRCC 患者(ORR 35%)。
延胡索酸水合酶缺陷型肾细胞癌(FH-dRCC)是另一类与 FH 基因缺陷相关的侵袭性亚型。多中心 I 期 SAFH 研究 [32] 探索了信迪利单抗联合阿昔替尼一线治疗的疗效,结果显示 ORR 达 56.1%,中位 PFS 为 19.8 个月,且胚系 FH 突变患者较体系突变患者获益更显著(ORR:64% vs. 43%;mPFS:32.0 vs. 12.6 个月)。
结语
综上所述,2025 年肾癌诊疗研究取得全面进展:围手术期治疗方面,靶免联合新辅助策略显著改善了局部晚期(尤其伴癌栓)患者的肿瘤降期与手术结局;晚期一线治疗中,免疫联合靶向或双免疫方案的长期生存数据日益成熟,治疗选择更趋精准,同时以 HIF-2α抑制剂为代表的新型药物及联合方案不断拓展疗效边界;后线治疗涌现出多种破解耐药的有效组合;罕见亚型肾癌(如 FH 缺陷型、MET 驱动型 pRCC)的精准治疗也取得突破性进展。展望未来,生物标志物的深度探索、围手术期治疗模式的优化、新型免疫疗法(如双抗、ADC)的研发以及针对罕见亚型的全球合作,将是推动肾癌治疗格局持续演进的关键方向。
参考文献
[1] Bex A, et al. ASCO-GU2022 Abs289
[2] Bex A, et al. 2025ASCO Abs4509
[3] Huang JW, et al. J Immunother Cancer. 2024 Jun 11;12(6):e008475
[4] Gu LY, et al. Signal Transduct Target Ther. 2024 Oct 4;9(1):264
[5] Gu LY, et al. 2025ASCO Abs4535
[6] Burgers F, et al. 2025ESMO
[7] Haas NB, et al. 2025ASCO Abs4514
[8] Larkin J, et al. 2025ESMO
[9] Choueiri TK, et al. 2025ASCO Abs4505
[10] Motzer RJ, et al. 2025ASCO-GU Abs439
[11] Albiges L, et al. 2025ASCO-GU Abs438
[12] Zhang T, et al. 2025ASCO Abs4516
[13] Suarez C, et al. 2025ESMO
[14] Suarez C, et al. Annals of Oncology. 2025
[15] Jonasch E, et al. N Engl J Med. 2021 Nov 25;385(22):2036-2046
[16] Iliopoulos O, et al. Lancet Oncol. 2024 Oct;25(10):1325-1336
[17] Else T, et al. Clin Cancer Res. 2024 May 1;30(9):1750-1757
[18] Srinivasan R, et al. Lancet Oncol. 2025 May;26(5):571-582
[19] Albiges L, et al. 2025ASCO-GU Abs440
[20] Liu ZH, et al. 2025ESMO 2598MO
[21] Hahn AW, et al. 2025ESMO
[22] Hahn AW, et al. Annals of Oncology. 2025
[23] Choueiri TK, et al. 2023ESMO LBA87
[24] Choueiri TK, et al. Lancet Oncol. 2023 May;24(5):553-562
[25] Choueiri TK, et al. 2025ASCO-GU Abs549
[26] Bergmann L, et al. Ann Oncol. 2025 Jul;36(7):796-806
[27] Lothar Bergmann, et al. ESMO 2025
[28] Ahrens M, et al. ESMO 2025
[29] Suárez C, et al. J Clin Oncol. 2023 May 10;41(14):2493-2502
[30] Jackson-Spence F, et al. 2025ASCO-GU Abs444
[31] Srinivasan R, et al. N Engl J Med 2025;392:2346-56
[32] Zhang XM, et al. JAMA Oncol, 2025
专家介绍

盛锡楠
北京大学肿瘤医院
北京高博医院
主任医师,教授,博士生导师
北京大学肿瘤医院泌尿肿瘤内科副主任
北京高博医院黑色素瘤与肉瘤内科/泌尿肿瘤内科
中国抗癌协会泌尿生殖肿瘤整合康复专业委员会副主任委员
中国抗癌协会泌尿系统肿瘤专业委员会常委
中国临床肿瘤学会(CSCO)理事
中国临床肿瘤学会肾癌专家委员会常委兼秘书长
中国临床肿瘤学会尿路上皮癌专家委员会常委
中华医学会泌尿外科学分会临床研究学组副组长
国家肿瘤质控中心膀胱癌质控专家委员会委员
北京肿瘤防治研究会泌尿肿瘤分委会候任主任委员
北京医学会肿瘤分会常委
内容来源 | 肿瘤瞭望
好文章,需要你的鼓励
















