来源:临床儿科杂志
作者:沈子涵 1,2 张 钏 1 郑 雷 1 周秉博 1 田芯瑗 1 王玉佩 1 惠 玲 1,2
作者单位:1. 甘肃省妇幼保健院/甘肃省中心医院/甘肃省出生缺陷与罕见病临床医学研究中心;2. 甘肃中医药大学第一临床医学院
基金项目:甘肃省科技计划资助项目;兰州市科技计划项目
通信作者:王玉佩,惠玲 电子信箱:wang_yupei_jade@163.com,zyhuil@hotmail.com
推荐引用格式:
沈子涵, 张钏, 郑雷, 等. 基于 X 染色体失活分析探讨 2 例 X 连锁智力障碍 Bain 型患儿的临床与遗传学特征 [J]. 临床儿科杂志, 2026, 44(3): 192-201 DOI:10.12372/jcp.2026.25e0552
SHEN Zihan, ZHANG Chuan, ZHENG Lei, et al. Clinical and genetic analysis of two children with Bain type of X-linked intellectual disability caused by HNRNPH2 gene variations based on XCI analysis[J]. Journal of Clinical Pediatrics, 2026, 44(3): 192-201 DOI:10.12372/jcp.2026. 25e0552
摘要
目的 探讨 2 例 X 连锁智力障碍 Bain 型(MRXSB)患儿的临床表现及遗传学特征,分析 X 染色体失活(XCI)分析在基因型-表型关联中的作用。方法 以 2023 年 2 月和 2023 年 11 月因「全面性生长发育迟缓、智力障碍」就诊的 2 例女性患儿作为研究对象,收集先证者的临床资料,对先证者及其家系进行家系外显子组测序(trio-WES)及 Sanger 测序验证;通过 XCI 检测试剂盒分析甲基化敏感位点,结合毛细管电泳定量分析 X 染色体偏倚失活程度;应用生物信息学工具预测变异致病性。结果 2 例患儿分别为 11 和 10 月龄女性,均表现为全面性生长发育迟缓、智力障碍、肌张力低下及运动里程碑缺失,其中先证者 1 伴有喂养困难、吞咽障碍及屏气发作。trio-WES 提示 2 例患儿均存在 HNRNPH2 基因(NM_019597)c.616C>T(p.Arg206Trp) 杂合变异,Sanger 测序验证该变异均属新发变异。XCI 分析提示先证者 1 与先证者 2 均存在 X 染色体偏倚失活,偏倚率分别为 17.3% 和 14.0%。结论 本研究首次确诊了 2 例发病年龄<1 岁的 MRXSB 女性患儿,通过 XCI 分析发现患儿 X 染色体均发生偏倚失活,结合患儿较早、较典型的临床表型,推测患儿 XCI 偏倚程度可能与表型严重性相关。XCI 是女性 X 连锁智力障碍(XLID)临床异质性的核心调控机制,XCI 联合 trio-WES 对女性 XLID 早期诊断及预后评估具有重要价值。
关键词
HNRNPH2 基因; X 连锁智力障碍 Bain 型; 外显子组测序; X 染色体偏倚失活
引言
X 连锁智力障碍(X-linked intellectual disability,XLID)是一类由 X 染色体上基因致病性变异引起的以认知障碍和适应能力降低为主要临床特征的疾病 [1-2]。由于基因变异的类型、表观遗传学调控及 X 染色体随机失活模式等因素的差异,这类疾病通常表现出临床异质性,因此临床医师难以找到有力证据证明表型与基因型的相关性,并判断患儿疾病的严重程度 [3]。X 连锁智力障碍 Bain 型(intellectual disability,X-linked,syndromic,Bain type,MRXSB)(OMIM#300986)的致病基因为 HNRNPH2,该基因位于 X 染色体 q22.1 区,编码核不均一核糖核蛋白 H2(heterogeneous nuclear ribonucleoprotein H2,hnRNP H2),其致病性变异会导致 hnRNP H2 蛋白错误定位于细胞质 RNA 颗粒内并异常积累,最终导致一系列以神经发育障碍为主的退行性病变 [4]。MRXSB 的临床特征主要为生长发育迟缓、智力障碍、运动缺陷及肌肉骨骼问题,部分患者存在面部畸形、癫痫及孤独症谱系障碍,极少数出现早期卒中和过早死亡 [5]。本研究回顾性分析 2 例生长发育迟缓、智力障碍的女性患儿的临床资料,应用家系外显子组测序(trio-whole exome sequencing,trio-WES)结合 X 染色体失活(X-chromosome inactivation,XCI)检测,揭示其表型-基因型-XCI 相关性,为临床诊断提供依据。
1 对象与方法
1.1 研究对象
选取 2023 年 2 月及 11 月就诊于甘肃省妇幼保健院的 2 例 MRXSB 女性患儿及其父母作为研究对象。
1.2 研究方法
1.2.1 临床资料收集 收集患儿相关信息,包括基本情况(现病史、既往史、个人史及家族史)、体格检查情况、实验室检查结果、康复科评估信息及头颅磁共振成像(MRI)、脑电图等检查资料。
1.2.2 外周血基因组 DNA 提取 采集患儿及其父母外周血各 3 mL 置于 EDTA 抗凝管,使用基因组 DNA 提取试剂盒 [货号:DP304-02,天根科技生化(北京)有限公司] 提取基因组 DNA,用核酸浓度测定仪 NanoDrop 2000(美国 ThermoFisher Scientific 公司)测定 DNA 纯度和浓度,使浓度控制在 50~200 ng/μL,-20℃ 保存。
1.2.3 外显子组测序 采用 Roche KAPA Hyper Exome 芯片从外周血 DNA 中捕获基因组外显子区域并测序,测序深度 200×,通过国际千人基因组数据库(1000 Genomes, http://www.internationalgenome.org)、外显子组整合数据库(ExAC, http://exac.broadinstitute.org )等公共数据库筛选变异,根据美国医学遗传学与基因组学学会(American College of Medical Genetics and Genomics,ACMG)发布的《ACMG 遗传变异分类标准与指南》对候选变异的致病性进行评估 [6]。
1.2.4 Sanger 测序验证 根据外显子组测序(WES)检出的候选变异,对患儿及其父母进行 Sanger 测序验证,针对 HNRNPH2 基因(NM_019597)c.616C>T(p.Arg206Trp) 变异位点设计引物,正向引物序列为 5』-CAAGGAAGAGATTGTTCAGTTCT-3』,反向引物序列为 5』-CTATAATGATGGATATGGCTTTGG-3』,产物大小 398bp。PCR 反应体系:2×PCR-Mix 12.5μL,ddH2O 10μL,DNA(50~70ng/μL)1.5μL,正反向引物(10μmol/L)各 0.5μL,总体积 25μL。用琼脂糖凝胶 DNA 回收试剂盒 [货号:DP219-02,天根科技生化(北京)有限公司] 对 PCR 扩增产物进行纯化后,用 ABI-3500 DX DNA 测序仪测序,应用 Snap gene 软件对测序结果进行比对分析。
1.2.5 致病性变异生物信息学分析 应用罕见病数据库(Rare Disease Database,https://rddc.tsinghuagd.org/zh)、多态性表型预测工具(polymorphism phenotyping v2,PolyPhen-2, http://genetics.bwh.harvard.edu/pph 2)及深度测序突变预测工具(Mutation Taster, https://www.mutationtaster.org)等对该位点致病性进行分析。利用美国通用蛋白质资源数据库(the universal protein resource,UniProt,https://www.uniprot.org)获取 hnRNP H2 蛋白在不同物种间氨基酸序列,应用 SnepGene 软件进行氨基酸序列保守性分析,应用在线蛋白三维建模工具 SWISS-MODEL(https://swissmodel.expasy.org)对蛋白结构进行预测,并应用蛋白结构可视化工具 Pymol v2.3.0 软件( https://www.pymol.org)对蛋白三维结构进行可视化分析。
1.2.6 X 染色体随机失活分析 采用 XCI 检验试剂盒(XCIFiler)(货号:G011-15,上海晶准生物医药有限公司),利用多重聚合酶链反应(PCR)-毛细管电泳 DNA 片段分析技术,对 2 个家系 X 染色体上 4 个伴随甲基化酶切敏感位点的多态性遗传标记进行扩增,通过计算酶切前后等位基因峰高比值判断 XCI 状态。按试剂盒说明判读:若 XCI<25% 时,X 染色体呈非随机失活状态(偏倚失活),若 XCI ≥ 25% 时,X 染色体呈随机失活状态。同时用短串联重复序列(short tandem repeat,STR)分析方法的 5 个 X 多态性位点构建家系 X 染色体单倍型。PCR 产物均通过 ABI-3500DX DNA 测序仪毛细管电泳分离,使用 GeneMapper 软件进行结果分析。
2 结果
2.1 临床资料
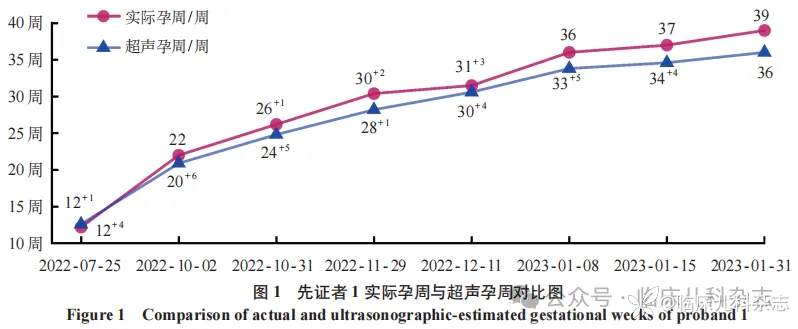
先证者 1 为 11 月龄女性,系 G2P2,足月顺产娩出,出生体重 3.2 kg,头围 32.6 cm,身长及 Apgar 评分不详,分娩过程无异常,无窒息缺氧抢救史。母亲孕早期产检未见异常,孕 20 周起超声孕周小于实际孕周(图 1),其体重、双顶径、头围、腹围及股骨长位于正常范围内,余未见异常,否认孕期服用药物、毒物及放射性物质接触史,否认妊娠期高血压、糖尿病及甲状腺疾病等病史。患儿 1 月龄行体格检查提示其发育落后于同龄儿童,通过母乳成分分析、喂养行为及膳食评估排除了喂养行为异常;2 月龄行口腔评估提示患儿口腔感统功能敏感性低;3 月龄头部控制欠佳;6 月龄俯卧位手肘支撑差,不会翻身,扶坐差;7 月龄出现吞咽困难,患儿拒食,食量下降;8 月龄全身肌张力偏低,无自主翻身活动,不能手支撑,喂养困难,并伴发音障碍及感觉过敏现象(对声光刺激呈现过度觉醒反应),发育过程中未见行为及精神问题(如孤独症谱系障碍、注意缺陷与多动障碍)及睡眠障碍。患者父母体健,非近亲结婚,无特殊家族史,有一兄,足月顺产娩出,现 4 岁,体健。
2023 年 11 月,患儿因「哭闹诱发屏气发作」就诊。患儿于入院前 10 天因情绪激动(剧烈哭闹)出现发作性症状 1 次,具体表现为意识不清,口唇发绀,双眼上翻,双手握拳,四肢及躯干僵直伴短暂震颤,无口吐白沫或小便失禁,无发热,症状持续约 10 分钟,自行终止,缓解后患儿乏力,就诊于当地医院,给予吸氧治疗。入院前 1 天,患儿于哭闹时再次屏气发作伴姿势性强直,表现同前,遂就诊于本院。体格检查:体重 7.8 kg(<-3SD),身长 78 cm(<-3SD),头围 40.2 cm(<-3SD)。患儿神志清,精神可,头颅五官无特殊,心、肺、腹查体未见异常,生殖器发育正常。患儿双手抓握能力差,不能独坐及翻身,头控尚可,偶有饮水呛咳,全身肌张力偏低,肌力减弱,腱反射正常,病理反射未引出,脑膜刺激征阴性。脑电图:清醒期背景 3.5~4.0 Hz θ波活动稍增多,提示界限性脑电图。头颅 MRI 平扫未见异常。神经发育评估:Alberta 婴儿运动量表(AIMS)评分 17 分,粗大运动小于第 1 百分位;Gesell 发育量表评分:适应性 51 分,大运动 38 分,精细动作 40 分,语言 40 分,个人-社交 47 分,综合 43.2 分,落后于正常年龄 6 个月,为中度发育迟缓。入院给予营养神经等对症支持治疗,其间无屏气发作。出院时诊断为 HNRNPH2 基因变异相关 X 连锁智力障碍(Bain 型)、全面性发育迟缓(中度)、中枢性肌张力低下、吞咽功能障碍、屏气发作。
患儿出院后于本院规律康复治疗 6 月余,给予患儿颈、腰部及四肢功能综合训练,感觉和综合训练、身体功能障碍作业治疗及经颅磁刺激等综合康复治疗,经治疗后患儿可独坐 1 分钟,双手粗大抓握能力较前提高,可扶物站立 1 分钟左右。Gesell 发育量表评分:适应性 57 分,大运动 22 分,精细动作 47 分,语言 49 分,个人-社交 51 分,综合 45.2 分,落后幅度由 6 个月扩大至 7.2 个月,提示神经发育迟缓进行性加重,后期患儿再无屏气症状发作。
先证者 2 为 10 月龄女性,系 G3P3,于孕 40+5 周因「瘢痕子宫合并胎儿窘迫 1 天」经剖宫产娩出,出生体重 2.3 kg(<-2SD),头围 30.2 cm(<-2SD),身长 47 cm(<-2SD),Apgar 评分生后 1 分钟 9 分、5 分钟 10 分,羊水清、量中,无脐带缠绕情况,胎盘正常,分娩过程无异常。母亲孕期产检未见异常,否认孕期服用药物、毒物及放射性物质接触史,否认妊娠期高血压、糖尿病及甲状腺疾病等病史。患儿自幼生长发育落后,2 月龄手部无抓握意向,口腔感觉迟钝;3 月龄头控不稳,无俯卧抬头;5 月龄无翻身,抓物笨拙,无应答声;6 月龄不可独坐,无翻身能力;7 月龄食量减少,无精细动作,发育过程中未见行为及精神问题、癫痫及睡眠障碍。父母体健,非近亲结婚,无特殊家族史,患儿有 2 个姐姐,均为足月剖宫产娩出,现体健,未见发育迟缓。
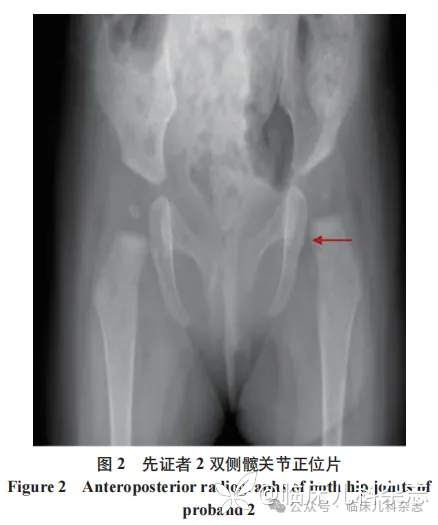
2023 年 2 月,患儿因「生长发育落后」就诊于本院门诊。体格检查 :体重 6.5 kg(<-2SD),身长 65 cm(<-1.5SD),头围 41.3 cm(<-1.5SD)。患儿一般状况可,精神好,头颅五官无特殊,心肺腹查体未见异常,生殖器发育正常。患儿四肢肌力弱,抬头 30 度,自主翻身不能,坐位前倾,前臂旋前,精细运动欠佳,拇指内收。腱反射正常,病理反射未引出,脑膜刺激征阴性。双侧髋关节 X 线正位片:双侧股骨头骨化中心发育不良,左侧髋关节 Shenton 线欠连续(图 2),头颅 MRI 未见明显异常。Gesell 发育量表:大运动 27 分,精细动作 20 分,适应性 27 分,语言 30 分,个人-社交 30 分,综合 26.8 分,落后于正常年龄 9 个月。家庭康复 2 个月后门诊复诊,患儿体重 7.3 kg(<-3SD),身长 67 cm(<-1.5SD),头围 42.0 cm(<-2SD),运动功能无进步(全身肌力弱,仍无法翻身、独坐,俯卧位支撑弱),关节问题加重(左下肢短缩、扶立位足外旋),右侧拇指持续内收影响精细动作。之后患儿失访。
2.2 基因检测与生信分析
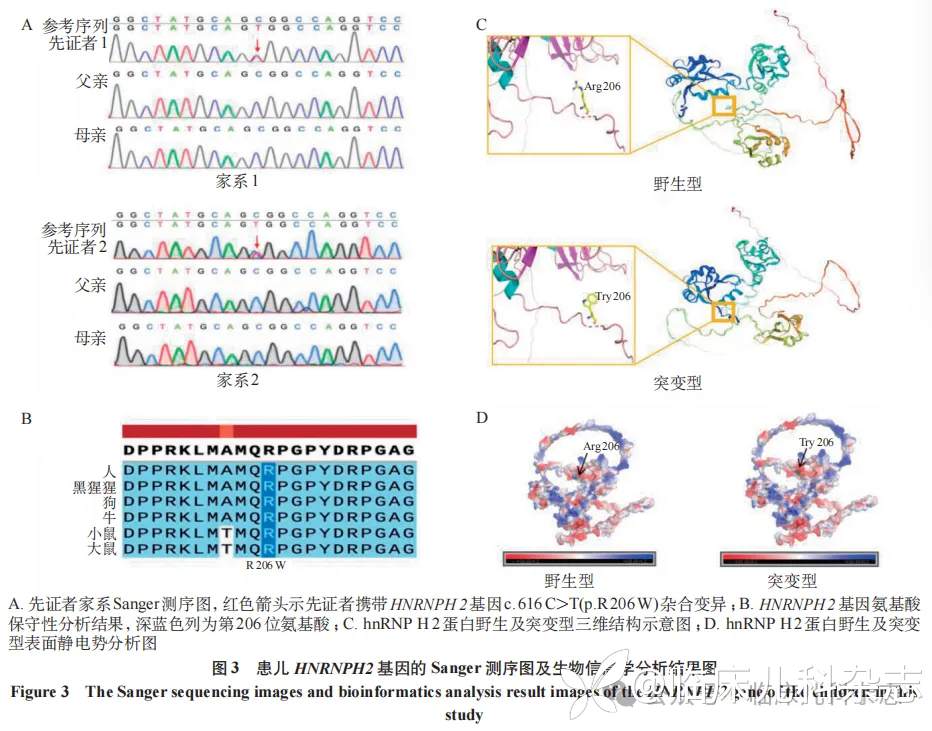
WES 提示先证者 1 和先证者 2 均存在 HNRNPH2 基因 c.616C>T(p.Arg206Trp) 杂合变异,为新发变异,关联疾病为 MRXSB,Sanger 测序验证证实上述变异,且父母均为野生型(图 3A)。该变异在 ClinVar 数据库收录,PubMed 数据库报道为致病性。根据 ACMG 指南,该变异评级为致病性(PS4+PS2_Very Strong+PP2+PP3+PM2)。具体证据包括:①变异在受影响个体中的发生率显著高于 gnomAD 对照人群中的发生率(PS4);②经双亲验证为新发变异且无家族史,患者临床表型与基因关联一致(PS2_Very Strong);③在 ESP、千人及 ExAC 数据库中人群频率对于显性遗传等位基因频率都为 0,对于隐性遗传的突变频率允许是低频(PM2);④该基因在 HGMD 数据库及 ClinVar 数据库中致病/疑似致病变异数 ≥ 10,且其中错义变异占比 ≥ 50%,良性/疑似良性变异占比不高于 10%(PP2);⑤ PP3 :经多种软件预测有害(SIFT 预测 0 分,提示有害;REVEL 评分 0.92,提示有害;PolyPhen2 评分 1 分,提示可能有害;CADD 评分 22.5,提示有害),通过 UniProt 数据库获取多物种序列比对显示该位点高度保守(图 3B)。通过 SWISS-MODEL 构建野生型及突变型 hnRNP H2 蛋白三维结构模型可见,突变没有改变蛋白质分子中的氢键网络,其二级结构未发生明显扭曲(图 3C);突变使静电势绝对值略微增加,提示突变可能轻微增强局部负电性,从而影响 hnRNP H2 蛋白与核转运蛋白的结合及转运效率(图 3D)。
2.3 X 染色体随机失活分析
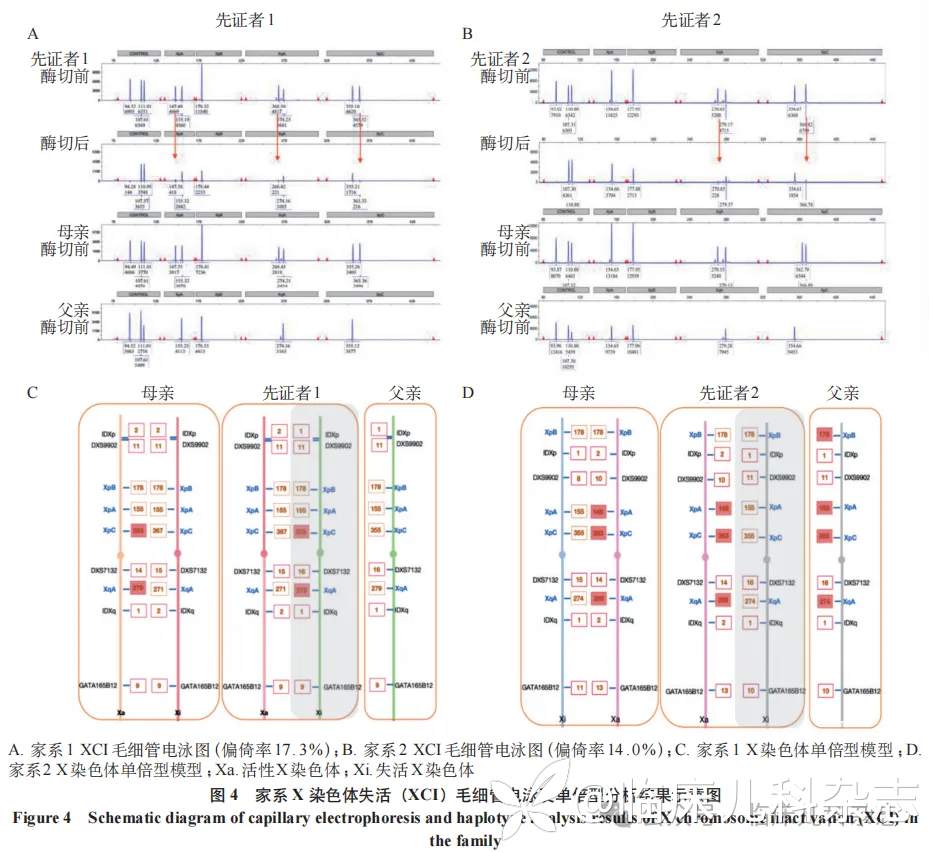
根据 4 个伴甲基化酶切敏感的多态性遗传标记分析 2 例患儿家系 X 染色体随机失活模式,分别计算各位点 XCI 值并计算其算术平均值,作为该样本 XCI 最终检验结果。经计算,2 例患儿均存在不同程度 X 染色体偏倚失活情况:先证者 1 的 XCI 比例为 17.3%,为母源性 X 染色体优先保留活性,父源 XCI 比例较高;先证者 2 的 XCI 比例为 14.0%,为母源性 X 染色体优先保留活性,父源 XCI 比例较高(图 4)
3 讨论
XCI 是雌性个体中关键的剂量补偿机制,通过随机沉默父源或母源 X 染色体并形成失活的巴氏小体,以确保两性间 X 连锁基因表达的平衡,其分子基础依赖于 X 染色体失活特异转录因子(X-inactive specific transcript,XIST)基因启动的非编码 RNA 介导的染色质重塑及 DNA 甲基化修饰 [6]。XCI 的随机性对两性发育至关重要,在正常女性中,父源性与母源性 X 染色体保持活性的比例接近 50%,仅少数个体因随机波动或选择压力出现 X 染色体偏倚失活(通常定义为某一亲本源占比 ≥ 75%)。对于 X 连锁性遗传病,XCI 模式决定变异基因的表达比例,直接影响疾病严重程度,其临床意义涵盖疾病诊断、预后评估、治疗靶点探索等多个层面,对罕见遗传病的研究具有重要指导价值 [7]。
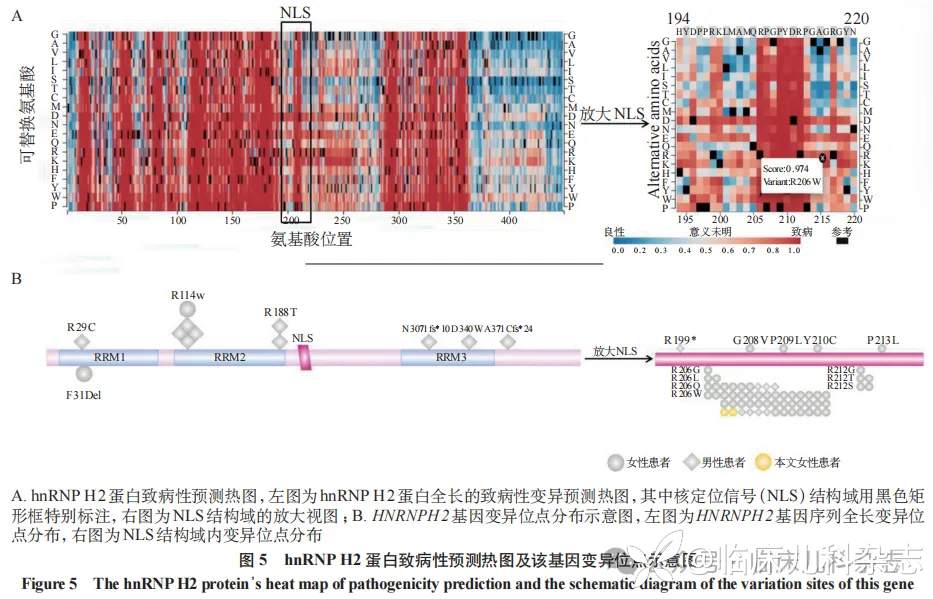
MRXSB 由 Bain 等 [1] 于 2016 年首次报道,是一种 X 连锁显性遗传的神经发育障碍性疾病,其致病机制与 HNRNPH2 基因功能异常相关。HNRNPH2 基因定位于 X 染色体 q22.1 区,含 3 个外显子,编码由 449 个氨基酸组成的蛋白,是异质性核糖核蛋白(hnRNPs)家族中的成员 [8]。hnRNP H2 蛋白作为 RNA 结合蛋白,能与前体信使 RNA 结合并形成核糖核蛋白颗粒,使其在细胞核与细胞质间穿梭,通过影响剪接位点调控前体信使 RNA 剪接,最终调控基因表达,该蛋白广泛表达于脑组织、胃肠道及心肺等器官。HNRNPH2 由 3 个 RNA 识别基序(RNA recognition motif,RRM)结构域构成,分别为 RRM1、RRM2 和 RRM3,RRM 结构域通过协同作用特异性识别 RNA 底物,并介导前体信使 RNA 结合形成核糖核蛋白复合体,参与 RNA 剪接调控 [9]。此外,该蛋白包含一个核定位信号(nuclear localization sequence,NLS,氨基酸 194~220),对维持其在细胞质与细胞核间穿梭至关重要 [10]。AlphaFold 蛋白预测工具显示,NLS 区域内(特别是氨基酸 206~213)的变异具有较强致病性,可能与核转运功能受损直接相关(图 5A)[11-12]。截至目前,该基因已报道变异位点 19 个,其中 12 个位于 NLS 区域,热点变异位点——c.616C>T(R206W) 也位于 NLS 内(图 5B)。c.616C>T 为热点变异的原因,一方面与其编码蛋白在不同物种间的高度保守性相关;另一方面,既往研究证实 NLS 区域内的变异通过影响 hnRNP H2 蛋白与核转运蛋白β2(karyopherin-β2,Kapβ2)的结合,导致细胞质-细胞核转运障碍,使 hnRNP H2 蛋白异常滞留于细胞质 RNA 颗粒中,干扰前体信使 RNA 剪接调控,从而引发智力障碍及小头畸形等神经发育障碍性症状 [13-14]。从基因序列上看,该变异位于 HNRNPH2 基因 2 号外显子的 CpG 二核苷酸序列中,推测其具有甲基化倾向,而甲基化胞嘧啶(5mC)易通过自发脱氨基作用转化为胸腺嘧啶(T),通过促进 DNA 脱氨或干扰修复效率增加该位点变异概率,X 染色体中 CpG 岛的密集分布及女性胚胎发育早期 XIST 基因介导的甲基化沉默可能加剧此类变异的积累 [15],此推测需通过重亚硫酸氢盐测序或单分子甲基化分析进一步验证。
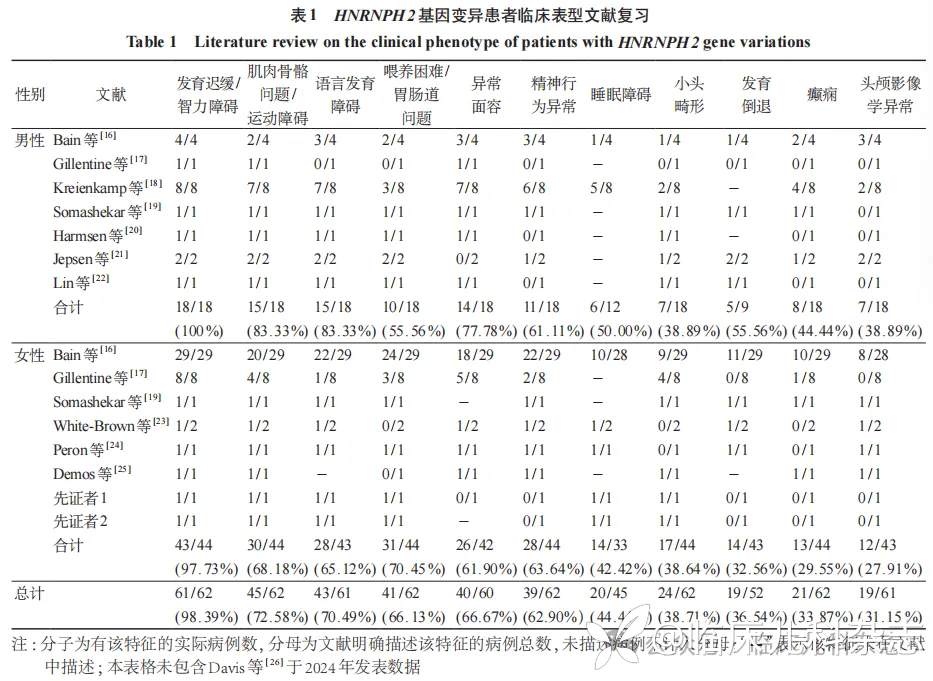
MRXSB 患者的临床特征主要为生长发育迟缓及智力障碍,语言发育障碍,运动缺陷以及肌肉骨骼问题(如脊柱侧凸、关节炎、髋关节脱位、踝关节畸形、肌张力降低及肌痛等,导致行走困难或运动时出现震颤及抽搐等情况,严重者需终身卧床),喂养困难及胃肠道症状(如胃食管反流、吞咽困难、腹泻及异食癖等)等,部分患者还具有行为及精神问题(如孤独症谱系障碍、注意缺陷与多动障碍、焦虑及抑郁症状等),癫痫(如强直阵挛、肌阵挛、凝视及痉挛等,且大部分为药物难治性癫痫),异常面容,小头畸形及睡眠障碍等,极少数发生早期卒中和过早死亡 [16-17]。截至 2025 年 7 月,全球共报道 75 例 MRXSB 患者(包括本文 2 例),患者发病年龄为 2~38 岁,其中男性 18 例、女性 57 例,推翻了早期男性胚胎致死的假设。男性患者表现出更严重的临床表型,其运动障碍、癫痫及语言障碍等的发生率显著高于女性,这一现象归因于男性仅携带单个 X 染色体,无法通过 X 染色体随机失活保留正常等位基因而补偿变异危害 [18];女性患者表型则因 XCI 调控呈现较大异质性,但相较于男性患者更易出现胃肠道问题,见表 1[16-26]。White-Brown[23] 报道 1 例携带 HNRNPH2 基因 c.616C>T 但无 MRXSB 相关临床表现的女性患者,其临床与极度偏倚的 XCI 模式相关(XCI 比例为 1%)。本研究的 2 例患儿均为 X 染色体偏倚失活,结合患儿发病年龄较早,症状较为典型,推测携带变异的染色体保留活性的比例较大,上述情况极为罕见,X 染色体偏倚率与 HNRNPH2 基因的关系需进一步通过扩大样本量及开展功能性试验证实。
目前针对 MRXSB 尚无有效的治疗方法,临床上主要以对症支持、营养支持及康复理疗为主,但常规康复手段有限。Korff 等 [27] 通过小鼠模型证实致病性 HNRNPH2 变异可重现人类表型,而完全敲除该基因的小鼠因 HNRNPH1 代偿性上调未出现异常,结果提示或可通过靶向诱导 HNRNPH1 补偿表达(如反义寡核苷酸疗法)以改善 MRXSB 患者症状 [28]。本研究先证者 1 经康复训练 6 个月后,患儿治疗效果不佳,其认知、生长发育及大运动功能均无明显改善,可见常规康复手段对 MRXSB 的治疗存在局限性,未来需探索基于致病机制的个体化治疗策略。
综上,本文报道的 2 例患儿分别于 11 及 10 月龄确诊为 MRXSB,为目前确诊年龄最小的患者,结合出生后均存在神经运动发育迟滞(肌张力异常、智力障碍及里程碑缺失),提示其临床表型较重。上述临床表现结合 XCI 分析提示,2 例患儿携带 HNRNPH2 基因 c. 616C>T 变异的 X 染色体优先保留活性的可能性较大,因此出现较早较重的临床表型。相较于先证者 1,先证者 2 的 Gesell 发育综合评分更低且所有能区均全面严重落后,其运动功能大部分丧失(无翻身、坐位、爬行)且康复完全无效,合并髋关节发育不良及混合型肌张力异常,提示先证者 2 症状更严重,该结论与两者 XCI 比例相符(先证者 2 的 XCI 比例小于先证者 1)。若想进一步证实上述推断,需结合变异位点附近单核苷酸多态性 (SNP) 位点进行单倍型分析,或进行 RNA 水平检测,从而明确携带变异的染色体是否大部分保留活性 [29-30]。通过对 XLID 患儿的临床表型及 XCI 结果的综合分析,本文揭示了 X 染色体偏倚失活对女性 XLID 患者表型的重要影响,表明 XCI 联合 WES 对于女性 XLID 患者临床表现严重程度预测、疾病早期干预与治疗具有临床指导意义,同时提示 XLID 遗传疾病的表型异质性可能受 XCI 模式或变异位点功能影响。
参考文献 略
好文章,需要你的鼓励















