让临床听懂科研,让科研看见临床
妊娠期糖尿病(gestational diabetes mellitus , GDM)是全球范围内最常见的妊娠并发症之一,其发病率呈持续上升趋势。大量流行病学研究表明,GDM 不仅影响母体妊娠结局,更显著增加子代成年后发生肥胖、胰岛素抵抗、2 型糖尿病及心血管代谢疾病的风险。
骨骼肌作为人体最大的葡萄糖和脂质代谢器官,在维持机体能量稳态、调控胰岛素敏感性和运动能力中发挥核心作用。然而,宫内高糖暴露是否影响子代骨骼肌结构和功能,其分子调控机制尚缺乏系统性阐明。

近日,浙江大学医学院附属第四医院生殖医学中心黄荷凤院士研究团队与复旦大学附属妇产科医院杨红波研究员团队合作,在国际肌肉领域顶尖期刊 Journal of Cachexia, Sarcopenia and Muscle (JCSM,中科院 1 区,IF 9.1)上发表题为「Multi-Omics Revealed the Effects of Intrauterine Hyperglycemia Exposure on the Development of Skeletal Muscle in Offspring」 (宫内高糖暴露对子代骨骼肌发育影响的多组学研究)的原创性研究成果。
本研究围绕「宫内高糖暴露对子代骨骼肌发育及代谢功能的长期影响」这一关键科学问题,构建妊娠期糖尿病小鼠模型,系统开展多时间维度、多组学层级的综合研究,首次从表型、转录调控及表观遗传重编程等多个层面,系统研究了宫内高糖暴露导致子代骨骼肌功能障碍的表观遗传学机制,揭示了先锋转录因子 AP-1 在介导宫内高糖暴露损害子代骨骼肌发育过程中的关键作用。
研究团队对 GDM 子代在出生后不同发育阶段进行长期随访,系统评估体重变化、体脂比例、葡萄糖耐量、胰岛素敏感性、肌肉力量及运动能力等指标。
结果显示,与健康小鼠子代相比,宫内高糖暴露子代在成年期表现出明显的肌肉比例下降、脂肪比例升高、肌力减弱和运动耐力降低等表型特征,同时伴随葡萄糖耐量受损和胰岛素抵抗,提示宫内高糖暴露可在发育早期「预设」一种不利于骨骼肌健康和代谢稳态的长期结构基础。在组织与超微结构层面,研究人员进一步发现,GDM 子代骨骼肌纤维横截面积显著缩小,线粒体结构紊乱,肌原纤维排列异常,并出现明显的肌内异位脂质沉积。这些结构性改变为骨骼肌功能下降提供了直接的形态学证据,提示宫内高糖暴露不仅影响代谢调控,还深度损害了骨骼肌发育过程中的组织结构基础。
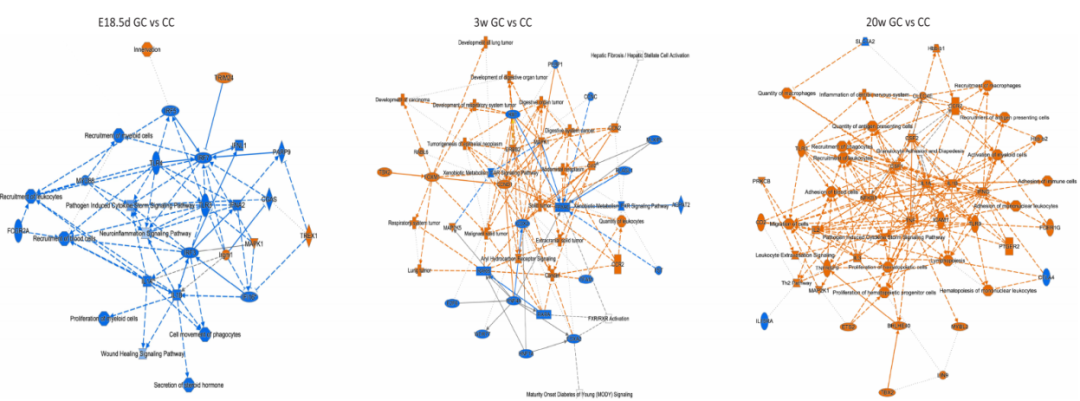
在分子机制层面,研究团队综合运用 RNA-seq 与 ATAC-seq 技术,对胎儿期、幼年期及成年期骨骼肌进行多时间轴动态分析。结果发现,宫内高糖暴露可引起骨骼肌转录组发生显著重编程,差异表达基因主要富集于免疫炎症反应、趋化通路及脂质代谢等关键生物学过程。同时,ATAC-seq 分析显示,宫内高糖暴露导致子代骨骼肌各个时期均呈现染色质开放程度的明显下降。
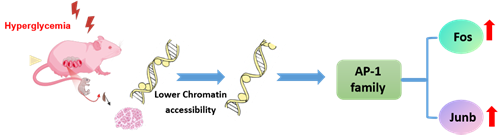
值得注意的是,转录因子结合位点富集分析进一步锁定 AP-1 家族为关键调控枢纽。研究发现,Fos、JunB 等 AP-1 家族成员在胎儿期、幼年期及成年期骨骼肌中持续高表达,并在染色质开放区域显著富集,构成调控网络的核心节点。蛋白水平实验证实,Fos 和 JunB 在 GDM 子代骨骼肌中显著上调,而出生后运动干预可明显下调其表达水平。该结果提示,AP-1 转录因子可能是连接宫内高糖暴露与骨骼肌发育异常之间的关键分子枢纽,在发育编程过程中发挥核心调控作用。
为进一步验证高糖对成肌细胞的直接作用,研究团队构建胎鼠原代成肌细胞高糖培养模型,并开展非靶向代谢组学分析。结果显示,高糖环境可显著诱导成肌细胞代谢谱重编程,脂肪酸合成与延长通路明显激活,细胞内脂滴大量积聚,同时 Fos 与 JunB 表达同步升高。该结果表明,高糖本身即可直接驱动成肌细胞发生代谢异常和脂质沉积,支持宫内高糖通过「代谢–转录–表观遗传」偶联机制影响骨骼肌发育命运。
该研究从发育源性疾病理论框架出发,首次系统构建了「宫内高糖暴露—表观遗传重编程—AP-1 介导转录调控—骨骼肌异常发育表型」的完整机制链条,深化了对妊娠期代谢异常影响子代长期健康风险的认识。研究成果不仅为妊娠期糖尿病子代代谢疾病的早期风险评估提供了理论基础,也为围绕生活方式干预开展精准预防策略提供了重要科学依据,在发育生物学、代谢医学及转化医学领域具有重要学术价值和潜在临床意义。
浙江大学医学院附属第四医院生殖医学中心主治医师/助理研究员刘睿博士、浙江大学医学院 2024 级博士生佘俊森为本文共同第一作者。浙江大学医学院附属第四医院生殖医学中心黄荷凤院士,复旦大学附属妇产科医院/生殖与发育研究院杨红波研究员为本文共同通讯作者。
好文章,需要你的鼓励
















