通讯员:罗羽茜
近日,南昌大学第二附属医院肿瘤中心刘安文教授、陈磊峰教授、罗羽茜博士等团队成员的研究成果在国际知名期刊《Advanced Science》(中国科学院 1 区 Top 期刊,影响因子 14.1)正式发表。该研究首次系统揭示了放疗联合免疫治疗所致心脏损伤的关键机制,并提出针对性防治策略,标志着医院在肿瘤心脏病学领域的研究水平再上新台阶。

随着肿瘤免疫微环境及免疫逃逸机制研究的不断深入,靶向 PD-1/PD-L1 和 CTLA-4 的免疫检查点抑制剂(ICI)疗法已彻底改变了胸部恶性肿瘤的治疗格局。然而,患者个体差异的存在以及部分肿瘤固有的原发耐药问题,在一定程度上限制了该疗法的获益。临床试验与真实世界研究均证实,免疫检查点抑制剂联合治疗策略,尤其是与放疗相结合的方案,显著延长了肺癌患者的总生存期,已成为胸部恶性肿瘤的常规治疗选择。
然而,免疫检查点抑制剂治疗引发的免疫毒性及放疗诱导的不良反应,可能对胸腔重要器官(特别是肺部和心脏)造成累积性损伤。这不仅限制了联合疗法的有效性,更损害了癌症患者的长期生存获益。因此,在当前胸部恶性肿瘤患者放免联合治疗广泛应用的时代背景下,针对该联合方案可能导致的严重心血管不良事件的识别、管理以及发病机制研究,具有重要的临床意义。
心脏纤维化是免疫治疗或放射治疗诱发心脏损伤的重要病理生理过程,其早期表现为保护性修复反应,但若持续进展且未受干预,将引发心室顺应性下降、心力衰竭及心律失常性猝死等终末期心脏事件。因此,探索放免联合治疗诱导心脏纤维化的具体机制,有助于开发有效的预防和治疗策略,从而改善癌症患者肿瘤治疗的疗效及生存质量。
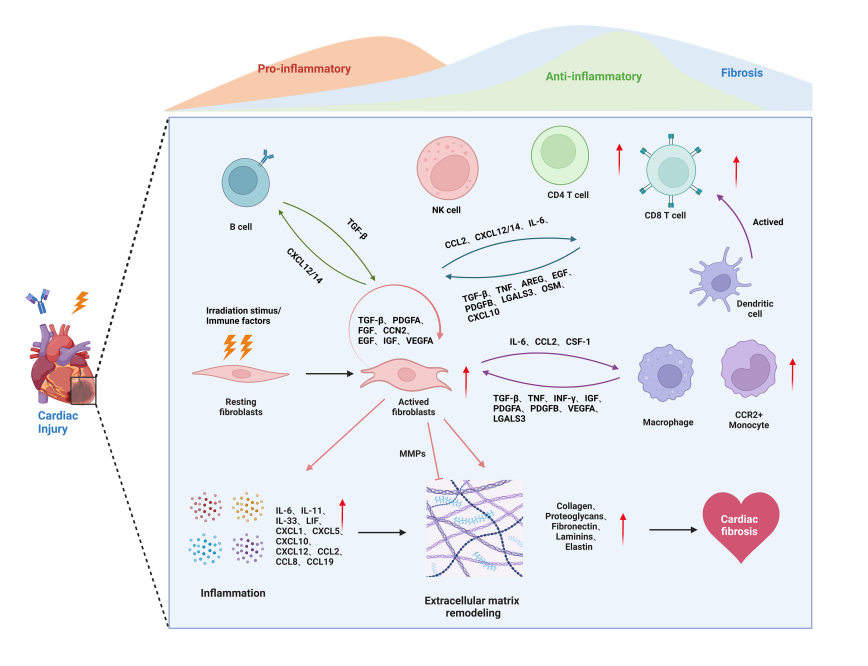
刘安文教授团队的最新研究发现,放免联合治疗可显著诱发心脏纤维化,且该病理进程随时间进行性加重。通过运用单细胞转录组测序技术,团队证实成纤维细胞是心脏纤维化的关键驱动细胞:在心脏辐射联合 ICI 干预后,成纤维细胞比例显著升高,其细胞外基质(ECM)及促纤维化分子表达明显上调,通过自分泌环路促进纤维化进展;同时,活化的成纤维细胞与巨噬细胞、T 淋巴细胞等免疫细胞互作,形成「免疫-基质」调控网络,共同加速心肌纤维化。
研究进一步明确,成纤维细胞分泌的 IL-6 是核心驱动分子。临床样本显示,接受放免联合治疗的胸部肿瘤患者血清 IL-6 水平显著升高;通过 IL-6 基因敲除小鼠模型及药物干预实验证实,IL-6 受体抑制剂托珠单抗可有效阻断该互作通路,显著减轻放免联合治疗诱发的心脏损伤及纤维化,且在荷瘤小鼠模型中可协同增强抗肿瘤疗效。该研究借助单细胞转录组测序技术,首次揭示了 IL-6 介导的成纤维细胞-巨噬细胞互作是放免联合治疗致心脏毒性的核心机制,为临床优化肿瘤联合治疗方案、降低心脏不良反应提供了干预靶点和治疗策略。
据了解,刘安文教授团队自 2013 年赴 MD 安德森癌症中心访学以来,长期深耕肿瘤治疗相关心脏病学领域的临床与基础研究。团队围绕肿瘤治疗相关心脏损伤的发病机制与防治策略展开系统攻关,先后主持国家自然科学基金面上项目、省级重点研发计划等课题 8 项;以第一作者或通讯作者身份在国内外期刊发表学术论文 100 余篇,其中在肿瘤治疗相关心脏损伤机制领域,《International Journal of Radiation Oncology Biology Physics》《Biochimica et Biophysica Acta Reviews on Cancer》《Cancer Immunology, Immunotherapy》及《International Immunopharmacology》等权威期刊发表 SCI 论文 10 余篇。
好文章,需要你的鼓励
















