ASH2022 | 潘静主任团队:供者来源 CD7 CAR-T 治疗 r/r T-ALL/LBL 的Ⅱ期研究新进展
CD7 作为 T 细胞表面非常稳定的标志物之一,已成为当前 T 系肿瘤领域 CAR-T 疗法探索的热门靶点。在即将来临的第 64 届美国血液学会(ASH)年会上,高博医学(血液病)北京研究中心北京高博博仁医院潘静主任团队开展的一项「供者来源 CD7 CAR-T 治疗难治/复发急性 T 淋巴细胞白血病/淋巴瘤(r/r T-ALL/LBL)的疗效和安全性:来自Ⅱ期临床试验的中期分析」将以壁报形式精彩亮相。
此前,该研究的Ⅰ期学术成果已连续 2 年荣登美国临床肿瘤学会(ASCO)年会,并获选 2021 ASCO 年度会议 Highlight 摘要,受到了业内的高度认可与广泛关注。为此,我们特别整理研究精要,以飨读者。
摘要号 2011:供者来源 CD7 CAR-T 治疗难治/复发急性 T 淋巴细胞白血病/淋巴瘤(r/r T-ALL/LBL)的疗效和安全性:来自Ⅱ期临床试验的中期分析

研究背景
此前,供者来源 CD7 CAR-T 治疗复发或难治急性 T 淋巴细胞白血病(r/r T-ALL)的Ⅰ期临床研究(Pan et al. J Clin Oncol 2021;39:3340-3351)结果已公布。在此基础上,汇报该研究Ⅱ期临床试验的中期研究结果。
研究方法
Ⅱ期临床试验和Ⅰ期临床试验有相似的纳入/排除筛选标准。既往接受过造血干细胞移植(SCT)的患者接受来自既往 SCT 供者的 CAR-T 细胞;而未接受过 SCT 的患者则接受新供者来源的 CAR-T 细胞,并由该供者担任其 CAR-T 治疗后 SCT 的供者。
Ⅱ期临床试验采用贝叶斯最优Ⅱ期设计(BOP2),以评估目标剂量为 1×106 (±20%)/kg 的 CD7 CAR-T 细胞治疗 r/r T-ALL/LBL 的有效性和安全性(NCT04689659)。
研究的主要终点为疗效性,次要研究终点为安全性。期中分析将在Ⅱ期临床试验入组的前 20 人完成 3 个月的随访后进行。患者的生存状况将被持续记录,而与 CAR T 相关的严重不良事件(SAEs)则追踪到患者接受其他抗白血病治疗。
研究结果
1. 入组情况
进行Ⅱ期临床试验期中分析的 20 例患者,与Ⅰ期临床试验的 20 例患者的基线特征相似(图 2),但Ⅱ期临床试验纳入了更多的纵隔肿瘤患者。
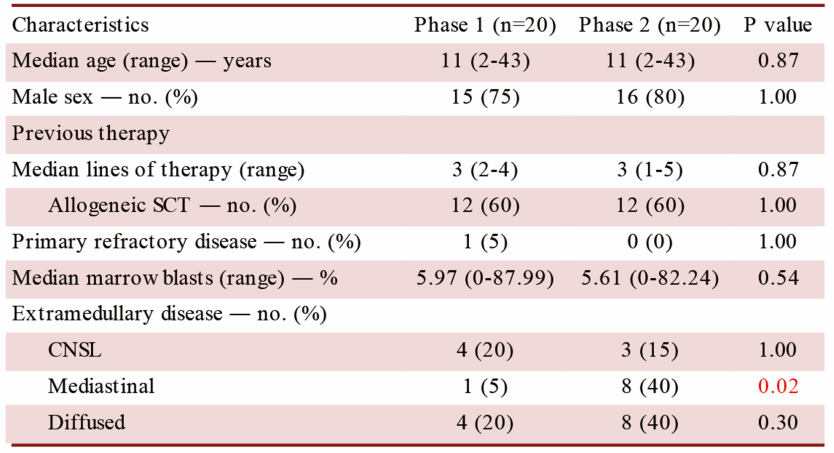
截至 2022 年 5 月 14 日,共 18 例(90%)患者接受 CD7 CAR-T 治疗后有效,中位随访时间 11.0(7.6~14.6)个月。
2. 疗效报告
接受 CD7 CAR-T 细胞输注后 3 个月时,最佳总体反应率(BOR)为 90%;输注后 1 个月和 3 个月时的客观缓解率(ORR)均为 90%,这与Ⅰ期临床试验的疗效相似(患者输注后 1 个月和 3 个月的 ORR 均为 95%)。
其中,输注后 3 个月时纵隔肿瘤患者的完全缓解(CR)率低于无纵隔肿瘤的患者,尽管在统计学上没有显著差异(p = 0.07,图 3)。
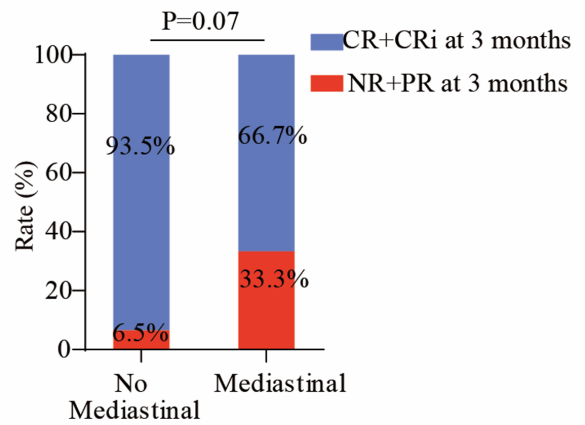
截至最后一次随访,在 12 例(67%)未接受进一步治疗的患者中,患者体内均持续检测到 CAR-T 细胞。其中 3 例仍维持缓解状态,7 例复发(3 例 CD7+,3 例 CD7-,1 例未知),2 例死于感染。
6 例(33%)患者接受了 SCT,移植后未检测到 CAR-T 细胞。其中,3 例患者仍维持缓解状态,2 例患者复发(均为 CD7-),1 例死于感染。
患者疾病复发的中位时间为 4(1.6~10.5)个月;1 年无进展生存(PFS)率为 62.3%,1 年总生存(OS)率为 60.0%。其中,无纵隔肿瘤的患者的 OS 获益显著优于纵隔肿瘤患者(p<0.05,图 4)。
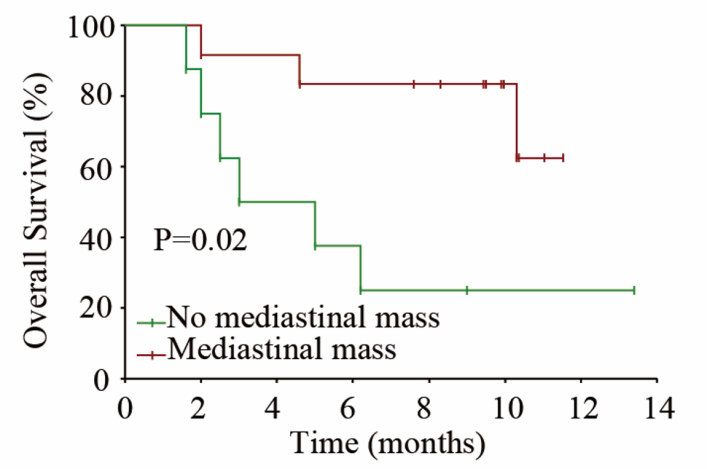
此外,随着随访时间的延长(中位随访时间 1.5 年),Ⅰ期临床试验的更新数据显示患者的 PFS 率为 60.0%,OS 率为 70.0%。
3. 安全性报告
观察到的短期不良事件包括 3 级或更高级别的细胞因子释放综合征(CRS,10%),以及 1~2 级移植物抗宿主病(GVHD,40%),均是可控的。
在 3 例患者中观察到共计 3 起迟发(>回输后 30 天)SAE:1 例患者在回输后 2 个月时发生 5 级败血症;1 例患者在回输后 2 个月时发生 5 级暴发性肝炎;1 例患者在回输后 5 个月时发生 5 级肺炎。
发生了严重感染的 3 例患者中,有 2 例未接受进一步治疗。这些感染患者体内的总 T 细胞中位计数达到 654.34 /μL(范围 :41.87 ~1210.46 /μL),尽管稳步增加,但仍显著低于正常水平。治疗的总体安全性特征与Ⅰ期临床试验相似(图 5)。
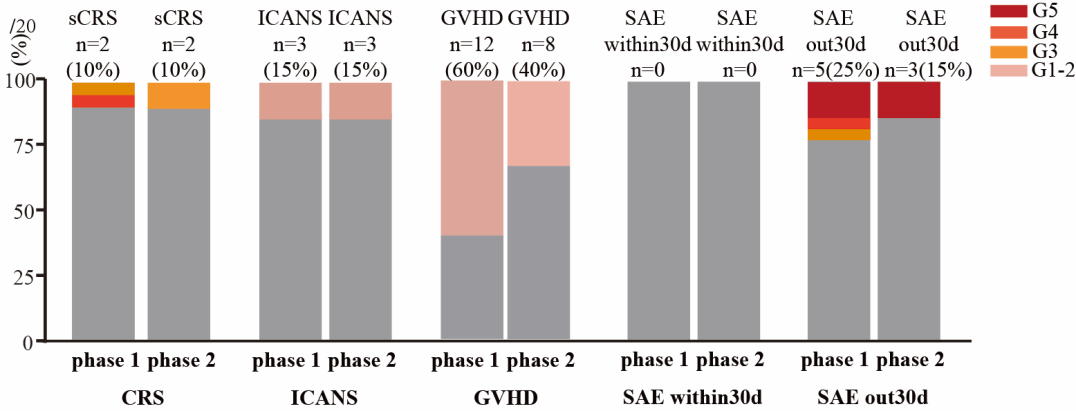
研究结论
供者来源 CD7 CAR-T 的Ⅱ期临床试验期中分析结果显示出与Ⅰ期临床试验相似的、令人鼓舞的治疗潜力。复发是影响长期疗效的主要因素,其中 CD7 阴性复发在 CAR-T 细胞的监视下经常发生。迟发性 GVHD 和感染在长期随访中可能发生,应谨慎处理。此外,纵隔肿瘤患者的总体生存获益较差,有待后续进一步研究。
好文章,需要你的鼓励