2020 年 12 月 5-8 日,第 62 届美国血液学会年会(ASH 2020)如期在线上举行。作为全球血液学领域最大最权威的国际学术盛会之一,会议期间将有超过数千多份摘要呈现。中国在嵌合抗原受体
2020 年 12 月 5-8 日,第 62 届美国血液学会年会(ASH 2020)如期在线上举行。作为全球血液学领域最大最权威的国际学术盛会之一,会议期间将有超过数千多份摘要呈现。
中国在嵌合抗原受体 T 细胞(CAR-T)领域的研究处于世界前列,来自高博医疗集团南方春富(儿童)血液病研究院李春富教授团队的卜朝可医生在本次会议上报告了 CLL1 CAR-T 治疗儿童复发难治急性髓系白血病相关研究数据。
CAR-T 疗法在治疗多种血液肿瘤方面取得了显著成功,如治疗 B 细胞恶性肿瘤的 CD19 CAR-T 以及治疗多发性骨髓瘤(MM)的 BCMA CAR-T 均表现亮眼。然而,CAR-T 治疗复发难治急性髓系白血病(R/R AML)的疗效却并不理想,无论是靶向 CD33、CD123、LeY、NKG2D 还是 CD70 受体,总体反应率均低于 CD19 CAR-T。由于 AML 的异质性,很难找到理想的 CAR-T 靶点。
李春富教授团队选择 CLL1 作为治疗靶点,并报告了 CLL1 CAR-T 治疗儿童 R/R AML 患者的疗效与安全性的 I 期临床试验数据。
CLL1 在正常造血干细胞(HSC)中不表达,但在 AML 细胞和白血病干细胞(LSCs)上高表达,因此选择 CLL1 作为靶点。2019 年 10 月至 2020 年 3 月,研究纳入 3 例儿童 R/R AML 患者,回输二代 CLL1 CAR-T 细胞。
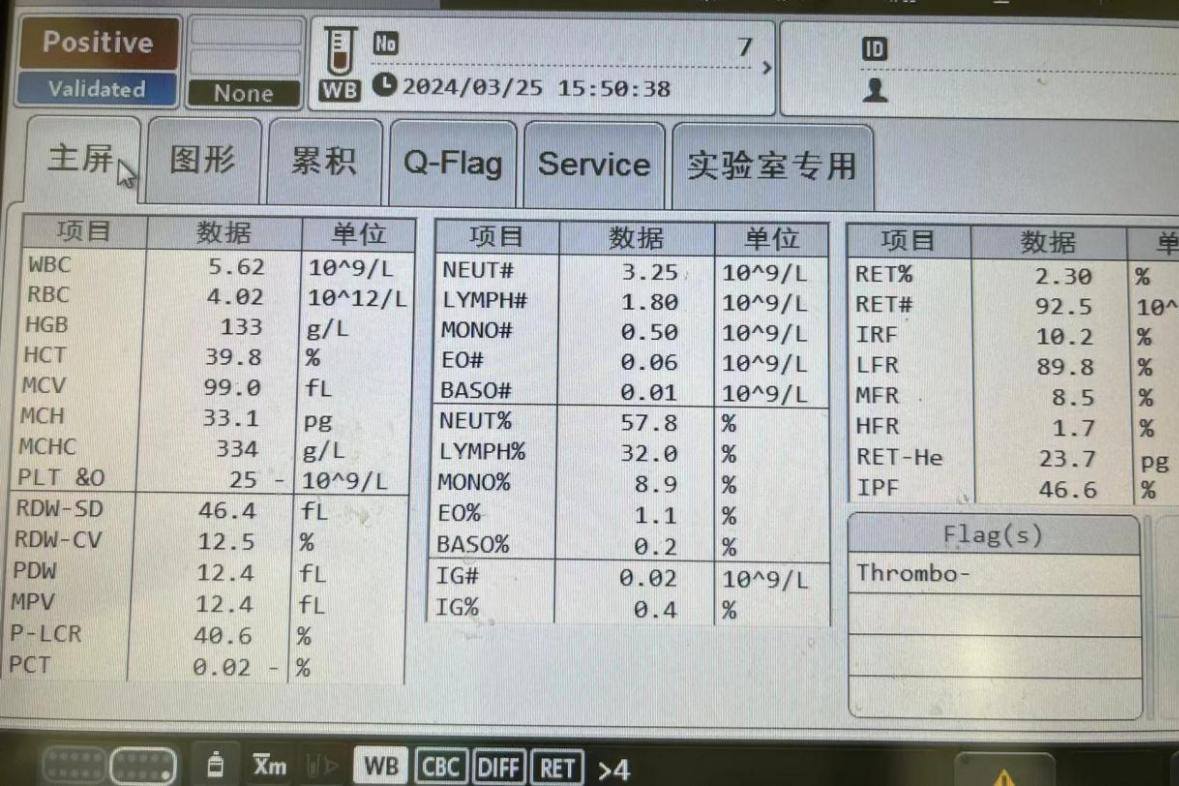
研究结果显示,3 例患者出现细胞因子释放综合征(CRS,Ⅰ级 2 例,Ⅱ级 1 例),无神经毒性反应。所有患者均出现全血细胞减少、粒细胞减少和单核细胞减少。治疗后所有不良反应均得到缓解。
患者 1 是难治 AML 患者,95% 以上 AML 母细胞呈 CLL1 阳性。CLL1 CAR-T 细胞回输第 21 天,患者达到完全缓解/微小残留病(MRD)阴性(CR/MRD-)。该患者在第 35 天行造血干细胞移植(HSCT),并一直保持 CR/MRD-状态(到 2020 年 7 月,CAR-T 输注后 8 个月)。
患者 2 是 HSCT 后复发患者,并有严重的骨髓坏死(BMN),因此减少 CAR-T 输注剂量。CAR-T 细胞回输后第 14 天患者达到了 CR/MRD-。患者在第 38 天行二次 HSCT,二次移植后 2 个月因 GVHD 死亡。
患者 3 是难治 AML 患者,约 85%AML 母细胞呈 CLL1 阳性。输注后第 14 天患者达到 CR/MRD+(1%)。但是第 30 天评估时 AML 母细胞增至 11%,其中大多数为 CLL1 阴性。
该患者第 30-34 天接受阿扎胞苷治疗,第 45 天时 AML 细胞降至 2.8%。值得注意的是,该患者之前阿扎胞苷治疗无效,这表明 CLL1 CAR-T 可以清除 LSC,从而使 AML 肿瘤细胞对化疗敏感。该患者第 75 天行 HSCT,至今保持 CR/MRD-(2020 年 7 月,CAR-T 输注后 7 个月)。
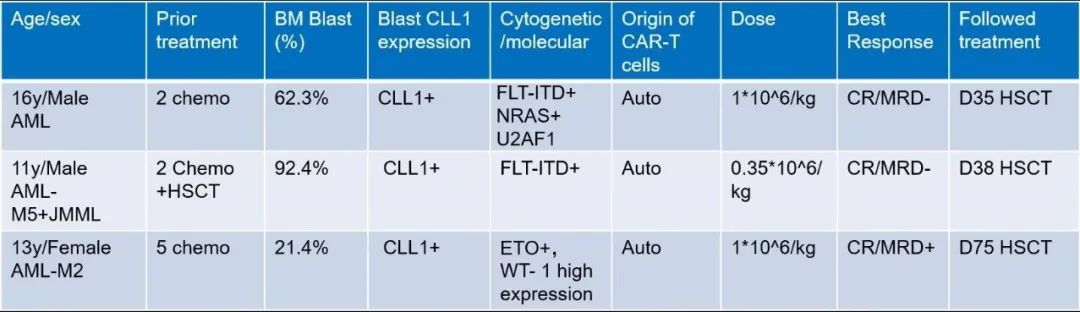
本研究初步结果表明,CLL1 CAR-T 治疗 R/R AML 患者有效且毒性可控。该研究中所有患者均在 1 个月内达到 CR,且 CRS 反应轻微(Ⅰ-Ⅱ级)。对于 AML 母细胞 CLL1 阴性的患者,CLL1 CAR-T 治疗后 CLL1-细胞可能会起致病作用,联合阿扎胞苷可能帮助患者达到完全缓解。
参考来源:Chaoke Bu, Zhiyong Peng, Min Luo, et al. Phase I Clinical Trial of Autologous CLL1 CAR-T Therapy for Pediatric Patients with Relapsed and Refractory Acute Myeloid Leukemia. 2020 ASH Annual Meeting, Abstract #2859.
*声明:本内容仅代表文章来源方观点,不代表本站立场。本内容仅供医学药学专业人士阅读,不构成实际治疗建议。
封面图来源:站酷海洛
好文章,需要你的鼓励