近日,两位阿尔茨海默病早期患者在河科大二附院神经内科三病区并肩完成了仑卡奈单抗输注治疗。这不是巧合,而是越来越多患者家庭的选择——当疾病修饰治疗成为现实,希望不再孤单。
从"无药可医"到"并肩作战"
阿尔茨海默病曾被视为"衰老的宿命",患者只能眼睁睁看着记忆流逝。仑卡奈单抗改变了这一现状:作为全球首个对因治疗药物,它能直接清除致病蛋白,延缓疾病进展 27% 。而近日同时选择治疗的两位患者,正是看中了这一"黄金窗口期"——在早期阶段干预,为大脑争取更多宝贵时间。
两位患者,同一种选择
她们互不相识,却做出了相同的决定:都处在阿尔茨海默病早期,符合最佳治疗时机;都经过严格评估,确认脑内淀粉样蛋白沉积;都选择每两周一次门诊输注,不影响日常生活。
治疗室内,两位老人平静地接受治疗,家属在旁陪伴。这温馨的一幕,正是现代医学赋予的底气——对抗阿尔茨海默病,不再需要孤军奋战。
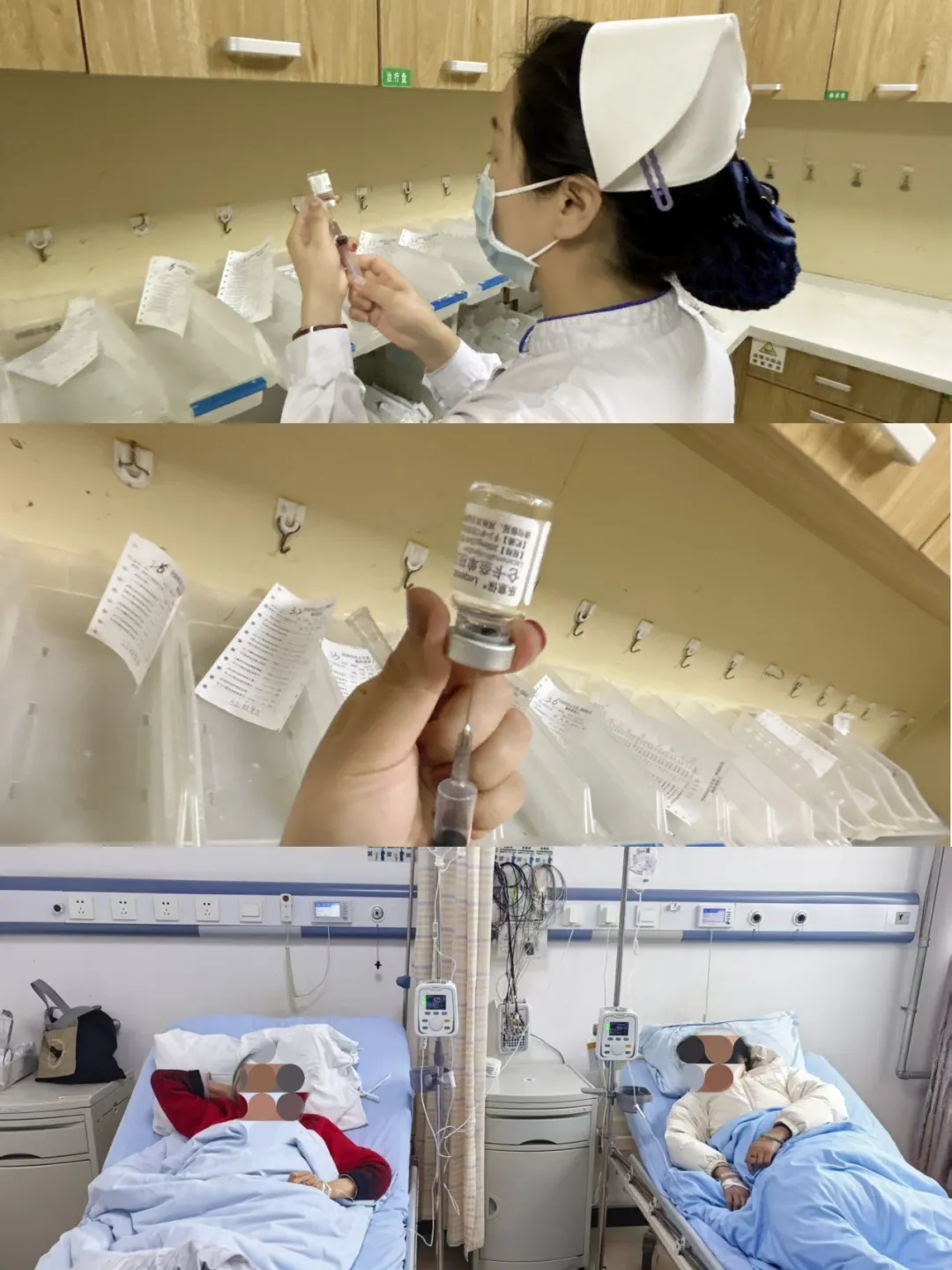
病例纪实:从记忆滑坡到认知稳定
60 岁的王先生(化名)因近半年来频繁出现记不住近期事务、重复提问、购物遗漏等情况前来就诊。家属反映其性格较前淡漠,日常理财和家务能力有所下降。经神经内科系统评估,包括 MMSE、ADAS-Cog 及 CDR 量表测试,结果显示其认知功能明显低于同龄人群水平。脑脊液生物标志物检测显示 Aβ1-42 水平显著降低,同时 Aβ42/40 比值下降,结合 Aβ PET/CT 影像呈现典型大脑皮层淀粉样蛋白沉积,临床确诊为早期阿尔茨海默病。
在充分知情并排除禁忌症后,王先生开始接受伦卡奈单抗(Lecanemab)静脉输注治疗,每两周一次,持续 20 个月。治疗期间定期进行 MRI 监测以评估淀粉样蛋白相关影像学异常(ARIA)风险,未见有症状性脑水肿或微出血。令人鼓舞的是,随访期间其 CDR-SB 评分保持稳定,未出现进一步恶化,日常生活能力得以维持。
阿尔茨海默病的
病理机制与靶向干预策略
阿尔茨海默病是一种以进行性认知衰退为特征的神经退行性疾病,其核心病理机制围绕β-淀粉样蛋白(Aβ)的异常聚集展开。正常情况下,Aβ肽由淀粉样前体蛋白(APP)经酶切产生,并被有效清除。但在疾病状态下,Aβ1-42 因其疏水性强、易聚集,逐渐形成可溶性寡聚体和不溶性斑块,沉积于大脑皮层,引发突触功能障碍、神经炎症及 tau 蛋白过度磷酸化,最终导致神经元丢失。
其中,脑脊液中 Aβ1-42 浓度降低是中枢 Aβ沉积的重要间接证据——因其被「困」于斑块中而无法释放入液相。同时,Aβ42/40 比值因 Aβ42 选择性沉积而下降,成为更敏感的早期诊断指标。这些生物标志物的变化往往早于临床症状数年,构成「生物标志物阳性」的诊断基础。
在此背景下,靶向清除 Aβ成为延缓疾病进展的关键策略。伦卡奈单抗作为一种人源化 IgG1 单克隆抗体,特异性识别并结合 Aβ原纤维(fibril),促进其通过小胶质细胞介导的吞噬作用被清除,从而减少脑内淀粉样斑块负荷。多项Ⅲ期临床试验已证实,伦卡奈单抗可显著降低 PET 检测中的淀粉样蛋白标准摄取值比(SUVR),并在统计学上延缓 CDR-SB 评分的年化下降速率约 27%,展现出明确的疾病修饰效应。
治疗响应的多维验证:
生物标志物与临床结局的协同改善
在王先生的治疗过程中,动态监测提供了有力的支持证据。治疗前脑脊液检测显示 Aβ1-42 为 5.647 pg/mL,处于典型低值范围;Aβ42/40 比值为 0.0564,提示显著的 Aβ代谢紊乱。经过 20 个月规范治疗后,Aβ1-42 回升至 7.18 pg/mL,Aβ42/40 比值改善至 0.0582,反映出中枢 Aβ清除效率提升,病理进程可能已被部分逆转。PET-CT 也提示 Aβ沉积较前减轻。

与此同时,CDR-SB(临床痴呆评定量表总和商)作为衡量认知与功能损害的核心临床终点,在治疗期间保持稳定,未见恶化趋势。这一「生物标志物改善+临床稳定」的双重响应模式,正是当前抗 Aβ疗法所追求的理想治疗目标——不仅改变病理轨迹,更转化为患者可感知的功能获益。
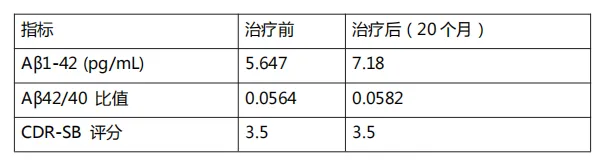
注:数据来源于患者匿名化临床记录,单位与检测方法符合国际标准
该案例虽为个体经验,但其所体现的治疗逻辑与大型研究结论高度一致,提示对于早期诊断患者,及时启动靶向治疗有望实现疾病进程的「踩刹车」。
目前越来越多的阿尔茨海默病患者开始伦卡奈单抗治疗。随着生物标志物技术的发展和疾病修饰药物的落地,阿尔茨海默病正从「不可逆衰亡」转向「可干预慢病」。伦卡奈单抗为代表的免疫疗法标志着我们首次具备了直接清除致病蛋白的能力。尽管仍需关注 ARIA 等安全性问题,但通过规范筛查与监测,风险可控。
好文章,需要你的鼓励
















