
近日,淮安市第一人民医院 病理科与南京大学王宏伟/黄志强教授团队合作的一项关于恶液质引起的骨骼肌萎缩的重要代谢网络的研究成果在国际知名期刊《Cell Metabolism》(IF 27.7,中科院 1 区)发表。
该研究发现了恶液质引起的骨骼肌萎缩的重要代谢网络, 揭示了 DNMT3A/REDD1 的表观调控机制, 提出蛋氨酸和 SAM 补充是改善恶液质骨骼肌萎缩的潜在营养途径。我院病理科魏璐璐博士为文章共同第一作者,南京大学医学院王宏伟教授、黄志强助理教授和苏北人民医院王永祥教授为本文的共同通讯作者。
肿瘤恶液质,又称恶病质,是肿瘤患者常见且严重的并发症,表现为体重下降、食欲减退、骨骼肌萎缩和脂肪降解,其显著影响患者生存质量并增加死亡风险。肿瘤恶液质目前缺乏有效的治疗手段,传统营养支持仅能部分缓解症状,因此深入研究其发病机制尤为重要。
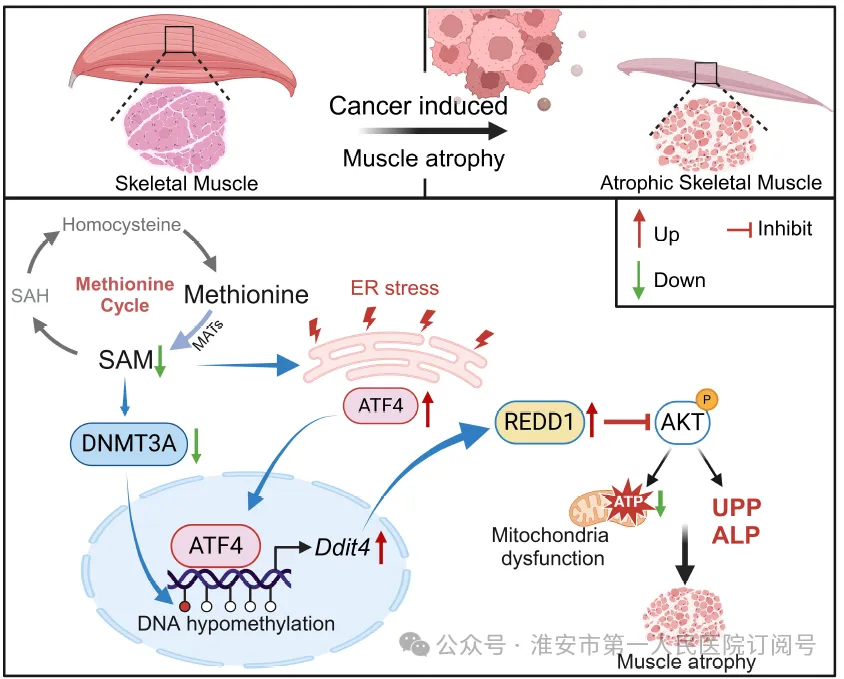
该研究从临床晚期肿瘤患者恶液质的骨骼肌表型分析入手,利用多组学研究方法,分析了在恶液质骨骼肌萎缩过程中,蛋氨酸代谢异常的病理学表型特征,发现存在严重的蛋氨酸循环障碍。SAM 的缺失导致 DNMT3A 表达下调,降低肌管细胞中 DNA 的甲基化修饰水平;另一方面,通过诱导内质网应激(ERS),激活转录因子 ATF4,从而增加细胞中 AKT 通路抑制因子 REDD1 的表达水平。通过转基因和基因敲除小鼠工具,作者阐明 REDD1 的缺失显著改善肿瘤引起的体重损失和骨骼肌降解,并识别出蛋氨酸-DNMT3A-ATF4-REDD1 的表观遗传调控机制。
作者介绍

魏璐璐,淮安市第一人民医院病理科住院医师,南京大学博士研究生,江苏省双创博士,南京大学/南京医科大学附属淮安第一医院联合培养博士后,长期从事肿瘤恶液质引起的骨骼肌萎缩的分子机制研究,以第一作者身份发表 SCI 论文 6 篇,累计影响因子 59.8 分,主持淮安市科技局自然研究项目 1 项,南京医科大学附属淮安第一医院高层次人才项目 1 项。
好文章,需要你的鼓励
















