近日,西安交通大学第一附属医院郑焱、王雅和康复大学刘健康团队联合在国际权威期刊《Advanced Science》发表重要成果,围绕传统中药白鲜皮展开深入研究,开发出可改善银屑病的新型纳米制剂,并揭示其背后关键分子机制,为慢性皮肤病治疗提供新思路和新方向。

01
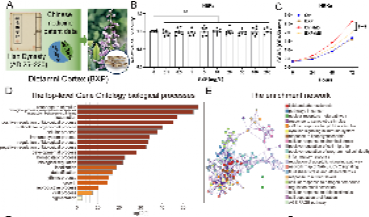
研究背景:银屑病治疗的临床困境与中药白鲜皮的潜力
银屑病是一种免疫介导的慢性皮肤病,全球患病率 2%-3%,复发率高,重症可伴发皮肤畸形、功能障碍及多器官共病,严重影响患者身心健康。目前临床治疗手段存在成本高、副作用大、长期疗效衰减,复发率高等问题,而外用药物受皮肤屏障限制,透皮吸收效率极低。白鲜皮作为传统中药,在治疗皮肤病方面拥有悠久历史,其在银屑病治疗相关中药复方专利中使用率高达 38.36%。但白鲜皮水溶性差、生物利用度低,且长期口服可能引发肝肾毒性,极大限制了其临床应用。我院郑焱教授团队长期从事中医中药治疗银屑病发病机制的研究。
02
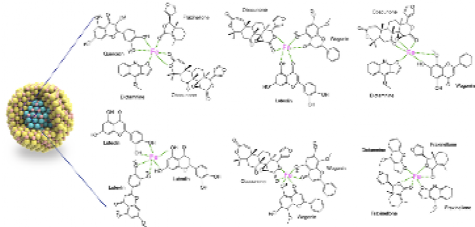
核心成果:新型制剂突破中药瓶颈,显著改善银屑病症状
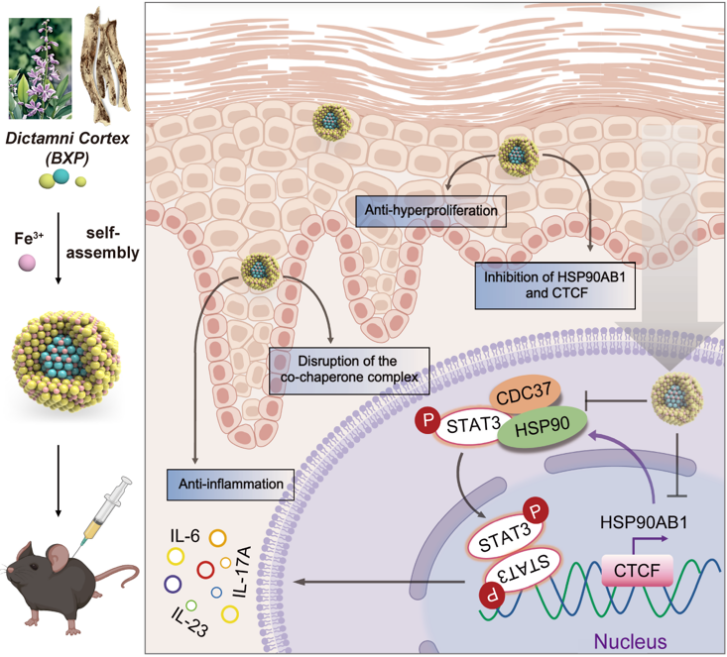
为解决白鲜皮的应用局限,我院郑焱、王雅联合刘建康团队开发了基于白鲜皮的新型制剂(BXP-Fe (III) ICPs,简称 NB)。该制剂无需额外载体,能针对性改善白鲜皮的药理缺陷:一方面提升了其在体内的利用效率,另一方面可在银屑病炎症部位的酸性微环境中精准释放有效成分,避免健康组织受损;同时,制剂中的成分还能补充银屑病患者表皮中显著减少的铁元素,协同辅助治疗。
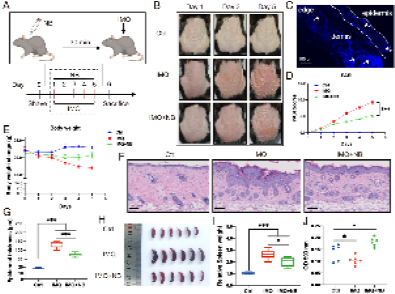
实验验证显示,无论是在细胞模型(M5 细胞因子诱导的人表皮角质形成细胞)还是动物模型(咪喹莫特 IMQ 诱导的银屑病小鼠)中,这种新型制剂都能有效抑制角质形成细胞过度增殖,减轻炎症反应和氧化应激,显著改善皮损外观与病理特征。

03
机制揭秘:CTCF-HSP90AB1-STAT3 轴的精准调控
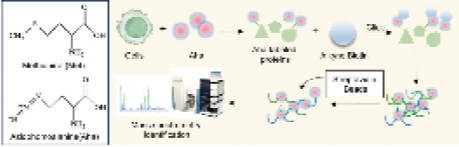
为明确制剂的作用原理,研究团队通过新生蛋白质组学分析,锁定了热休克蛋白 90 α 家族 B 类成员 1(HSP90AB1)这一核心靶点——该蛋白在银屑病患者皮损中表达显著升高,是推动疾病发展的关键分子。
进一步研究发现,新型制剂通过两大途径发挥作用:
1. 抑制分子伴侣复合物形成:HSP90AB1 需与辅助分子 CDC37 结合形成复合物,才能激活下游 STAT3、Akt 等关键信号蛋白(这些蛋白会促进角质形成细胞增殖和炎症)。NB 制剂能破坏二者结合,从而阻断疾病进展。
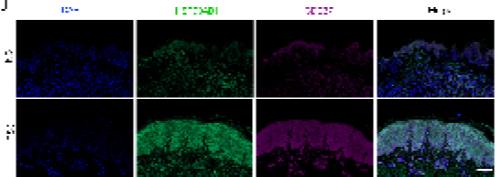
2. 抑制 HSP90AB1 转录:前期实验结果发现 NB 下调了 HSP90AB1 的蛋白水平,通过 CUT&Tag 技术表明 NB 可下调其转录因子 CTCF 的表达,进而直接减少 HSP90AB1 的生成;
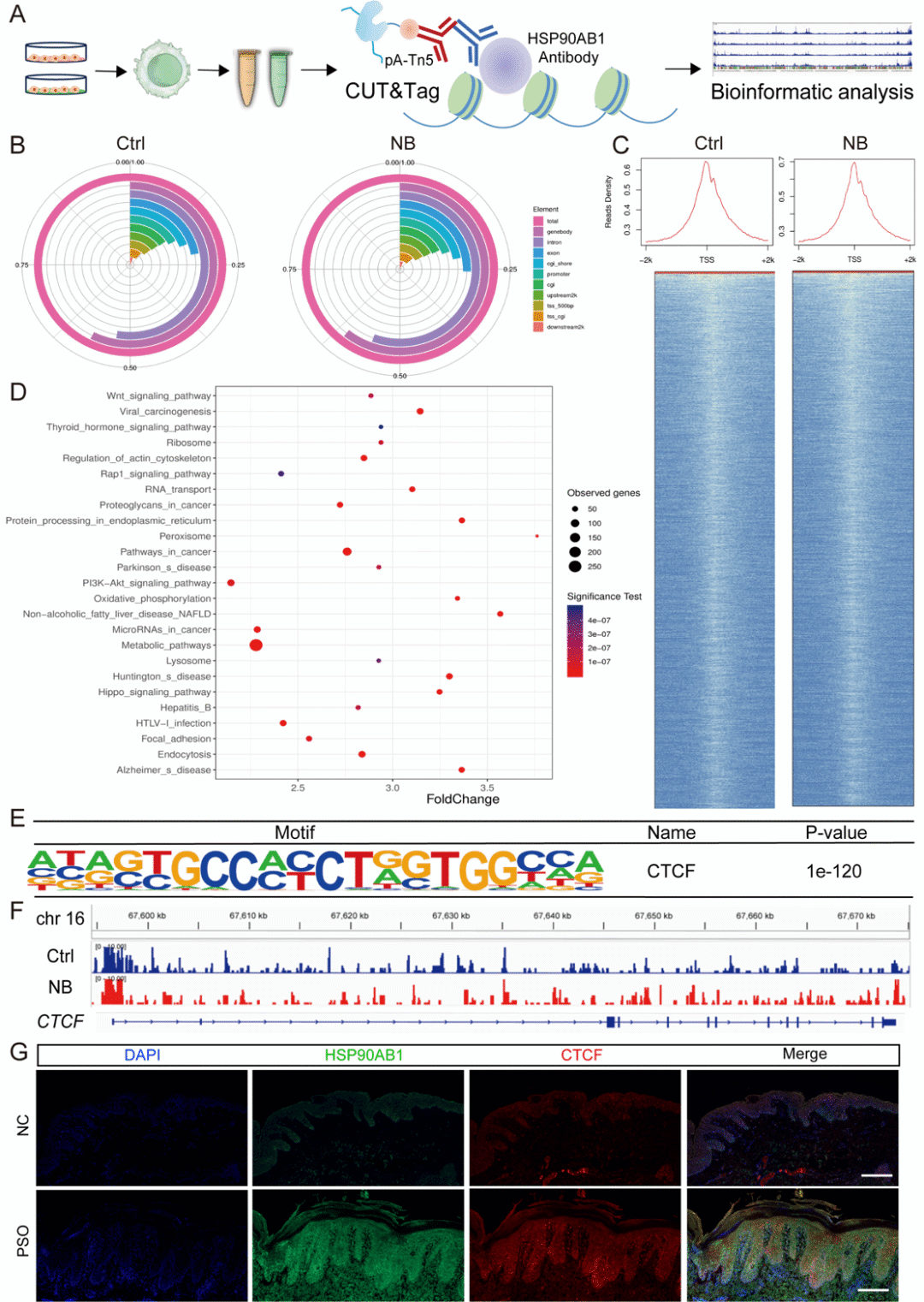
值得注意的是,与临床研究中常用的 HSP90 抑制剂 AUY922 相比,该制剂的治疗效果更优,还能避免传统抑制剂可能引发的「热休克反应(HSR)」(一种代偿性耐药机制)。单细胞数据分析进一步证实,CTCF 和 HSP90AB1 在银屑病患者的角质形成细胞、CD4⁺T 细胞中异常高表达,二者构成的调控轴是银屑病发病的核心环节。
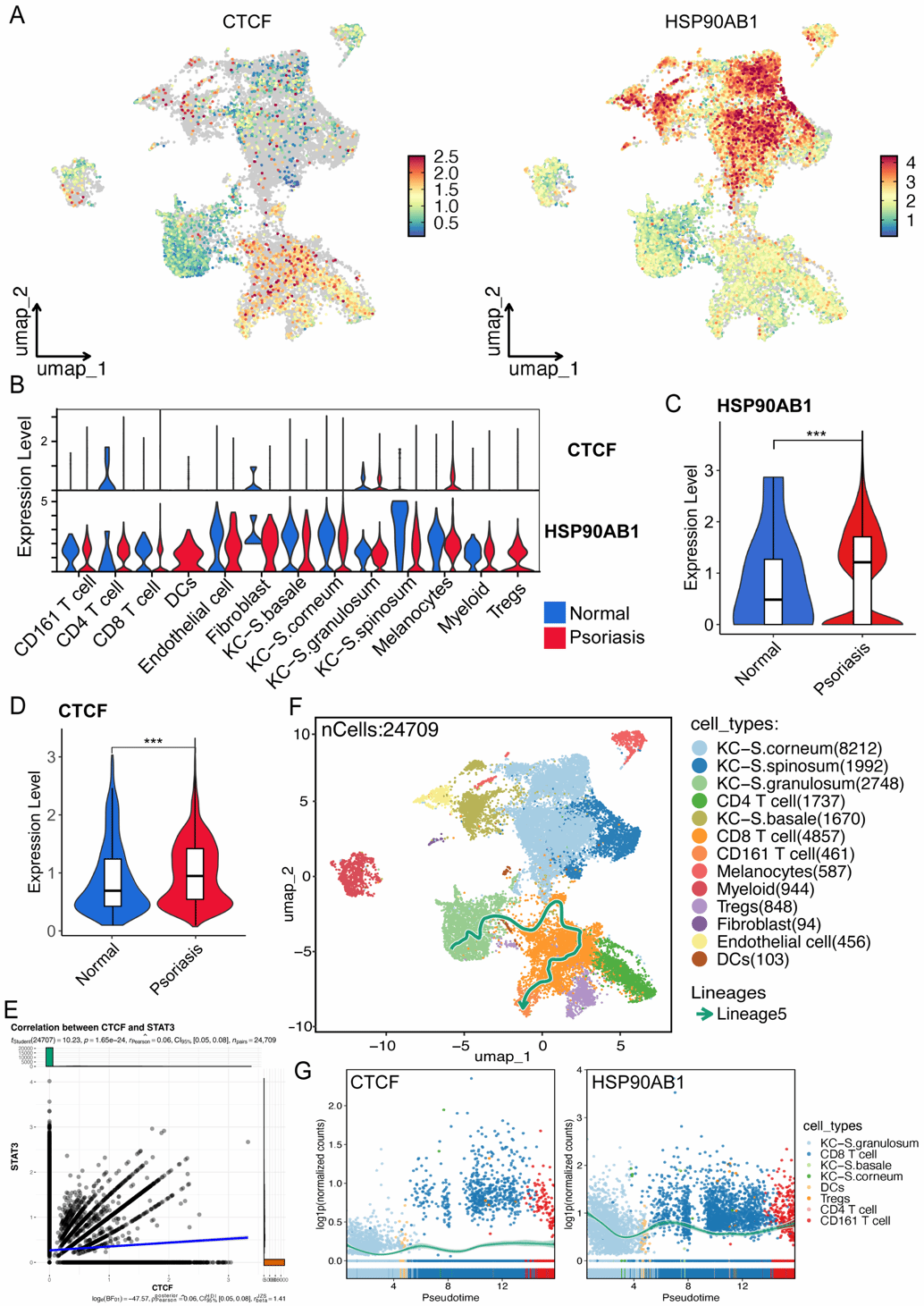
这项研究不仅为银屑病治疗提供了更具针对性的新方案 —— 既保留中药白鲜皮的整体疗效,又通过制剂优化解决了其应用瓶颈;更重要的是,首次揭示了 CTCF-HSP90AB1-STAT3 轴在银屑病发病中的关键作用,为后续开发靶向药物提供了明确方向。未来,团队将进一步推进该制剂的临床转化研究,探索其在更多皮肤病中的应用可能,助力传统中药的现代化发展,为患者带来更安全、有效的治疗选择。
本次研究的重要突破,离不开医工交叉理念的深度融合与多学科团队的协同攻关。研究以临床需求为导向,将传统中医药理论与现代工程技术、生命科学深度结合:皮肤科团队凭借对银屑病发病机制与临床痛点的深刻认知,明确了白鲜皮的优化方向与疗效验证标准;材料科学团队运用配位自组装技术,解决了中药成分水溶性差、递送效率低的核心技术瓶颈;生物医学团队则通过蛋白质组学、单细胞分析等技术,精准解析了制剂的分子作用机制。这种「临床需求 - 技术突破 - 机制验证」的跨学科协作模式,不仅实现了传统中药的现代化改造,更推动了皮肤病治疗从「经验性干预」向「精准化靶向」的跨越,为医工交叉助力中医药创新与慢性疾病治疗提供了典型范例。
好文章,需要你的鼓励
















