好医友获悉,近日美国 FDA 宣布批准 PD-1 抑制剂 Libtayo(Cemiplimab-rwlc)一项新适应,用于一线治疗 PD-L1 高表达(肿瘤比例评分≥50%)的晚期非小细胞肺癌(NSC
好医友获悉,近日美国 FDA 宣布批准 PD-1 抑制剂 Libtayo(Cemiplimab-rwlc)一项新适应,用于一线治疗 PD-L1 高表达(肿瘤比例评分≥50%)的晚期非小细胞肺癌(NSCLC)患者。这些患者的肿瘤必须是转移性或局部晚期肿瘤,不适合手术切除或最终放/化疗,并且肿瘤不携带 EGFR、ALK 或 ROS1 畸变。
在一项关键的试验中,Libtayo 在延长总体生存期方面显著优于化疗。意味着,Libtayo 成为了继 K 药、T 药后又一款获批单药治疗 PD-L1 高表达肺癌患者的免疫药物。
稳坐死亡率「头把交椅」的肺癌
无论是在全球还是在中国,肺癌仍是癌症死亡的主要原因。2020 年,全球新确诊病例约 220 万。
肺癌主要分为小细胞肺癌和非小细胞肺癌,而 NSCLC 约占所有肺癌的 85%。NSCLC 患者中有 75% 的人确诊时已是晚期,且新确诊病例中,PD-L1 表达≥50% 的肿瘤细胞约占总数的 25%~30%。
作为全球癌症死亡的主因,晚期 NSCLC 患者仍需要更多的治疗选择。
PD-1 抑制剂:Libtayo
Libtayo 是一款针对 PD-1 靶点的全人类单克隆抗体药物。通过与 PD-1 特异性性结合,可以重新激活 T 细胞受体信号,增强人体免疫系统对于癌细胞的杀伤能力,达到自然抗癌的效果。
早在 2018 年,Libtayo 首次获批用于治疗晚期皮肤鳞状细胞癌(CSCC)成人患者。
而在今年 2 月初,Libtayo 获批治疗治疗先前已用 Hedgehog 蛋白通路抑制剂(HHI)治疗或不适合 HHI 治疗的晚期基底细胞癌(BCC)患者。
在所有批准的适应症中,Libtayo 的推荐剂量为每三周 30 分钟静脉输注 350 mg,直至疾病进展或出现不可接受的毒性。
值得一提的是,Libtayo 也已在中国获批开展临床试验,与化疗联用或单药一线治疗晚期或转移性 NSCLC 患者。
死亡风险降低 43%!试验数据惊艳
这一批准是基于一项开放标签、随机、多中心的 3 期临床试验(称为 EMPOWER-Lung 1)的积极数据。
试验入组了 710 例 PD-L1 高表达(≥50%)的晚期 NSCLC 患者,随机分配接受 Libtayo 一线单药治疗或含铂化疗。主要终点是 OS 和 PFS,次要终点包括总体缓解率、缓解持续时间和生活质量。
最近发表在《柳叶刀》杂志上的试验数据显示:
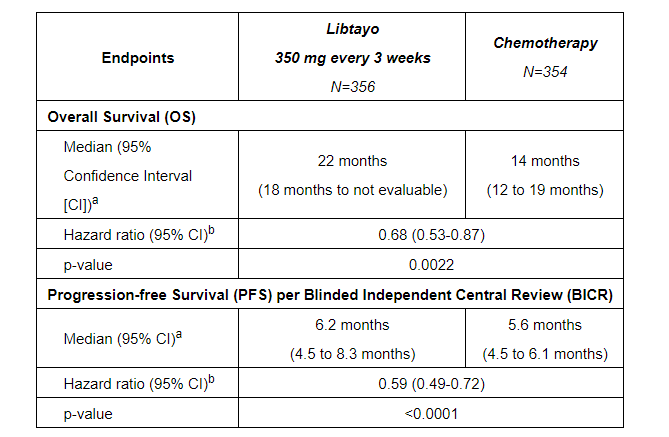
1、在肿瘤 PD-L1 表达≥50% 的患者中,与化疗组相比,Libtayo 治疗组将死亡风险降低了 43%,且安全性和耐受性良好。
2、Libtayo 治疗组的中位总生存期(OS)为 22 个月,而化疗为 14 个月。
3、Libtayo 单药治疗还可改善患者无进展生存期(PFS)。治疗组 PFS 为 6.2 个月,对照组为 5.6 个月。
值得注意的是,这项试验允许最初分到化疗组的患者在疾病进展后转到 Libtayo 组接受治疗。因此,目前约 70% 的化疗组患者在试验过程中转到 Libtayo 组。
这是 Libtayo 在美国获得的第三项适应症,这一批准意味着晚期非小细胞肺癌患者迎来了一种有效的治疗新方案。
好医友汇总了非小细胞肺癌已获批一线免疫疗法(中美):
美国:
2016 年 10 月,美国 FDA 批准帕博利珠单抗(K 药)用于一线治疗 PD-L1 高表达的转移性非小细胞肺癌患者。
2017 年 5 月,FDA 批准博利珠单抗(K 药)与培美曲塞和卡铂联合用于转移性非小细胞肺癌患者的一线治疗,无论 PD-L1 表达水平。
2018 年 10 月,美国 FDA 批准帕博利珠单抗(K 药)联合卡铂、紫杉醇/白蛋白紫杉醇用于鳞状非小细胞肺癌一线治疗,无论 PD-L1 表达水平。
K 药已完成了对非小细胞肺癌的全覆盖。
2020 年 5 月,FDA 批准 PD-1 抑制剂纳武利尤单抗(O 药)联合 CTLA-4 抑制剂伊匹木单抗(Y 药)及含铂双药化疗用于一线治疗 EGFR 和 ALK 阴性的转移性或复发性非小细胞肺癌,无论 PD-L1 表达水平。
2020 年 5 月,FDA 批准阿替利珠单抗(T 药)单药一线治疗 PD-L1 高表达、且 EGFR 和 ALK 阴性的转移性非小细胞肺癌患者。
中国:
2019 年 3 月,国家药监局批准 K 药联合化疗用于 EGFR 和 ALK 阴性非鳞状晚期非小细胞肺癌的一线治疗,无论 PD-L1 表达水平。
2019 年 10 月,国家药监局批准 K 药单药一线治疗 PD-L1 阳性非小细胞肺癌,无需联合化疗。
2019 年 11 月,国家药监局批准 K 药联合化疗(卡铂+紫杉醇)一线治疗晚期鳞状非小细胞肺癌。
2020 年 6 月,国家药监局批准国产 PD-1 抑制剂卡瑞利珠单抗(艾瑞卡)联合培美曲塞和卡铂用于无 EGFR 和 ALK 阴性、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌一线治疗。
2021 年 1 月,国家药监局批准国产 PD-1 抑制剂替雷利珠单抗(百泽安)联合紫杉醇和卡铂用于局部晚期或转移性鳞状非小细胞肺癌的一线治疗。替雷利珠单抗成为首个获批一线治疗晚期肺鳞癌的国产 PD-1。
2021 年 2 月,国家药监局批准国产 PD-1 抑制剂信迪利单抗(达伯舒)联合培美曲塞和铂类化疗用于 EGFR 和 ALK 阴性、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌患者一线治疗。
参考资料:
https://www.fda.gov/drugs/drug-approvals-and-databases/fda-approves-cemiplimab-rwlc-non-small-cell-lung-cancer-high-pd-l1-expression
https://www.onclive.com/view/fda-approves-cemiplimab-for-frontline-advanced-nsclc-with-high-pd-l1-expression
*声明:本内容仅代表文章来源方观点,不代表本站立场。本内容仅供医学药学专业人士阅读,不构成实际治疗建议。
封面图来源:站酷海洛
好文章,需要你的鼓励
















