来源:首都医学科学创新中心
2026 年 4 月 3 日,首都医学科学创新中心冷方伟教授、SUNY Downstate 的 Yu-San Huoh 教授以及哈佛医学院 Sun Hur 教授在 Nature Immunology 发表综述文章「Multimerizing transcription factors FOXP3 and AIRE as chromatin architectural regulators」。该文章整合免疫学、基因组学、生物化学与结构生物学的最新进展,系统梳理了 FoxP3 与 Aire 这两个关键免疫转录因子的作用机制,并提出重要新概念:转录因子可通过多聚化重塑染色质三维结构,从而在整体层面调控基因表达网络,为理解免疫耐受及复杂转录调控提供了新的视角。

FoxP3 是调节性 T 细胞(Treg)的核心转录因子,在免疫耐受的建立与维持中发挥关键作用。然而,其作用机制存在一个「谜题」:FoxP3 在基因组上广泛结合,却仅对少数基因产生直接且幅度有限的调控效应。最新研究表明,FoxP3 能够在富含 TnG 微卫星的 DNA 区域形成稳定且具有可塑性的多聚体,像「分子桥梁」一样连接远距离染色质位点,促进染色质环及更高阶结构的形成。由此,FoxP3 不再仅是作用于单基因的「开关」,而更像一个「染色质架构师」,通过调节基因组空间结构,在全局层面精细调控基因表达(Nature, 2023; Molecular Cell, 2025)。此外,不同形式的 FoxP3 组装(如二聚体与高阶多聚体)还能协同参与 DNA 识别与桥接,作为组装起点驱动更大尺度的三维结构重塑(Immunity, 2022; Cell reports, 2025)。
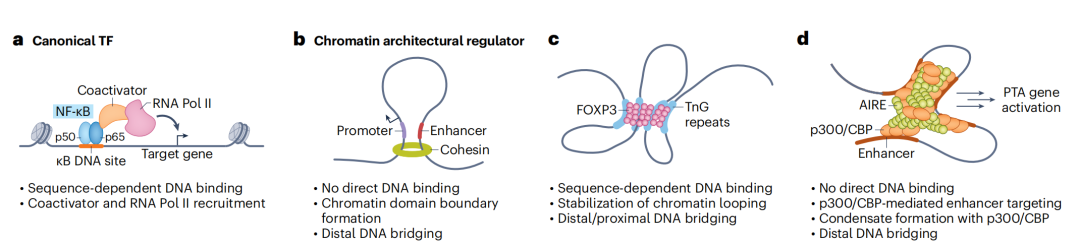
另一关键因子 Aire 则在胸腺中主导中枢免疫耐受,通过诱导外周组织抗原表达来清除自身反应性 T 细胞。不同于传统转录因子,Aire 缺乏明确的序列特异性 DNA 识别能力,而是依赖 CARD 结构域发生自发聚合,在细胞核中形成离散的「凝聚体」。这些凝聚体富集转录共激活因子(如 p300/CBP),并定位于预先活跃的增强子区域,构建转录活跃的「枢纽环境」。值得注意的是,Aire 高占据的基因组区域与其强烈激活的靶基因往往并不重叠,提示其可能通过远距离甚至跨染色体的瞬时接触实现基因激活,呈现出随机性和细胞间异质性的表达特征。同时,Aire 的聚合受到精细调控:PHD 结构域通过识别广泛存在的 H3K4me0 标记抑制非特异性聚合,而 CTT 与共激活因子的相互作用则在特定染色质环境中触发聚合,实现「抑制—激活」的动态平衡(Nature Communications, 2020; Nature Immunology, 2024)。
总体而言,无论是 FoxP3 通过多聚化桥接染色质形成结构网络,还是 Aire 通过凝聚体构建转录枢纽,这些发现共同指向一种新的转录调控模式:基因表达不仅取决于转录因子「结合在哪里」,更取决于其「如何组装以及如何塑造染色质的三维结构」。这一「结构维度」的新框架,不仅解释了传统模型难以回答的问题,也提示类似机制可能广泛存在于其他转录因子中,为理解复杂生命过程中的基因调控网络提供了新的视角,并为未来靶向转录因子「组装状态」的精准干预策略开辟了新方向。
好文章,需要你的鼓励
















