来源:《临床儿科杂志》
作者:梁志如 1,2 郭林梅 1 王 霏 1,2 赵晓云 1
作者单位:1. 中国人民解放军联勤保障部队第九四○医院儿科;2. 西北民族大学医学部
基金项目:甘肃省自然科学基金项目
通信作者:赵晓云 电子信箱:zxl2296@163.com
推荐引用格式:
梁志如, 郭林梅, 王霏, 等. 狼疮性肠炎还是炎症性肠病:1 例合并胃肠道症状的系统性红斑狼疮诊治报告 [J]. 临床儿科杂志, 2026, 44(1): 56-63 DOI:10.12372/jcp.2026.24e0351
LIANG Zhiru, GUO Linmei, WANG Fei, et al. Lupus enteritis or inflammatory bowel disease: a report of the diagnosis and treatment of systemic lupus erythematosus complicated with gastrointestinal symptoms[J]. Journal of Clinical Pediatrics, 2026, 44(1): 56-63 DOI:10.12372/jcp. 2026.24e0351
摘要
系统性红斑狼疮(SLE)和炎症性肠病(IBD)是两种以异常免疫应答为特征的系统性疾病,发病原因主要由易感基因和环境因素之间的相互作用,在临床中,这两种疾病同时发生比较少见。本例报告中,患儿,女,以腹痛起病入院,经检查诊断为系统性红斑狼疮、溃疡性结肠炎。经英夫利昔单抗(IFX)联合免疫抑制剂治疗,患儿自身免疫症状得到缓解。因此,对患有 SLE 的患者出现胃肠道症状如腹痛或腹泻时,特别是如果与 SLE 发作无关,应谨慎排除 IBD。
关键词
系统性红斑狼疮; 溃疡性结肠炎; 英夫利昔单抗; 儿童
引言
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种以致病性自身抗体和免疫复合物形成并介导多器官、组织损伤的自身免疫性疾病。肠道受累并非罕见,SLE 常见的肠道损伤包括狼疮性肠炎(lupus enteritis,LE)、蛋白丢失性肠病(protein-losing gastroenteropathy,PLE)、假性肠梗阻(intestinal pseudo-obstruction,IPO)等,其中以 LE 最多见。溃疡性结肠炎(ulcerative colitis,UC)是炎症性肠病(inflammatory bowel disease,IBD)的常见类型之一,是一种慢性免疫介导性肠道疾病,病变以直肠或远端结肠的浅溃疡为主,严重者可累及全结肠。UC 在我国发病率逐渐升高,其病因复杂、病程漫长、病变范围及轻重程度存在个体差异,复发率较高。SLE 合并 UC 国外虽相对报道较多,但是国内较少见。本文报道了 1 例 SLE 治疗过程中合并发生 UC 的儿童案例,在治疗过程中使用了近年来较受关注的生物制剂英夫利昔单抗(infliximab,IFX),以供临床医师参考与讨论。
1 病史描述
1.1 第一次入院
患儿,女,10 岁,因间断腹痛 10 天伴发热 1 天于 2018 年 2 月收入中国人民解放军联勤保障部队第九四〇医院儿科。患儿于就诊前 10 天间断出现腹痛及双下肢疼痛,无皮疹、关节肿胀,无腹泻,大便性状未见改变,未见黏液脓血便。入院前 1 天出现发热,体温 39.2℃。因在门诊对症治疗无效,收治入院。
入院时体温 36.7℃,呼吸 26 次/分,心率 110 次/分;贫血貌,双侧颊部可见红斑,压之褪色;触及颈部淋巴结肿大;心律不齐,心音低钝,心前区闻及 3/6 级收缩期吹风样杂音;腹软,脐周轻压痛,肝脾肋下未触及,肠鸣音如常;双下肢无浮肿;神经查体未见异常。血常规示白细胞计数(WBC)2.44×109/L、中性粒细胞(NEU)1.19×109/L、红细胞(RBC)2.19×1012/L、血红蛋白(Hb)63 g/L、血小板计数(PLT)195×109/L;C-反应蛋白(CRP)77.6 mg/L、红细胞沉降率(ESR)77 mm/h;补体 C3 52.3 mg/dL、补体 C4 13.6 mg/dL;乳酸脱氢酶(LDH)1003IU/L、LDH-1 407 IU/L、肌酸激酶(CK)772 IU/L、肌酸激酶同工酶(CK-MB)32 IU/L、天冬氨酸氨基转移酶(AST)124 IU/L、丙氨酸氨基转移酶(ALT)44 IU/L、甘油三酯(TG)2.49 mmol/L;肌红蛋白 221.9 μg/L;粪常规示隐血试验弱阳性;尿常规正常;铁蛋白 3807 μg/L、铁离子 8.2μmol/L、不饱和铁结合力 61.2μmol/L、转铁蛋白 1.5 g/L。骨髓细胞学检查示粒系增生,中幼粒比例增高,红系增生,晚幼红比例增高,淋巴细胞正常,提示增生性贫血,排除急性白血病可能;EB 病毒抗体 IgA、IgG 阳性;柯萨奇病毒 IgG 阳性,埃可病毒 IgG 阳性;巨细胞病毒 IgG、IgM 阴性;结核菌γ干扰素释放实验、血清结核抗体均阴性;真菌葡聚糖、内毒素均正常;抗核抗体(ANA)阳性(1∶320)、抗 dsDNA 抗体弱阳性、抗 Sm 抗体阳性、抗 rRNP 抗体阳性、抗 U1-snRNP 抗体阳性。胸片示心影明显增大,彩色多普勒超声心动图提示心包积液。胸部 CT 示两肺正常,心腔密度低于心肌,心包积液。腹部彩色多普勒超声示肠系膜淋巴结肿大,肝、胆、胰、脾、双肾正常。
根据 2012 年系统性红斑狼疮国际协作组(SLICC)发布的 SLE 分类标准,诊断为 SLE。结合患儿发热、肌炎、低补体血症、抗双链 DNA 抗体升高、白细胞计数减少等临床证据,SLEDAI-2000 评分 10 分,提示中度活动。SLE 出现消化道症状并不少见,但很多症状通常与疾病活动无关。本例患儿发病以心脏、血液系统受累为主,胃肠道症状除腹痛外,无其余特异性表现,腹痛原因考虑急性肠系膜淋巴结炎或 SLE 相关的胃肠道症状。遂给予泼尼松(10 mg,tid)及抗感染、改善心肌功能、纠正贫血等治疗 11 日,症状缓解后出院。出院诊断为 SLE、心包积液、重度缺铁性贫血。出院后继续予泼尼松(10 mg,tid)治疗。
1.2 第二次入院
出院 1 个月后,患儿再次出现发热并伴腹痛,脐周明显,呈阵发性钝痛,可耐受,无远处放射,门诊予口服抗感染、调节肠胃药物治疗 1 周,效差,遂第二次收治入院。入院时体温 39℃,咽充血,口腔黏膜见 2 个约 0.5 cm 大小溃疡,肝肋下可触及 2 cm,质软,边缘锐利,脾脏未触及。血常规示 WBC 3.38×109/L、NEU 2.54×109/L、 RBC 2.97×1012/L、Hb 91 g/L、PLT 194×109/L;抗核抗体阳性(1∶320)、抗 Sm 抗体阳性、抗 U1-snRNP 抗体阳性;补体 C3 54 mg/dL、补体 C4 12.7 mg/dL;LDH 743IU/L、LDH-1 217IU/L、AST 623IU/L、ALT 255IU/L、TG 2.32 mmol/L、ESR 89 mm/h;尿、粪便常规正常;彩色多普勒超声心动图示左室轻度扩大。患儿 2 次病情发作均有腹痛,完善腹部彩色多普勒超声示脂肪肝,余无异常,腹痛原因考虑为 SLE 相关的胃肠道症状;予保肝、调理肠胃对症治疗。患儿已口服中等剂量泼尼松治疗 1 月,病情复发,且肝酶明显升高,临床诊断为 SLE 活动期。为快速控制症状,在泼尼松(25 mg,bid)水平上加用环磷酰胺(首次剂量 0.5 g),治疗 10 日,症状好转后出院。出院后给予环磷酰胺(0.6 g,1 次/月)治疗 5 个月,继续环磷酰胺(0.6 g,3 个月 1 次)维持序贯治疗 5 次。病情控制良好,泼尼松逐渐减量至 15 mg/次,2 日 1 次。
1.3 第三次入院
2020 年 2 月,患儿因间断呕吐 3 天入院,进食后即吐,非喷射性,呕吐为胃内容物,未见咖啡样血性物,伴剑突下阵发性疼痛,无远处放射,无发热头痛、认知功能障碍及精神异常,大小便正常,体重减轻 3 kg。双侧颊部可见红斑,伴色素沉着;腹软,右上腹、剑突下压痛阳性,肝脾肋下未触及,肠鸣音活跃,神经系统无明显异常。
入院后暂考虑 SLE 胃肠道受累、狼疮性脑病待查,给予泼尼松(15 mg,2 日 1 次)、止吐、补充电解质、保护胃黏膜等治疗 3 天,效差,仍频繁呕吐,且呕吐物中可见黄绿色胆汁样物,大便为黑色稀样便,3~7 次/天。将泼尼松调整为(30 mg,qd)治疗 3 天,呕吐逐渐好转。查血、尿、便常规未见异常;抗核抗体阳性(1∶320)、抗 dsDNA 抗体弱阳性、抗 Sm 抗体阳性、抗 rRNP 抗体阳性、抗 U1-snRNP 抗体阳性;补体 C3 57 mg/dL、补体 C4 7.2 mg/dL;ESR 42 mm/h;CK-MB 54IU/L、TG 2.59 mmol/L、高密度脂蛋白胆固醇(HDL-C)0.78 mmol/L、低密度脂蛋白胆固醇(LDL-C)3.3 mmol/L;头颅核磁及腰椎穿刺未见异常,排除狼疮性脑病可能;腹部 CT 示肝脏密度弥漫性减低,考虑脂肪肝,腹盆腔积液,膀胱壁增厚,结直肠肠壁增厚、水肿;腹部彩超示肠管扩张、积液,左侧肾集合系统轻度分离。结合风湿免疫科意见,诊断活动性 SLE、LE,并建议完善胃镜检查排除胃部疾病,家属拒绝。为控制狼疮活动,改善病情,予静脉甲基泼尼松龙冲击(600 mg,qd)联合静注免疫球蛋白(10 g,qd)治疗 3 天,患儿病情逐渐好转。出院后予泼尼松(25 mg,bid)联合羟氯喹(0.05 g/次,tid)维持治疗。1 周后继续第 11 次环磷酰胺序贯治疗。至 2020 年 6 月,患儿病情稳定,停止环磷酰胺冲击,院外给予泼尼松(15 mg,qd)联合羟氯喹(0.08 g,bid)及保护胃肠黏膜等对症治疗,病情控制良好,泼尼松逐渐减量至 7.5 mg,qd。
1.4 第四次入院
2022 年 8 月再次因发热伴腹痛、稀便 2 天住院,大便无黏液脓血,便常规未见异常。补体 C3 56 mg/dL;抗核抗体阳性(1∶160)、抗 Sm 抗体弱阳性、抗 rRNP 抗体阳性、抗 U1-snRNP 抗体阳性、抗 dsDNA 抗体阴性。腹部彩超示肝实质光点细密增强,分布不均匀,右肝见较强回声;双肾集合系统分离;胆、胰、脾未见异常,腹腔未见积液及包块。为明确肝脏情况,进一步完善腹部核磁示腹腔内部分肠管扩张并积液、积气;肝左内叶囊肿,直径 0.9 cm;腹膜后、双侧髂血管旁及腹股沟区多发增大淋巴结;盆腔少量积液。给予胃镜检查,可见贲门炎症,食管、胃黏膜未见明显异常。诊断考虑 LE、肝囊肿。患儿近 2 年病情控制良好,此次反复考虑与 SLE 再次活动相关,同时需谨慎长期使用激素及羟氯喹引起的胃肠道不良反应。为控制病情,及达到去激素化或少激素化,给予泼尼松(30 mg,qd)联合羟氯喹(0.075 g,bid)、吗替麦考酚酯(0.75 g,bid)、麦滋林(0.67 g,tid)等对症维持治疗,患儿病情平稳。治疗 11 日出院后继续口服上述药物(泼尼松后逐渐减量至 10 mg,qd)。2023 年 9 月因腹痛 4 天入院,查腹部 CT 示双侧肾盂稍扩张,积水;结肠内较多内容物滞留。SLEDAI 评分 2 分,考虑低活动性 SLE,继续泼尼松联合羟氯喹、吗替麦考酚酯治疗,并给予抗感染、调理肠道菌群、保护胃肠黏膜治疗,病情好转。
1.5 第五次入院
2024 年 1 月患儿再次出现右上腹持续钝痛 6 天,伴恶心,无呕吐,食欲欠佳,大便干结,收住入院。体格检查发现全身未触及明显肿大淋巴结,心肺无异常,腹膨隆,叩诊左侧呈鼓音,右侧肝区压痛明显,腹肌略紧张,肝肋下可触及 1.5 cm,触痛明显,质中等偏硬。血常规示 WBC 10.51×109/L、NEU 9.63×109/L、RBC 4.92×1012/L、Hb 155 g/L、PLT 239×109/L;PCT 0.23ng/mL;纤维蛋白原 (FIB)5.79 g/L、D-二聚体 1.19 mg/L;血清 CRP 74.8 mg/L、补体 C3、C4 正常;抗核抗体阳性(1∶320)、抗 rRNP 抗体阳性、抗 U1-snRNP 抗体阳性;ESR 47 mm/h;便常规示隐血试验阳性。腹部彩超示肝内较强回声结节;胆、胰、脾、双肾、门静脉声像图未见异常。
患儿起病初,诊断 SLE 活动期,于早期使用糖皮质激素联合环磷酰胺冲击治疗。在病程中,患儿反复出现腹痛症状。至第三次入院时,完善腹部彩超及 CT,符合 LE 表现,故给予激素联合羟氯喹治疗。并于第四次入院时,联合免疫抑制剂吗替麦考酚酯治疗,患儿病情得到有效缓解。2024 年 1 月患儿因腹痛再次入院,为进一步明确腹痛病因,行上腹部磁共振成像(MRI)+磁共振胰胆管成像(MRCP)+扩散加权成像(DWI)示肝左内叶囊肿;双侧肾盂改变,考虑壶腹型肾盂可能;横结肠冗长、迂曲、扩张,其内较多内容物。肠镜示升结肠肝曲侧 - 横结肠中段见多发半环周不规则溃疡形成,覆白苔,周围黏膜充血。见图 1。余结肠、直肠、盲肠所见黏膜光滑,血管网清晰,肠管舒缩好,未见异常病变。病理结果示黏膜组织,灶性上皮脱落,肉芽组织增生,间质炎细胞浸润。符合溃疡征象伴急性活动期炎症改变。见图 2。
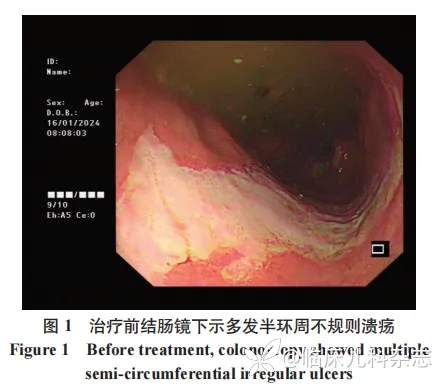
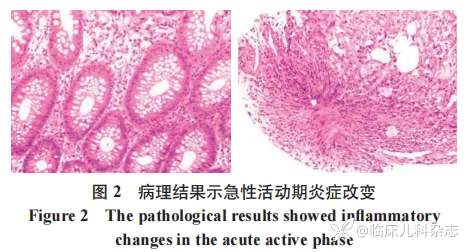
2 鉴别诊断
2.1 SLE 伴感染性肠炎
多种因素包括细菌、病毒、真菌、寄生虫等均可引起胃肠道反应,由于感染主要侵犯局部黏膜等因素,可能出现发热、呕吐、腹痛、腹泻等,经对症治疗后多预后良好。其中肠结核是结核分枝杆菌引起的肠道慢性特异性感染,常继发于开放性肺结核或喉结核而吞下含菌痰液;临床症状多为发热、盗汗等结核毒血症状;肠镜检查发现病变部位主要位于回盲部的炎症、溃疡、炎性息肉或肠腔狭窄,也可累及结直肠;可通过肠黏膜病理活检发现干酪样肉芽肿进行确诊。
在确诊过程中还需考虑 EB 病毒相关性肠炎的可能性。累及消化道的 EB 病毒感染临床少见,主要表现为腹痛、腹泻、发热为主,伴体重下降、食欲减退等非特异性表现,病情进行性加重,在晚期可出现高热、便血。EB 病毒相关性肠炎的肠道表现为多发溃疡,全消化道均可受累,结肠病变最多见;溃疡的形状、深度和大小存在差异,表现为散在分布的深大溃疡,为弹坑样、穿凿样,伴有黏膜糜烂、充血水肿,对症处理后黏膜可完全愈合。
患儿自发病以来,经多次检查,结核菌γ干扰素释放实验及血清结核抗体均阴性,内毒素及真菌葡聚糖检测正常,大便常规未检出寄生虫,且肠镜示肠道表现与感染性肠炎表现有差异,因此可基本排除结核杆菌、细菌、真菌、寄生虫、EB 病毒相关性肠炎所致结肠溃疡,并考虑将其归因于 SLE 相关的胃肠道表现。
2.2 狼疮性肠炎
LE 是 SLE 患者急性腹痛的主要原因之一,多种因素包括细菌感染、巨细胞病毒、药物反应、嗜酸性粒细胞增多、不洁饮食等可诱发 LE,其典型的症状包括呕吐、腹痛、腹泻,通常与肠系膜血管炎所致的肠道缺血性改变有关。目前普遍认为,腹部 CT 检查可以作为 LE 诊断的重要依据,典型特征包括肠壁水肿增厚(>3 mm)、肠腔扩张、肠壁异常强化(靶心征)、肠系膜血管充血及血管数量增多(梳状征)、肠系膜脂肪变薄和腹腔积液,可出现肾盂、输尿管积水,膀胱扩张,膀胱壁增厚,腹水、肠系膜淋巴结增大等影像学表现。然而,其他疾病如胰腺炎、机械性肠梗阻、炎症性肠病、腹膜炎及肠缺血等的腹部 CT 表现也可出现上述现象,因此,腹部 CT 检查并不能作为诊断 LE 的唯一标准。大多数 LE 患者的胃镜和肠镜检查结果并无明显特异性改变,且累及结肠者较少 [1],内镜下组织活检的主要表现为慢性炎症细胞浸润,特别是以淋巴细胞为主,可伴有黏膜水肿。
多数报道提示,LE 对糖皮质激素的反应好,经及时诊断和治疗,患者预后一般较好。对于糖皮质激素治疗无效、复发性 LE 及重症 SLE 患者而言,可联合免疫抑制剂(如环磷酰胺、麦考酚酯等)治疗,并有效预防复发 [2-3]。本例患儿诊断为 LE 后,给予激素联合免疫抑制剂及保护胃肠黏膜长期治疗后,病情控制尚可。患儿此次再次出现腹痛,综合各项检查,考虑溃疡征象可能与 LE 无关。
2.3 溃疡性结肠炎
UC 是一种累及结肠的慢性非特异性炎症性疾病,病变主要限于大肠黏膜与黏膜下层,呈连续性弥漫性分布,通常始自直肠,逐渐延伸至结肠近端,可累及全结肠甚至末端回肠。主要症状为腹痛、反复发作的腹泻、及黏液脓血便等,可能有贫血、铁缺乏、白细胞增多、血沉加快、CRP 增高。肠镜及活检是本病诊断与鉴别诊断的最重要手段之一。内镜下可见黏膜血管形态消失、充血、水肿、易脆、出血、糜烂、溃疡等,正常黏膜和炎症之间有明显的界限。组织学检查可见活动期时黏膜固有层内弥漫性中性粒细胞、淋巴细胞、浆细胞、嗜酸性粒细胞浸润及隐窝炎,慢性期时隐窝结构紊乱,腺体萎缩变形、排列紊乱及数目减少,杯状细胞减少,可出现潘氏细胞化生及炎性息肉。有文献显示,组织学中浆细胞的增多可能是诊断 UC 最早的特征。在症状发作的 2 周内有 1/3 的患者可见黏膜浆细胞的增多,相比之下,只有 20% 的患者在前 2 周内有明显的隐窝改变,因此,早期 UC 与感染性结肠炎通常较难鉴别,且隐窝结构的变化在儿童中比成年人更少见 [4]。
本例患儿以腹痛为主,无典型黏液脓血便、无反复发作的腹泻,肠镜示溃疡主要累及结肠,直肠黏膜无溃疡表现,病理示急性活动期炎症改变。在排除其他原因所致结肠炎的基础上,考虑不典型 UC,且早期使用糖皮质激素及免疫抑制剂可能减轻 UC 的病情。
3 诊疗与转归
经鉴别诊断,综合考虑诊断为「系统性红斑狼疮、溃疡性结肠炎」。UC 的一线治疗方案为氨基水杨酸制剂及糖皮质激素。5-氨基水杨酸(5-ASA)制剂和柳氮磺吡啶(SASP)常用于轻、中度 UC 的诱导缓解及维持治疗,对 5-ASA 疗效不佳的中度及重度病人首选药物为糖皮质激素。因本例患儿 UC 发生在长期使用激素及免疫抑制剂治疗期间,考虑类固醇难治性 UC。近年来,IFX、环孢素被广泛推荐使用于类固醇难治性 UC 患者的转换治疗 [5],并有效改善 UC 患者的预后。故给予泼尼松(40 mg/d)、羟氯喹(0.075 g 每次、2 次/日)、吗替麦考酚酯(0.75 g/次、2 次/日)联合 IFX 治疗,出院后继续服用上述药物,于首次给药后第 2 周、第 6 周、第 8 周继续来院复查并给予 IFX 序贯治疗。期间电话随访,家长诉患儿腹痛明显缓解。于 2024 年 3 月住院复查,尚未见药物不良反应。患儿病情平稳,复查抗核抗体阳性(1∶100)、抗 rRNP 抗体阳性、抗 U1-snRNP 抗体阳性;ESR 8 mm/h;便常规示正常。肠镜显示横结肠中段见半环周浅溃疡形成。覆薄白苔,周围黏膜充血,呈挛缩、缩窄状。其对侧见白色瘢痕形成。较未治疗前溃疡数量明显减少、面积缩小,呈愈合趋势。见图 3。
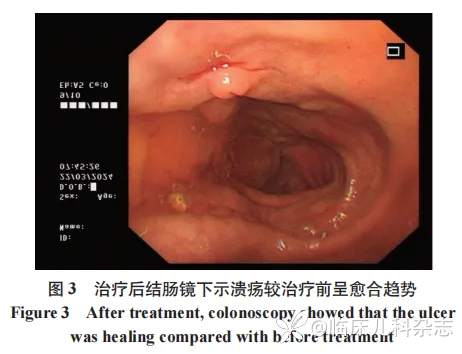
2025 年 4 月,患儿于我院复查,抗核抗体阳性(1:100)、抗 rRNP 抗体阳性、抗 U1-snRNP 抗体阳性;便常规示正常。肠镜显示降结肠、直肠黏膜略肿胀,血管网清晰,肠管舒缩好,未见异常病变。见图 4。具体诊疗同随访时间轴见表 1。
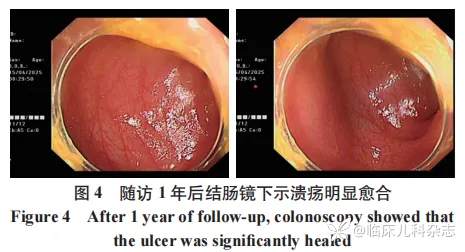

4 讨论
SLE 是一种以致病性自身抗体和免疫复合物形成并介导器官、组织损伤的自身免疫病。IBD 是一组以肠黏膜炎症为特征的慢性复发性疾病,包括 UC 和克罗恩病(Crohn’s disease,CD)。关于 SLE 和 UC 并存的报道很少,1964 年一项关于 SLE 的报道显示,在 520 例 SLE 患者中仅发生 2 例(0.4%)UC[6]。目前尚不清楚 SLE 和 IBD 同时发生是偶然情况还是真正的相关联,关于 SLE 和 IBD 之间的共同遗传易感性,仍存在争议。De Jager 等 [7] 研究显示,IBD 风险等位基因 CARD 15 (908R) 可能对 SLE 的发病风险有很大影响。但相反的是,在另一项研究中,与 IBD 相关的风险等位基因 CARD15 变异对 SLE 的易感性没有影响 [8]。且这两种疾病对类似的抗炎和免疫抑制药物,如 SASP、类固醇、甲氨蝶呤和硫唑嘌呤等都有反应,提示两者可能存在某种程度的相关性,但还需进一步的研究 [9]。
约 50% 的 SLE 患者会出现胃肠道症状 [10],腹痛最为常见,在临床诊断中,较难与 IBD 相鉴别,尤其是 UC,难以与 LE 鉴别。两种疾病都有一些共同的胃肠道特征,临床上主要依靠影像、内窥镜及组织病理鉴别。UC 在内镜下可见弥漫性糜烂和多发性浅溃疡,黏膜弥漫性充血水肿、颗粒状,脆性增加;组织病理可见固有膜全层弥漫性炎症、隐窝脓肿、隐窝结构异常、杯状细胞缺少等。SLE 患者胃肠道最常见的病理学病变是慢性、非特异性黏膜炎症和血管病变引起的缺血性改变,大致分为与血管炎相关且经常导致穿孔的病变和非特异性溃疡性或肉芽肿性结肠炎两类 [11]。本例患儿肠镜及活检未能证实血管炎存在,且穿孔很少发生在 UC 中,但经常在 LE 中观察到,因此有助于鉴别诊断。UC 可发生在 SLE 诊断之前或之后,大多数患者对类固醇联合羟氯喹或硫唑嘌呤有很好的反应,预后通常较好 [12-13]。
抗肿瘤坏死因子-α(TNF-α)是一种通过调节免疫细胞增殖、分化和存活而参与炎症和免疫反应的细胞因子。这些促炎性细胞因子通过激活免疫细胞,产生毒性分子,包括超氧产物、趋化因子、蛋白酶和细胞因子,导致组织损伤和炎症发展 [14],这类药物的代表主要为 IFX、阿达木单抗和赛妥珠单抗等,IFX 是 TNF-α人鼠嵌合体免疫球蛋白 G1 单克隆抗体,通过与跨膜性和可溶性 TNF-α结合,阻碍其与受体结合,从而抑制其活性,达到抗炎效果 [15]。对于 UC 的治疗,可针对不同病情使用不同类别的药物来诱导和维持疾病的缓解。通常,轻度至中度 UC 病例的首选治疗方案包括氨基水杨酸类药物,中度至重度可联合其他治疗包括使用皮质类固醇、免疫抑制剂和生物制剂,但在少数情况下,SASP、5-ASA 或 TNF-α拮抗药物等可能诱导药物性狼疮的发生。TNF-α既通过其促炎活性发挥有害的组织损伤作用,也可通过抑制侵袭性自身免疫反应发挥有益的活性。而 SLE 是一种自身免疫紊乱和炎性损伤的疾病,因此在这种自身免疫易感的慢性炎性疾病中阻断 TNF-α可能导致不同的结局,这取决于治疗的时间和持续时间 [16]。
近年来,随着生物制剂的发展,有证据表明在中度至重度 IBD 的早期使用 IFX 可以获得良好的治疗效果 [17]。接受抗 TNF-α治疗的患者很少出现狼疮综合征,且 IFX 可能对狼疮性肾炎患者有益 [18]。但在文献中关于 TNF-α拮抗类药物应用于 SLE 合并 UC 的病例较少提及。有报道显示,SLE 合并 CD 的患者在接受 IFX 治疗后,两种疾病都得到了缓解 [19-21]。同样免疫抑制剂的应用也可获得良好的疗效。报道显示 1 例 SLE 合并 UC 的 30 岁女性,在应用甲基强的松及环磷酰胺冲击 6 个月,且继续口服激素、5-氨基水杨酸类药物和羟氯喹等治疗后,获得了良好的疗效 [22]。同样,1 例 CD 合并 SLE 的 50 岁女性在接受甲泼尼龙、环磷酰胺冲击,及口服沙利度胺、甲硝唑治疗 5 个月后,症状也得到了明显的改善 [23]。
回顾本例患儿初次就诊至今,因在胃肠系统的评价中未及时进行肠镜检查及病理学评估,且患儿早期使用糖皮质激素及免疫抑制剂药物可能延迟了明显的下消化道 UC 的发生,及对这两种疾病共存的认知不足,未能及时发现 UC 的发生。因此,在临床诊治中,如果已知患有 SLE 的患者出现胃肠道症状,如腹痛或腹泻,特别是如果与 SLE 发作无关,则应谨慎排除 IBD。本例患儿在应用 IFX 后,腹痛缓解,溃疡明显愈合。这提示 IFX 可能是一个合理的治疗选择,但其有效性和安全性需要进行长期跟踪。
5 最终诊断
①系统性红斑狼疮,②溃疡性结肠炎。
好文章,需要你的鼓励















