来源:《临床儿科杂志》
作者:吴进军 1 熊 昊 2 曾 辉 3 陈 智 2 杨 李 4 孙 鸣 4 王卓 2 杜 宇 2 祁闪闪 4 王 伟 4 张兰男 2
作者单位:1. 华中科技大学同济医学院;2. 华中科技大学同济医学院附属武汉儿童医院血液肿瘤中心;3. 武汉市第六医院/江汉大学附属医院肿瘤科;4. 华中科技大学同济医学院附属武汉儿童医院儿童血液疾病研究室
基金项目:国家自然科学基金青年基金项目;湖北省自然科学基金青年项目;湖北省自然科学基金创新发展联合基金项目;武汉市自然科学基金探索计划市属医疗机构临床研究重点专项项目
推荐引用格式:
吴进军, 熊昊, 曾辉, 等. 异基因造血干细胞移植联合化疗治疗儿童髓系肉瘤 7 例临床分析 [J]. 临床儿科杂志, 2026, 44(1): 44-50 DOI:10.12372/jcp.2025.25e1007
WU Jinjun, XIONG Hao, ZENG Hui, et al. Clinical analysis of allogeneic hematopoietic stem cell transplantation on pediatric myeloid sarcoma[J]. Journal of Clinical Pediatrics, 2026, 44(1): 44-50 DOI:10.12372/jcp.2025. 25e1007
摘要
目的 评估异基因造血干细胞移植 (allo-HSCT) 联合化疗治疗儿童髓系肉瘤 (MS) 的疗效。方法 回顾性分析于血液肿瘤中心确诊并治疗的 7 例 MS 患儿临床资料。结果 7 例 MS 患儿中,男 3 例,女 4 例;诊断中位年龄 5 岁 2 个月;1 例以「局部包块」就诊,6 例在确诊急性髓细胞性白血病(AML)后发现存在髓外浸润;MS 浸润部位包括头面部(4 例)、纵隔(2 例)、髂骨(1 例)。7 例患者均接受 CCLG-AML-2019 方案化疗并桥接 allo-HSCT 治疗。移植前均接受清髓预处理,其中 5 例采用后置环磷酰胺(PTCY),2 例采用经典白消安联合环磷酰胺(BUCY)方案。7 例患儿均回输 G-CSF 动员后采集的外周血造血干细胞,回输单个核细胞(MNC)中位数 19.87×108/kg,CD34+细胞中位数 12.87×106/kg。中性粒细胞植入中位时间+15(13~15)d,血小板植入中位时间+12(11~17)d。随访截至 2025 年 6 月 30 日,中位随访时间 1008(371~1814)d,5 例存活,2 例复发后死亡。无移植相关死亡发生,预计 3 年 OS 为 71%。结论 早期诊断儿童 MS 仍存在挑战,规范化疗并尽早桥接 allo-HSCT 对部分患者能获得相对较好的疗效。
关键词
髓系肉瘤; 急性髓细胞性白血病; 异基因造血干细胞移植; 儿童
引言
WHO 血液肿瘤分类第五版(2022 年)将髓系肉瘤(MS)定义为出现在骨髓解剖位置以外含有髓系母细胞的肿块 [1]。通常可浸润皮肤、软组织和中枢神经系统 (central nervous system,CNS) 等,是急性髓细胞性白血病 (acute myelocytic leukemia,AML)、骨髓增生异常综合征 (myelodysplastic syndrome,MDS)、骨髓增殖性肿瘤 (myeloproliferative neoplasms,MPN) 或 MDS/MPN 的一种独特组织型表现 [2],也有文献报道 MS 与 AML 可相互转化 [3],仅 1% 的 MS 病例是无骨髓受累情况下发病的,称为孤立性 MS[4]。既往研究显示儿童 MS 发病率低,临床表现多样,治疗效果欠佳,预后较差 [4]。本研究回顾性分析接受异基因造血干细胞移植 (allo-HSCT) 治疗的 7 例 MS 患儿的临床资料,现汇报如下。
1 对象与方法
1.1 研究对象
2020 年 1 月—2023 年 12 月武汉儿童医院血液肿瘤中心确诊并规范治疗 7 例 MS 患儿。所有患儿均完善 MICM 分型检查并符合 AML 诊断且影像学检查提示存在骨髓解剖位置以外的肿块。部分患儿通过外科切除或局部软组织穿刺获得病变组织后行病理检查,在无法进行活检的患儿中,可通过骨髓或外周血等其他组织的形态学和流式细胞术分析,以及与细胞遗传学和分子数据的结合,确立诊断 [5]。分别收集患儿性别、年龄、首发病情、局部肿物部位、影像学表现、MICM 分型及病理活检报告、治疗方法及疗效等资料。
所有患儿在接受化疗、放疗及 HSCT 前均向家长或法定监护人交代病情、治疗方案并签署相关检查及治疗同意书。本研究通过武汉儿童医院伦理委员会审批(No.2024 R086-F01)。
1.2 治疗方案
化疗:7 例患儿均根据 CCLG-AML-2019 方案接受诱导及巩固化疗,具体用药如下。第一疗程为阿糖胞苷+柔红霉素+高三尖杉酯碱(DAH);第二疗程为阿糖胞苷+伊达比星+高三尖杉酯碱(IAH);第三疗程为米托蒽醌+阿糖胞苷(MA)。以上药物剂量均参照 CCLG-AML- 2019 方案执行。
放疗:MS 对放射线敏感,成人研究发现采用螺旋断层放射治疗系统(TOMO)对 MS 患者进行放射治疗可有明显临床效果并降低复发率 [6],既往研究也建议儿童 MS 患者在 HSCT 之前行局部放射治疗以进一步清除残留病灶 [7]。
allo-HSCT:依据 CCLG-AML-2019 方案,MS 患儿均为高危组,在接受 2~3 个疗程化疗后,如有合适供者,均可接受 allo-HSCT。本研究所有患儿均在接受 2~3 个疗程规范化疗后接受 allo-HSCT。
移植方式:所有患儿接受 allo-HSCT 的移植物均为集落刺激因子(G-CSF)动员后采集的外周血造血干细胞,具体方法为 G-CSF 10 μg/(kg· d)×5d 动员供者外周血干细胞,第 5 天用费森尤斯血细胞分离机进行外周血造血干细胞采集。
预处理:7 例患儿均接受清髓预处理方案,具体用药方案如下。PTCY 方案,CTX 10 mg/(kg·d)×2d(-8d,-7d) ;Me-CCNU 250 mg/m2(-6d) ;白消安(Bu)0.8~1.2 mg/(kg·次 ),q6h× 4d (-5d,-4d,-3d,-2d,根据患儿体重调整具体用量);Flu 40 mg/(m2·d)×5d (-6d,-5d,-4d,-3d,-2d),CTX 50 mg/(kg·d)(+2d,+3d);BUCY 方案,CTX 50 mg/(kg·d)×4d(-9d,-8d,-7d,-6d),Bu 0.8~1.2 mg/(kg·次),q6h×4d (-5d,-4d,-3d,-2d,根据患儿体重调整具体用量);ATG 10 mg/kg,分 3 天(-4d,-3d,-2d)使用。
移植相关感染预防:所有患儿移植前常规口服复方磺胺甲噁唑预防卡氏肺孢子虫感染,静滴卡泊芬净预防真菌感染,使用更昔洛韦预防巨细胞病毒 (CMV) 感染(-10d~-1d),移植+1d 天开始使用阿昔洛韦预防病毒感染。定期监测患儿血液 EBV/CMV-DNA、单纯疱疹病毒(HSV)-I 型 IgM 抗体、HSV-II 型 IgM 抗体检测结果,每周监测导管培养、CRP、降钙素原、G/GM 试验。如发现细菌感染,予经验性广谱抗生素治疗并完善病原学辅检及药敏实验,再根据病原学结果调整治疗。
移植后预防复发:7 例患儿均参考《造血干细胞移植后白血病复发监测、治疗及预防中国专家共识》予 DLI 方案预防复发 [8],根据患儿血象选用地西他滨(+90d 开始给药,每次 10 mg/m2,1 次/周,共 24 次)化疗,对于地西他滨不能耐受者,可选用阿扎胞苷(+90d 开始给药,每次 75 mg/m2,1 次/周,共 24 次)化疗;于第 1 次化疗后隔日输注冻存供者外周血干细胞(有核细胞数约为 1×108/kg);如无不良反应发生且无复发,每月酌情再次 DLI 治疗,连续 2~3 次(根据患儿体重及造血恢复情况调整具体用量)。
1.3 随访
以患儿自确诊以来的住院病历、门诊记录及相关检测报告作为主要随访内容,通过查阅病历、电话随访等手段完成随访工作。存活患儿随访截止时间为 2025 年 6 月 30 日。
1.4 疗效标准
依据 CCLG-AML-2019 方案,总生存期 (OS) 定义为自诊断起至死亡或末次随访时间;完全缓解 (CR) 定义为临床无白血病浸润的症状和体征,外周血未发现白血病细胞,骨髓中原始细胞 ≤ 5%。血液学缓解 (HCR) 定义为临床无白血病浸润的症状和体征、外周血中性粒细胞 ≥ 1.5×109/L,血小板计数 ≥ 100×109/L,不存在白血病细胞,骨髓中原始细胞 ≤ 5%。分子生物学缓解 (MCR) 定义为流式细胞或融合基因微小残留病灶 (minimal residual disease,MRD) 转为阴性。患儿的临床特征以中位数、均值或百分率等表示。
2 结果
2.1 MS 患儿临床特征
纳入本研究的 7 例患儿中男性 3 例,女性 4 例;起病中位年龄 5 岁 2 个月(10 月龄~14 岁);7 例患儿中仅有 1 例(病例 2)以「局部包块」起病并诊断,6 例于诊断「AML」并进一步检查、评估过程中诊断。局部受累位置:头面部 4 例,纵隔 2 例,髂骨 1 例。5 例患儿病理诊断 MS,其中 4 例于移植前通过病变部位活组织检查确诊,1 例(病例 4)于移植治疗后 4 个月因分子学复发行病理活检确诊;另有 2 例患儿(例 6、例 7)家属多次拒绝病理活检,但根据骨髓细胞学、免疫分型、分子生物及遗传学等 MICM 结果,并结合影像学资料可临床诊断 MS[5]。所有 7 例患儿均完善 MICM 检查,见表 1。
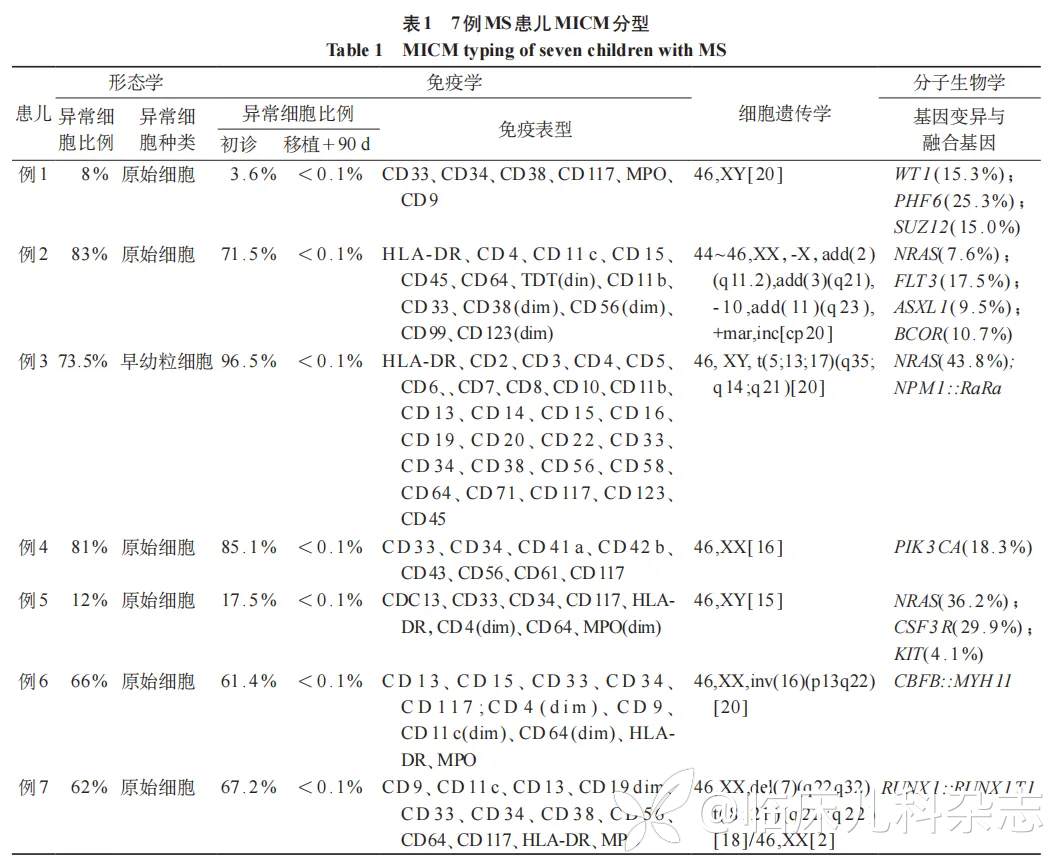
2.2 影像学表现
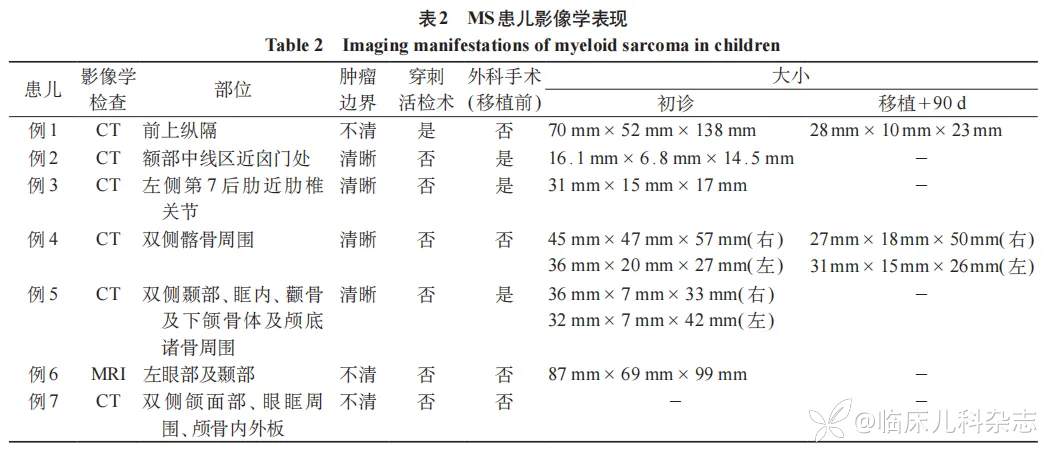
7 例患儿中 1 例患儿(例 6)以「左眼肿胀不适」入院,考虑肿物位于眼眶软组织内,故行 MRI 平扫+增强检查,余 6 例患儿均行 CT 平扫+增强检查。4 例患儿(例 2、例 3、例 4、例 5)的影像学表现为边界清晰的肿物,余 3 例患儿在影像学检查中表现为边界模糊的肿物。1 例患儿(例 7)病灶多发且边界模糊,余 6 例患儿病灶影像学表现为单发肿物。3 例患儿(例 2、例 3、例 5)通过外科手术切除局部肿物,故于移植后+90d 复查影像学检查中未见肿物影像,2 例(例 6、例 7)经过化疗、allo-HSCT 等治疗后+90d 复查亦未见明显异常组织影,2 例(例 1、例 4)患儿复查肿物大小较初诊有所减小。7 例患儿初诊及治疗后影像学表现见表 2。
2.3 治疗
化疗:所有患者均接受标准 CCLG-AML-2019 方案化疗。
放疗:对于无放疗禁忌症且有放疗适应证的 4 例患儿(例 1、例 3、例 4、例 7)在移植前行局部 TOMO 放疗。余 3 例患儿未行 TOMO 放疗,其中例 2 移植前化疗后骨髓抑制明显且肺部影像学结果提示多发结节,考虑合并真菌感染,例 5 于移植前未达到 CR 且化疗后骨髓抑制明显,例 6 因髓外浸润部位为右侧眼部周围软组织,故未予放疗。
allo-HSCT:7 例患儿在接受 2~3 个疗程化疗后均接受 allo-HSCT 治疗。其中例 1 接受中华骨髓库无关供者捐献的 HSCT,余 6 例患儿外周血造血干细胞来源于其父亲或母亲。回输单个核细胞(MNC)中位数 19.87(7.4~24.28)×108/kg,回输 CD34+细胞中位数 12.87(7.1~14.7)×106/kg。allo-HSCT 中位年龄为 2.9(0.8~14.0)岁,诊断距移植中位时间间隔为 110(84~572)天。粒细胞植入中位时间+15(13~15)d,血小板植入中位时间+12(11~17)d。7 例患儿 allo-HSCT 相关信息详见表 3。
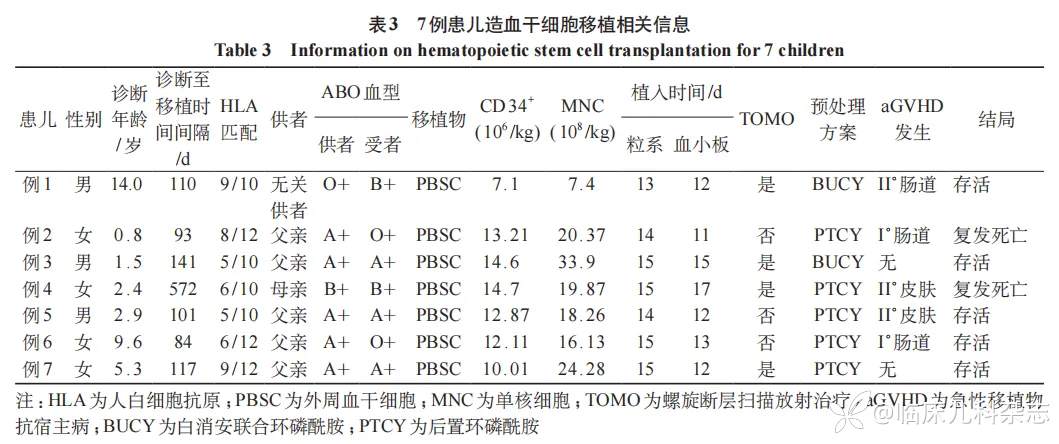
移植预处理:7 例患儿均接受以 Bu 为基础的清髓预处理方案;其中 5 例患儿为后置环磷酰胺 (PTCY) 方案,余 2 例(例 1、例 3)患儿为 Bu 联合环磷酰胺(BUCY)方案。
移植相关并发症:截至移植后+100d,5 例患儿发生 aGVHD 且均为 I~II˚,其中例 4、例 5 的 aGVHD 主要发生于皮肤,例 1、例 2、例 6 的 aGVHD 主要发生于肠道,5 例患儿经糖皮质激素联合免疫抑制剂的 aGVHD 治疗方案治疗后均可缓解,余 2 例患儿在随访期内未发生 aGVHD。移植后+100d 内定期监测患儿 CMV-DNA、EBV-PCR、HSV-I 型 IgM 抗体、HSV-II 型 IgM 抗体检测结果,仅 1 例(例 7)于移植后+46d 出现 CMV-DNA 阳性(8.09×104),经更昔洛韦抗感染治疗后好转,余患儿均未见阳性检测结果。
2.4 随访
随访截至 2025 年 6 月 30 日,所有患儿移植+90d 复查骨髓 MRD 均为阴性。5 例患儿持续 CR 并存活,2 例(例 2、4)因复发死亡。中位随访时间 1008(371~1814)d。预期 3 年 OS 率为 71%。
例 2 患儿于移植后+120d 复查骨髓白血病融合基因 MLL::AF10 基因定量 0.03%,考虑分子学复发,予环孢素减量,+130d 回输供者冻存外周血干细胞 6.5 mL( 细胞数 1×107/kg),+157d 复查骨髓白血病融合基因 MLL::AF10 基因定量转阴,+167d 开始予地西他滨(10 mg/m2),1 次/周,共 13 次。+272d 患儿无明显诱因出现发热,外周血白细胞计数 48.42×109/L 且可见幼稚细胞。进一步骨髓细胞学检查可见 77% 原始细胞,流式 MRD 检测可见 61% 异常细胞,MLL::AF10 基因定量 5.48%,考虑骨髓细胞学复发,患儿家属放弃治疗后死亡。
例 4 患儿于移植后+233d 复查骨髓 CBFA2T3::GLIS2 基因 0.017%,考虑分子学复发,于+239d 回输供者淋巴细胞;+274d 复查骨髓 CBFA2T3::GLIS2 基因 0.097%,+281d 加用维奈克拉抗肿瘤治疗,+317d 骨髓 CBFA2T3::GLIS2 基因 0.158%,考虑患儿病情进展。于+324d 起行预激方案 [9],予地西他滨 5 mg/m2×1d 后因患儿对地西他滨不能耐受,改为阿扎胞苷 75 mg/m2×4d。+356d 患儿无明显诱因出现发热伴右肩部新发肿物,行右肩部肿物手术切除及病理活检,提示肿物为 MS,考虑髓外复发。家属放弃治疗并出院后死亡。
3 讨论
MS 可发生于人体任何部位,孤立性 MS 易误诊为恶性淋巴增生性疾病 [10-11],光镜下 MS 可被误诊为非霍奇金淋巴瘤或其他实体肿瘤,有报道 MS 误诊率达 75%[12],即使及时诊断并接受经典化疗及 HSCT 治疗后其预后也并不理想,1 年及 3 年 OS 分别为 71.4% 和 64.3%[13]。
儿童 MS 占 AML 患儿比例在各中心报道差异较大(0%~5.7%),提示儿童 MS 诊断较困难且诊断标准存在差异 [14]。本中心儿童 MS 在 AML 占比为 7.9%(7/88)。目前认为白血病患儿出现来源不明实性肿块,特别是多发病灶,无论发生在什么部位,均应首先考虑 MS 可能性 [10]。本研究的 7 例 MS 患儿中有 4 例为头面部受累为主,2 例纵隔受累为主,1 例髂骨受累为主,与既往报道儿童 MS 浸润部位类似 [15]。PET/CT 在评估髓外浸润性肿瘤及疗效方面或有一定优势 [11]。
取得肿瘤组织并进行病理检查是确诊 MS 的「金标准」,但在无法进行活检的患者中,可通过骨髓或外周血等其他组织的形态学和流式细胞术分析,以及与细胞遗传学和分子数据的结合,明确诊断 [5]。本研究中例 6 因发热伴眼眶肿胀、血常规结果异常就诊,骨髓细胞学考虑急性粒单核细胞白血病伴嗜酸性粒细胞增多,骨髓免疫分型可见髓系幼稚细胞增多(61.4%),融合基因提示 WT1 阳性,骨髓染色体核型发现 16 号染色体臂间倒位;眼眶 MRI 结果示左眼部及颞部软组织增厚肿胀(87 mm×69 mm×99 mm),考虑血液系统疾病所致。综合该患儿相关辅检诊断符合 MS。例 7 因发现面部肿块就诊。肿块部位增强 CT 检查示扫描所见皮下组织及颌面骨、颅骨多处异常改变,考虑疾病浸润所致,结合该患儿 MICM 结果可临床诊断 MS。
目前仍推荐 MS 需接受常规多药联合强化疗的 AML 方案治疗。本研究 7 例患者均接受 CCLG-AML-2019 方案化疗,且 3 年 OS 优于既往报道 [16]。这可能得益于目前儿童 AML 方案将 MS 列为高危因素,并推荐尽早桥接 allo-HSCT 治疗 [17]。
MS 对放射线较为敏感,局部病灶接受放射治疗可以提高临床疗效并降低复发率 [6,18]。本中心复发率较既往研究低,也可能获益于积极辅以放疗干预,能在化疗基础上进一步清除残留肿瘤病灶。
既往研究发现 MS 合并 FLT3-ITD/RUNX1/ASXL1/TP53 突变预后较差 [19]。近期人源化抗 CD33 单克隆抗体及以与 MS 相关的 BCR-ABL1、FLT3-ITD 和 FIP1L1-PGFRA 突变为靶点的酪氨酸激酶抑制剂治疗 MS 患者已取得良好效果 [20],或可积极应用于儿童 MS 患者。本研究中有 2 例患儿死亡,例 2 及例 4 患儿起病年龄分别为 10 月龄、2 岁 5 个月,均较中位起病年龄年幼,提示低龄可能与 MS 患儿预后不良相关。限于本研究样本数较少,此推论有待多中心研究进一步验证。
综上所述,儿童 MS 临床表现无明显特异性,特别是孤立性 MS 仍易误诊,需结合骨髓 MICM、局部病理活检及全身影像学等综合诊断。接受儿童 AML 高危组化疗方案并积极桥接 allo-HSCT 可使儿童 MS 生存获益。如有条件可在移植前接受全身或局部放疗,但仍有待进一步开展大样本多中心临床研究以优化目前的治疗策略。
好文章,需要你的鼓励















