来源:雨露肝霖
目前,临床治愈是慢乙肝治疗最理想的治疗终点,并且大量研究显示以聚乙二醇干扰素α(PEG IFNα)为基础的抗病毒治疗策略是实现临床治愈的最佳选择。随着研究的不断深入,对于低病毒血症(LLV)患者、慢乙肝儿童、HBV 相关肝硬化/肝癌患者及 HBV-HIV 合并感染者等特殊人群的治疗探索和研究也逐渐丰富。
近期,空军军医大学唐都医院康文教授和连建奇教授团队在 Drug Design, Development and Therapy 上发表的一篇最新综述详细总结了慢乙肝特殊人群经 PEG IFNα治疗实现临床治愈的现状、趋势和挑战,肝霖君与您分享部分重要内容。

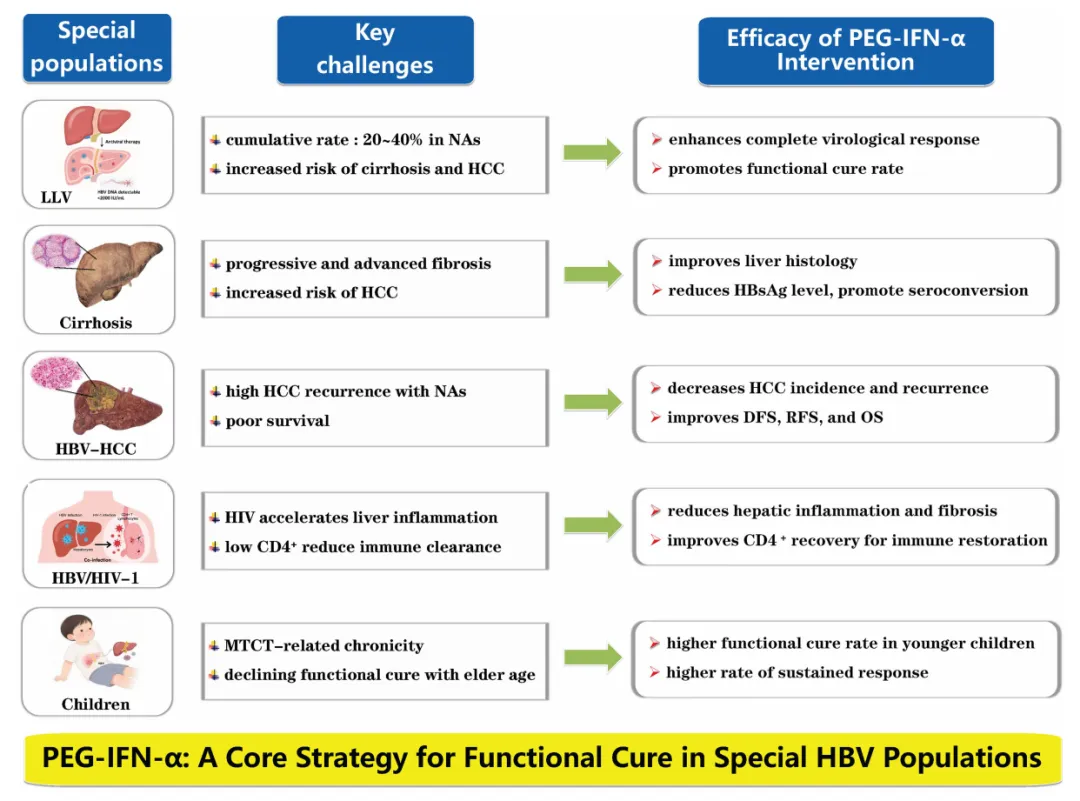
一、部分病毒学应答或低病毒血症患者
01 流行病学
即使使用一线 NAs 治疗,仍有约 20 - 40% 的慢乙肝患者出现 LLV。
02 临床危害
LLV 患者肝脏炎症和肝纤维化发生率较高:76.2% 的患者肝脏炎症处于 G2 - G4,61.1% 的患者肝纤维化处于 F2 - F4。
LLV 是终末期肝病进展的独立危险因素。持续的 LLV 会促进治疗期间肝纤维化的进展,并与 HBV 相关肝癌患者的总生存期(OS)较差及肿瘤复发相关。LLV 还会损害 HBV 相关不可切除肝癌患者接受免疫检查点抑制剂治疗的疗效。
03 治疗进展
长期抗病毒治疗对于伴有 LLV 的代偿期乙肝肝硬化患者仍然有益,可显著降低肝癌年发生率。此外,有效的抗病毒治疗也可降低伴有 LLV 的 HBV 相关肝癌患者的死亡率。因此,必须考虑调整 LLV 患者的治疗方案以实现完全病毒学应答(CVR)。
肝内 HBV 储存库和 HBV DNA 整合是慢乙肝患者出现 LLV 的主要原因。在获得 HBsAg 清除、肝内 HBsAg 转阴的患者中,PEG IFNα可强效抑制整合 HBV DNA 和 cccDNA 的转录活性。因此,《中国慢性乙型肝炎防治指南(2022 年版)》也推荐 LLV 或应答不佳的患者可联合 PEG IFNα治疗。
一项研究纳入 81 例经 NAs 治疗产生部分病毒学应答的 HBeAg 阳性慢乙肝患者,换用 PEG IFNα治疗 19.6 个月后,38.3% 的患者获得 HBeAg 血清学转换,8.6% 获得 HBsAg 清除或血清学转换。
一项回顾性研究纳入 97 例 LLV 患者,分为 NAs 单药治疗组、NAs 联合治疗组和 NAs + PEG IFNα联合治疗组。治疗 96 周后,NAs 联合治疗组和 NAs + PEG IFNα联合治疗组的 CVR 率分别为 89.4% 和 87.5%,均高于 NAs 单药治疗组(55.9%)。
一项前瞻性研究纳入 240 例经 NAs 治疗出现 LLV 的 HBeAg 阴性慢乙肝患者,分为 PEG IFNα加用组和 NAs 加用组。治疗 48 周,PEG IFNα加用组的 CVR 率和 HBsAg 清除/血清学转换率均高于 NAs 加用组(97.5% vs. 85.9%;30.9% vs. 5.1%)。
中国降低乙肝患者肝癌发生率研究(绿洲)工程项目的亚组分析纳入 1640 例 LLV 患者。结果显示,与继续使用原 NAs 或换用其他 NAs 相比,换用或加用 PEG IFNα治疗 48 周的 HBsAg 血清学转换率显著更高(15.8% vs. 3.4%)。
综上,基于 PEG IFNα的治疗方案对于部分病毒学应答或 LLV 患者在实现 CVR 和临床治愈方面具有显著优势。
二、肝纤维化或代偿期肝硬化患者
失代偿期肝硬化是 PEG IFNα的绝对禁忌症,而乙肝肝纤维化及代偿期肝硬化患者可使用 PEG IFNα治疗。
PEG IFNα-2b 治疗可改善 HBeAg 阳性慢乙肝患者的肝组织学,肝脏坏死炎症评分和纤维化评分均显著降低。
在接受 PEG IFNα-2b 治疗的 HBeAg 阳性慢乙肝患者中,相比于无进展期肝纤维化的患者,进展期肝纤维化患者的病毒学应答率(HBeAg 血清学转换且 HBV DNA < 10,000 copies/mL;25% vs. 12%)及纤维化逆转率(66% vs. 26%)均更高。
一项研究将 218 名 Ishak 纤维化评分为 2 - 4 分的初治慢乙肝患者随机分配至 ETV 单药治疗组或 ETV + PEG IFNα联合治疗组。两组在治疗 78 周后的纤维化逆转率相似(68% vs. 56%),但联合治疗组的 HBeAg 和 HBsAg 清除/血清学转换率更高。
一项观察性研究纳入 54 名代偿期乙肝肝硬化患者,接受 48 周 PEG IFNα-2b 治疗后 HBsAg 水平显著降低,其中 3 例患者获得 HBsAg 清除,2 例获得 HBsAg 血清学转换。此外,观察期内无患者发生急性肝功能失代偿或进展为终末期肝病。
由于 PEG IFNα治疗可带来较高的停药后持续应答率,因此,对于乙肝肝纤维化或代偿期肝硬化患者,应考虑采用 PEG IFNα治疗,以期实现肝纤维化逆转及 HBsAg 清除。
三、HBV 相关肝癌防治
01 HBV 相关肝癌的流行病学
慢性 HBV 感染者发生肝癌的相对风险较非感染者高 14 - 223 倍,HBV 相关肝硬化患者的肝癌发生风险显著升高。
中国 HBV 相关肝癌发病数占全球总数的 69%,约 25 万例。基于马尔可夫模型的预测显示,2006 - 2030 年中国 HBV 感染者的肝癌年发病数呈上升趋势。
02 不同抗病毒治疗下的肝癌发生风险
抗病毒治疗对于降低 HBV 相关肝癌的发生和复发风险至关重要。
接受 NAs 治疗的慢乙肝患者仍面临较高的肝癌发生风险:获得病毒学应答的患者 5 年肝癌累积发生率为 11.4%,而未获得病毒学应答的患者高达 18.8%;ETV 与 TDF 预防效果相当,但 5 年肝癌累积发生率仍达 7% 左右。这其中的部分原因是,即使经过 10 年的治疗,NAs 也仅能小幅下调 HBV 整合频率和肝细胞克隆大小。
PEG IFNα不仅可通过激活自然杀伤细胞功能,恢复病毒特异性 CD8+ T 细胞应答以清除受感染的肝细胞,还能强效抑制整合 HBV DNA 与 cccDNA 的转录活性,因而较 NAs 可更有效降低肝癌发生率。
PARADISE 研究的中期分析显示,对于具有肝癌中高风险的慢乙肝患者,NAs + PEG IFNα-2b 治疗组的 2 年肝癌累积发生率为 0%。
与 ETV 治疗相比,无论 PSM 前后,接受 PEG IFNα治疗的慢乙肝患者 5 年肝癌累积发生率均为 0%。
(PEG) IFNα治疗组 10 年肝癌累积发生率显著低于 NAs 组(2.7% vs. 8.0%)。
(PEG) IFNα治疗组 10 年不良结局(失代偿期肝硬化、肝衰竭、肝癌、肝移植和死亡)累积发生率显著低于 NAs 组(1.1% vs. 11.9%)。
一项荟萃分析指出,HBsAg 清除后的合并肝癌发生率为 1.88%,而在无肝硬化的患者中,肝癌发生率降至 0.76%。
03 HBV 相关肝癌患者的术后辅助治疗策略
(PEG) IFNα可作为 HBV 相关肝癌患者在无禁忌症情况下的一种治疗选择。
(PEG) IFNα治疗在 HBV 相关肝癌患者中耐受性良好。基于 (PEG) IFNα的辅助治疗可有效降低患者肝癌术后(切除、消融或 TACE)的复发率,提高无病生存期(DFS)、无复发生存期(RFS)和 OS。
四、HBV/HIV-1 合并感染者
01 流行病学
HBV 和人类免疫缺陷病毒-1(HIV-1)都是血源性病毒,具有相似的传播途径。在全球 HIV 感染者中,HBV 感染率为 8.4 - 11.1%,其中 26.8% 为 HBeAg 阳性。一项基于 2010 - 2011 年中国国家免费抗病毒治疗计划数据的全国回顾性队列研究显示,8.7% 的参与者为 HBV/HIV-1 合并感染。
02 HBV 与 HIV-1 的相互作用及临床危害
HBV 和 HIV-1 之间存在复杂的相互作用,影响着合并感染者的临床结局。
慢性 HBV 感染与 HIV-1 感染者进展为获得性免疫缺陷综合征(AIDS)或死亡的风险增加相关。HIV-1 RNA 和 HIV-1 p24 抗原可在肝实质细胞和非实质细胞中检测到,且 HIV-1 DNA 在接受高效抗逆转录病毒治疗(HAART)的 HBV/HIV-1 合并感染者的肝细胞中持续存在。
在 HBV/HIV-1 合并感染的情况下,HIV-1 不仅通过微生物易位(脂多糖和可溶性 CD14 水平升高)和趋化因子诱导的活化 T 细胞向肝脏募集来促进肝脏炎症,还通过肝星状细胞中缺氧诱导因子-1α(HIF-1α)和转化生长因子-β1(TGF-β1)之间的正反馈加剧 HBV 诱导的肝纤维化。与单纯慢性 HBV 感染相比,HBV/HIV-1 合并感染者进展为肝硬化、肝衰竭和肝癌的风险更高。
03 治疗进展
HBV/HIV-1 合并感染者应同时治疗 2 种病毒,包括 2 种抗 HBV 活性的药物,以避免产生 NAs 耐药。
目前,PEG IFNα也已用于 HBV/HIV-1 合并感染的治疗:
一例 HBV/HCV/HDV/HIV-1 合并感染患者接受 24 周的 PEG IFNα +利巴韦林治疗,实现 HBsAg 血清学转换、HBV DNA 和 HDV RNA 转阴。
在一项 I 期临床试验中,10 例 HBV/HIV-1 合并感染者接受基于 PEG IFNα的治疗,大多数患者在治疗后 HBV DNA 下降,肝脏坏死炎症和纤维化评分改善。
正在接受 HAART 治疗的 HBV/HIV-1 合并感染者加用 48 周 PEG IFNα,可使 20% 的患者获得 HBeAg 清除,但未显著提高 HBeAg 血清学转换率或 HBsAg 清除率。
对于正在进行 HAART 治疗、获得病毒学应答(HIV-1 RNA 和 HBV DNA 阴性)、CD4+ T 细胞计数高水平(> 350 cells/mm3)且 HBsAg 低水平(< 1500 IU/mL)的 HBV/HIV-1 合并感染者,采用个体化的 PEG IFNα治疗可能更合适,且更有可能实现乙肝临床治愈。
五、慢乙肝儿童
01 流行病学
全球有超 630 万 5 岁以下儿童携带 HBV,5 岁以下儿童的 HBsAg 流行率为 0.9%。从 1990 年到 2021 年,全球儿童和青少年的 HBV 年龄标准化发病率有所下降。中国 1 - 4 岁儿童的 HBsAg 流行率已从 1992 年的 9.67% 显著下降至 2020 年的 0.30%。
02 治疗策略
慢性 HBV 感染儿童的治疗策略应基于 HBV DNA、ALT、HBsAg 和 HBeAg 水平、影像学检查或肝活检显示的肝脏炎症/纤维化情况进行综合评估。对于慢乙肝或有进展期肝病的儿童,无论 HBeAg 状态如何,都应立即启动抗病毒治疗。
开始抗病毒治疗的年龄是慢乙肝儿童实现临床治愈最关键的因素之一。1 - 3 岁患儿的 HBsAg 清除率超 60%,3 - 7 岁患儿为 40%。因此,应尽早对慢乙肝儿童实施干预,以期实现临床治愈。
目前,IFNα已被推荐用于 ≥ 1 岁的儿童,而 PEG IFNα被推荐用于 ≥ 3 岁的儿童。
平均 21 周的 IFNα治疗可使 22.2% 的慢乙肝患儿实现 HBsAg 清除和血清学转换。
2 - 16 岁的慢乙肝儿童接受 52 周的 PEG IFNα单药治疗,HBsAg 清除率可达 48.1%,HBsAg 血清学转换率达 47.1%,且超 90% 获得 HBsAg 清除的儿童在 104 周的随访期内持续应答。
一项荟萃分析表明,相比于 IFNα单药治疗,IFNα联合 NAs 治疗在病毒学抑制和血清学应答方面更有效。
处于免疫耐受期或不确定期的慢乙肝儿童接受 (PEG) IFNα治疗也能获得较高的 HBsAg 清除率:
高病毒载量且 ALT 正常或轻度升高的慢乙肝儿童接受以 IFNα为基础的治疗,36 个月的累积 HBsAg 清除率可达 56.3%。
「萌芽」项目的中期数据显示,在 HBeAg 阳性、ALT 正常的儿童和青少年中,接受 24 个月的 PEG IFNα治疗后,总体 HBsAg 清除率达 48.2%。
综上,对于 HBV DNA 阳性的慢乙肝儿童,应尽早启动抗病毒治疗(年龄 ≥ 1 岁可使用 IFNα,年龄 ≥ 3 岁可使用 PEG IFNα),以尽可能实现临床治愈。
六、PEG IFNα治疗的挑战及待解决的问题
基于 PEG IFNα的治疗可助力慢乙肝患者实现临床治愈,但其应用受到副作用和患者依从性的限制。通常情况下,常见副作用通过密切监测和积极管理可得以控制,严重不良事件较为罕见。而依从性障碍则可通过加强患者教育、提供支持性护理及优化医疗系统得以改善。在临床实践中,采取兼顾疗效、安全性与依从性的综合策略,对于优化 PEG IFNα的治疗至关重要。
目前 PEG IFNα发挥疗效的深层机制尚未完全阐明,主要由于现有临床数据与研究设计的局限性,特别是人群相关因素(如种族、宿主遗传变异)及特定地理区域中病毒基因型所起的作用尚不明确。通过开展多民族、基于遗传信息及基因型的分层研究来解决上述空白,不仅能加深对机制的理解,还能实现精准的、个性化的治疗策略。
总结
总体而言,PEG IFNα在慢乙肝特殊人群中的疗效和安全性良好,为临床治愈奠定了基础,并支撑 HBV 感染者管理的临床决策。PEG IFNα是慢乙肝特殊人群临床治愈的基石药物,同时,仍需具有协同潜力的新疗法来克服当前的局限性。将 PEG IFNα与 siRNA、Toll 样受体激动剂和反义寡核苷酸等新药相结合,或可靶向 HBV 的多个生命周期,解决尚未被满足的临床需求,有望距离实现 2030 年消除乙肝的目标更近一步。
参考文献:
Zhang Y, Li Y, Lian JQ, et al. Pegylated Interferon-α-Induced Functional Cure for Special Populations with Chronic Hepatitis B Virus Infection: Current Trends, Challenges and Prospection[J]. Drug Des Devel Ther, 2025, 19: 10411-10422.
好文章,需要你的鼓励
















