


AASLD2025 丨侯金林/李咏茵/唐利波教授团队:干扰素α通过「单核细胞-Tfh-B 细胞轴」增强 B 细胞应答,促进临床治愈
来源:雨露肝霖
编者按
2025 年第 76 届美国肝病研究协会(AASLD)年会于 11 月 7 - 11 日在美国华盛顿举行,肝霖君与您分享相关重要内容。
既往南方医科大学南方医院的侯金林教授、李咏茵教授和唐利波教授团队曾发表一项关于 B 细胞在干扰素α(IFNα)治疗期间的作用研究,结果表明 IFNα治疗增强 HBV 特异性 CD8+ T 细胞应答的潜在机制在于 PEG IFNα通过 B 细胞的抗原呈递和共刺激功能增强 B 细胞与 T 细胞的连接。近期,该团队再次在 AASLD 2025 摘要上发表最新研究结果,证实 IFNα通过「单核细胞-Tfh-B 细胞轴」增强 B 细胞应答,促进乙肝临床治愈。

研究背景
临床治愈是目前乙肝治疗的重要目标。前期的临床试验表明,与小干扰 RNA(siRNA)单药治疗相比,siRNA 与聚乙二醇干扰素α(Peg-IFNα)联合治疗可实现更高的临床治愈率。这一发现证实了 IFNα在介导临床治愈中的重要作用,然而,其潜在的免疫机制,特别是 IFNα促进抗病毒体液免疫的机制仍不清楚。因此,本研究旨在探究 IFNα调节 B 细胞免疫应答、促进临床治愈的免疫机制。
研究方法
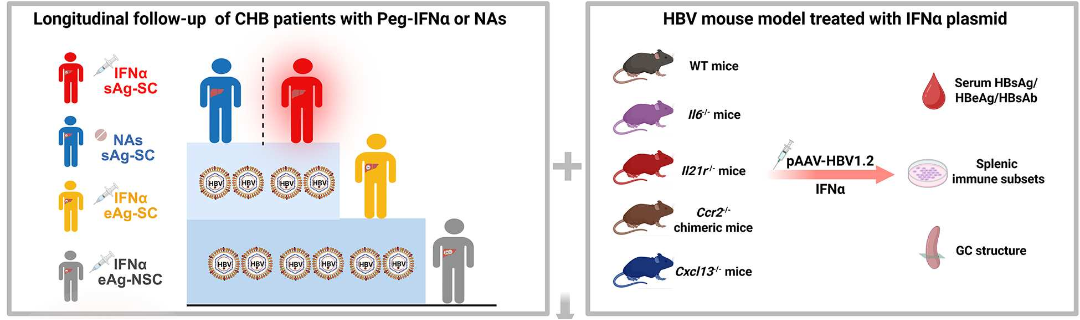
本研究对接受 Peg-IFNα治疗的慢乙肝患者展开了纵向随访,根据第 72 周时的病毒学转归结果进行分组:未 HBeAg 血清学转换组(HBeAg-NSC 组, n = 11)、HBeAg 血清学转换组(HBeAg-SC 组, n = 7)以及 HBsAg 血清学转换组(HBsAg-SC 组, n = 6);此外,还纳入 3 例经核苷(酸)类似物(NAs)治疗 5 年实现 HBsAg 血清学转换的慢乙肝患者作为对照组(NAs-HBsAg-SC 组)。
在基线和第 12 周时采集外周血用于单细胞 RNA 测序和流式细胞术分析。为进一步研究 IFNα对免疫细胞亚群和 HBV 特异性 B 细胞应答的影响,还做了体外细胞因子刺激试验,并在经 IFNα质粒处理的 II6−/−、II21r−/−、Ccr2−/−嵌合体和 Cxcl13−/− HBV 小鼠模型中进行体内验证。
研究结果
该研究证实临床治愈的核心通路为:IFNα → 单核细胞 → IL-6 → Tfh 细胞 → IL-21 → B 细胞:
IFNα激活单核细胞,使其大量分泌 IL-6。scRNA-seq 与体外实验证实,IFNα刺激后,单核细胞的 IL-6 相关基因程序显著上调,并成为 IL-6 的主要细胞来源。
IL-6 进而作用于滤泡辅助 T 细胞 (Tfh), 促使其高表达并分泌 IL-21。在获得 HBsAg 血清学转换的患者体内,发现 IL-6 塑造了 IL6ST-high Tfh 细胞亚群;体外实验证明 IL-6 可诱导 Tfh 细胞产生 IL-21,此效应在 IL-6 基因敲除 (II6−/−) 小鼠中未观察到。
IL-21 是 B 细胞的强效激活因子,驱动 B 细胞分化为浆细胞并形成生发中心,最终产生高水平的 HBsAg 特异性抗体,实现 HBsAg 清除和病毒抑制。
对 B 细胞的转录组分析显示,IL-21 刺激能显著富集体液免疫反应通路;scRNA-seq 进一步揭示,在临床治愈患者体内 Tfh 与 B 细胞间的 IL-21-IL21R 信号最为活跃;空间分析证实 IFNα通过 CXCL13-CXCR5 轴促进生发中心形成,而该过程在 IL-21 受体缺陷(II21r−/−)及 Cxcl13−/−小鼠中均无法实现。
研究结论
该研究表明 IFNα通过「单核细胞-Tfh-B 细胞轴」促进抗 HBV 的体液免疫,桥接先天免疫和适应性免疫,从而助力乙肝临床治愈,为优化基于 IFNα的治疗策略提供了免疫机制相关的循证证据。
参考文献:
Li Y, Zhong S, Zhou Y, et al. Interferon-α enhances HBsAg-specific B cell responses via monocyte Tfh-B cell axis to facilitate functional cure of hepatitis B. AASLD2025, Abstract (1132).
好文章,需要你的鼓励













