来源:《临床儿科杂志》
石小松, 傅世杰, 何小花, 吕辉, 陈厚杨, 陈茂琳, 陈捷. 福建省两地区百日咳鲍特菌抗原基因型特征及耐药性分析 [J]. 临床儿科杂志, 2025, 43(8): 575-582 DOI:10. 12372/jcp.2025.25e0425
SHI Xiaosong, FU Shijie, HE Xiaohua, LYU Hui, CHEN Houyang, CHEN Maolin, CHEN Jie. Antigenic genotypic characteristics and antibiotic resistance analysis of Bordetella pertussis in two regions of Fujian province[J]. Journal of Clinical Pediatrics, 2025, 43(8): 575-582 DOI:10.12372/jcp.2025.25e0425
本文作者:石小松 1 傅世杰 2 何小花 1 吕 辉 3 陈厚杨 2 陈茂琳 4 陈 捷 1
作者单位:1. 福州大学附属省立医院 福建医科大学省立临床医学院儿科(福建福州 350001);2. 三明市尤溪县总医院儿科(福建尤溪 365100);3. 福州大学附属省立医院 福建医科大学省立临床医学院检验科(福建福州 350001);4. 三明市尤溪县总医院检验科(福建尤溪 365100)
摘要:目的 分析中国福建省福州市及尤溪县百日咳鲍特菌(BP)抗原基因多态性特征与耐药表型,为优化疫苗策略和抗菌药物使用提供科学依据。方法 于 2024 年收集两地区 336 份百日咳临床疑似病例的咽拭子标本,经细菌培养、分离与鉴定后,对 7 个抗原基因(ptxP、ptxA、ptxC、prn、fim3、fim2、tcfA)以及 23S rRNA A2047 位点进行分析,以确定其多态性和变异情况。基于核心基因组单核苷酸多态性(cgSNPs)构建最大似然法系统发育树。采用 E-test 法检测大环内酯类、磺胺类及β-内酰胺类最低抑菌浓度(MIC)。结果 336 份疑似病例咽拭子标本中成功分离出 29 株 BP 临床株(8.6%,29/336),抗原基因谱分析显示,主要流行型别为 ptxP3/prn2/ptxC1/ptxA1/fim2-1/fim3-1/tcfA2(55.2%,16/29),ptxP3/prn2/ptxA1 型菌株比例达 72.4%(21/29),检出 prn150 突变株 4 株(13.8%)。系统发育分析表明,疫苗株 CS 形成了独立的进化分支(A 簇),2024 年福建分离株与 2020 年前国内菌株存在显著遗传差异,形成 B(ptxP3/prn2/ptxA1,含多数福建株)和 C(ptxP1/prn1/ptxA1,含既往分离株)两大进化簇。所有分离株均检测到 23S rRNA A2047 G 突变,对大环内酯类药物的 MIC>90 mg/L,呈现高度耐药;复方磺胺甲噁唑(TMP-SMX)的 MIC 为 0.005~0.45 mg/L;β-内酰胺类(头孢曲松、头孢噻肟、头孢哌酮/舒巴坦)的 MIC 为 0.004~0.64 mg/L。结论 福建地区 BP 流行株呈现独特的抗原基因进化特征且存在普遍的大环内酯类耐药现象。后续需强化基于分子分型的疫苗组分监测,并结合药敏结果精准优化抗菌治疗方案。
关键词: 百日咳; 百日咳鲍特菌; 抗原基因型; 全基因组测序; 大环内酯类耐药; 儿童
百日咳鲍特菌(Bordetella pertussis,BP)引起的「百日咳再现」已成为全球公共卫生领域的重大挑战 [1]。尽管百日咳疫苗的广泛接种显著降低了疾病负担,但自 20 世纪 80 年代以来,全球百日咳流行病学特征发生显著转变,呈现婴幼儿发病率反弹与青少年、成人病例激增的趋势 [2]。我国自 2015 年后,百日咳发病亦呈现上升趋势 [3],2024 年全国报告病例数较 2023 年增长约 1197%[4],作为东南沿海人口密集省份,福建省 4 年内病例数增长高达 2033%[5]。这一现象主要与 BP 抗原基因变异、疫苗免疫保护期缩短、耐药菌株扩散、检测与诊断能力的提升及 COVID-19 后易感人群的积累密切相关 [6]。现有研究已初步揭示部分区域 BP 菌株的分子流行病学特征 [7-9],但由于不同地区在气候条件、人口结构及疫苗接种策略等方面存在显著差异,病原体的传播模式与基因型演化路径亦有所不同。福建省因地处亚热带,气候湿润且人口流动性高,其独特的地理与人口特征可能加速病原体传播与基因型演化。然而,福建地区的 BP 基因型分布及耐药特征尚未有系统性研究。本研究拟通过分析福建省福州与尤溪两地区 BP 临床分离株的抗原基因型及耐药特征,旨在初步了解福建省部分地区 BP 菌株的分子生物学特性,为深入探究区域性病原变异规律、优化百日咳防控策略提供数据支撑。
1 对象与方法
1.1 研究对象
本研究以 2024 年 1 月至 12 月,福建省立医院及尤溪县总医院收治的百日咳临床疑似病例为研究对象。纳入标准 :①符合《中国百日咳诊疗与预防指南(2024 版)》[10] 疑似病例诊断标准,即具有百日咳典型临床表现之一;②年龄 ≤ 14 岁;③签署知情同意书。排除标准:①因严重并发症而无法配合研究;②样本质量不合格(如细菌培养失败或 DNA 提取失败)。针对所有疑似百日咳的病例,采集了两份鼻咽拭子样本。其中一份样本通过实时荧光定量聚合酶链式反应(PCR)检测,用于验证是否存在 BP 感染。另一份标本立即接种于含头孢氨苄(40 μg/mL)的改良木炭琼脂培养基(广东环凯微生物科技有限公司,C27500B1),并在 37℃ 有氧条件下培养 7 天,每日观察菌落生长情况;若 7 天内无典型 BP 菌落出现,则判定为培养阴性。获得纯培养物后,采用多重 PCR 方法检测 IS481、IS1001 和 IS1002 基因,其中 IS481 和 IS1001 为 BP 特异性基因,而 IS1002 用于鉴别其他鲍特菌种 [11]。经鉴定确定为 BP 的阳性分离株保存于-80℃ 超低温冰箱建立菌种库。
1.2 菌株基因序列组装与抗原基因型分析
将所有培养阳性的 BP 临床分离株复苏后,采用 Magen HiPure Bacterial DNA Kit(D3191-02)提取基因组 DNA,质控后将符合质量标准的 DNA 样品,使用 Illumina HiSeq 4000 系统构建双端测序文库(insert size 350 bp,Nextera XT 制备试剂盒),联合 Oxford Nanopore MinION 平台(R9.4.1 flow cell)实施混合测序策略以提升组装连续性。原始数据经 SOAPnuke(v1.5.6)质控,采用 SPAdes(v3.9.1)进行混合组装,QUAST(v5.0.2)以 Tohama I(NC_002929.2)为参考基因组评估组装质量(N50、contig 数等指标)。基于已报道的多态性位点 [12],使用 Primer Premier 5.0 软件设计引物,用于扩增 BP 中编码百日咳毒素(PT)和黏附素(PRN)等 7 个主要抗原蛋白的相关基因(包括 ptxP、ptxA、ptxC、prn、fim3、fim2 及 tcfA)和 23S rRNA 基因,通过梯度 PCR 优化过程,对扩增产物进行测序。利用 BLAST 在线工具( http://www.ncbi.nlm.nih.gov/blast/Blast.cgi )与 GenBank 数据库中的标准等位基因序列进行比对分析,以确定各毒力抗原的等位基因型。同时,重点检测 23S rRNA 基因 A2047 位点是否存在 G 碱基突变。
1.3 系统发育分析
整合国内多中心 BP 菌株及中国百日咳疫苗株 CS(CP086368.1),基于 Snippy 4.6.0 进行全基因组比对。采用核心基因组单核苷酸多态性(core genome single nucleotide polymorphisms,cgSNPs)筛选策略,设定保守位点保留阈值为 ≥ 95%,并利用 FastTree 2.1.11 软件构建最大似然法系统发育树,并运用 tvBOT[13] 实现拓扑结构可视化。参考基因组集包含国际标准株 Tohama I(NC_002929.2)、中国疫苗株 CS(CP086368.1)及 NCBI RefSeq 数据库收录的国内部分地区 BP 菌株基因组序列。
1.4 抗菌药物敏感性分析
采用标准化的药敏检测流程,将复苏后的 BP 临床分离株及质控菌株(流感嗜血杆菌 ATCC 49247、金黄色葡萄球菌 ATCC 29213)传代培养一次后制备成 0.5 McFarland 标准菌悬液(生物梅里埃公司),分别接种至特异性培养基 :BP 菌株选用含 1% 酪蛋白水解物的百日咳专用培养基(Oxoid 公司),质控菌株分别接种嗜血杆菌巧克力琼脂(BD 公司)及含 10% 脱纤维羊血的 MH 琼脂(科玛嘉生物)。使用 E-test 梯度扩散法(Liofilchem ETEST-032048)检测 BP 对红霉素、阿奇霉素、克拉霉素、复方磺胺甲噁唑(trimethoprim-sulfamethoxazole, TMP-SMX)、头孢曲松、头孢噻肟、头孢哌酮/舒巴坦 2∶1 共 7 种抗菌药物敏感性。试条贴附后平板分别置于 37℃ 有氧环境(BP 和金黄色葡萄球菌)或 5% CO2 环境(流感嗜血杆菌)中培养 72 小时。为确保实验结果的客观性和一致性,所有培养平板在接种前均被赋予唯一的匿名编号,并由一名不参与后续实验操作的研究人员进行独立编码。培养结束后,至少两名未参与菌株处理的研究人员在不知晓样本身份的前提下,独立读取并记录各平板的最低抑菌浓度(minimal inhibitory concentration,MIC),最终结果经交叉核对后录入。参考既往研究数据 [14](大环内酯类 MIC ≥ 32 mg/L 判定耐药)及 CLSI M100-Ed33(2023)指南 [15](β-内酰胺类及磺胺类参考流感嗜血杆菌标准),对药敏结果进行解释。同时通过金黄色葡萄球菌 ATCC 29213 的β-内酰胺酶活性检测(Nitrocefin 法)评估实验体系的稳定性与检验方法的可靠性。
2 结果
2.1 一般情况
本研究共采集百日咳临床疑似病例鼻咽拭子样本 336 份,其中 229 份经实时荧光定量 PCR 检测为 BP 核酸阳性,阳性率为 68.2%(229/336)。培养得到 29 株临床分离株,阳性率为 8.6%(29/336)。病例分布显示,福州市来源病例占 69.0%(20/29),尤溪县来源病例占 31.0%(9/29),菌株编号为 Fujian_1 至 Fujian_29。其中男性 16 例(55.2%),女性 13 例(44.8%)。年龄范围 2 个月至 10 岁 2 个月,中位年龄为 80(15~96)个月。2024 年各季度均有一定数量的阳性病例检出,检出数分别为 8 例、9 例、4 例和 8 例。疫苗接种史分析表明,72.4%(21/29)的病例已完成 4 剂次百白破疫苗全程接种,未接种者为 1 例未达首剂接种月龄的婴儿(2 月龄,3.4%)。
2.2 抗原基因型分析与 23S rRNA 基因位点检测
29 株 BP 临床分离株的 7 种毒力相关抗原基因(ptxP、ptxA、ptxC、prn、fim3、fim2、tcfA)进行系统分型,共发现 5 种基因型组合,主要流行基因型为 ptxP3/prn2/ptxC1/ptxA1/fim2-1/fim3-1/tcfA2(55.2%,16/29),其次为 ptxP3/prn2/ptxC2/ptxA1/fim2-1/fim3-1/tcfA2(17.2%,5/29)及 ptxP1/prn1/ptxC1/ptxA1/fim2-1/fim3-1/tcfA2(13.8%,4/29)。值得注意的是,4 株菌株(13.8%,4/29)携带新发现的 prn150 等位基因型(表 1)。基因多态性分析显示:ptxP 基因呈现 ptxP1(13.8%,4/29)与 ptxP3(86.2%,25/29)双态分布;prn 基因存在 prn1(13.8%,4/29)、prn2(72.4%,21/ 29)及 prn150(13.8%,4/29)三态分型;而 ptxA 基因全部表现为 ptxA1 单一表型(100%,29/29),未发现其他等位基因型。所有分离株(100%,29/29)在 23S rRNA 基因 A2047 G 位点(Escherichia coli 编号)均检测到 G 碱基突变。
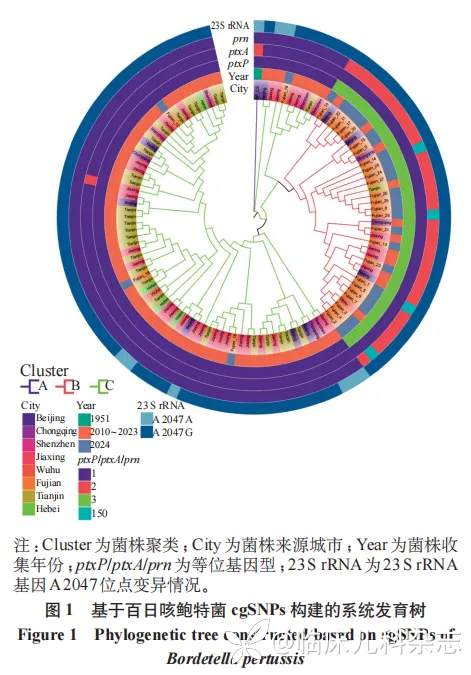
2.3 系统发育分析
基于 29 株 BP 临床分离株、疫苗株 CS 的全基因组序列及 NCBI SRA 数据库中收录的国内部分地区 BP 菌株基因组数据,通过 cgSNPs 构建系统发育树(图 1)。全基因组 SNP 进化树分析显示,111 株不同时期菌株呈现显著遗传分化,形成三个特征性聚类:A 聚类以疫苗株 CS 为核心形成独立进化分支,该 1951 年北京分离株(ptxP1/prn1/ptxA2 型)与其他菌株遗传距离较大;B 聚类以 ptxP3/prn2/ptxA1 为优势基因型,主要由 2020 年前采集的北京、重庆、嘉兴、芜湖等地区部分菌株及 2024 年福建地区的 21 株分离株及 4 株 prn150 型菌株构成;C 聚类则集中分布于 2020 年前天津、嘉兴、北京、深圳等地区,以 ptxP1/prn1/ptxA1 型为主,仅含 4 株 2024 年福建分离株,福建地区菌株呈现明显的基因型转换趋势,ptxP3 型占比达 86.2%(25/29)。
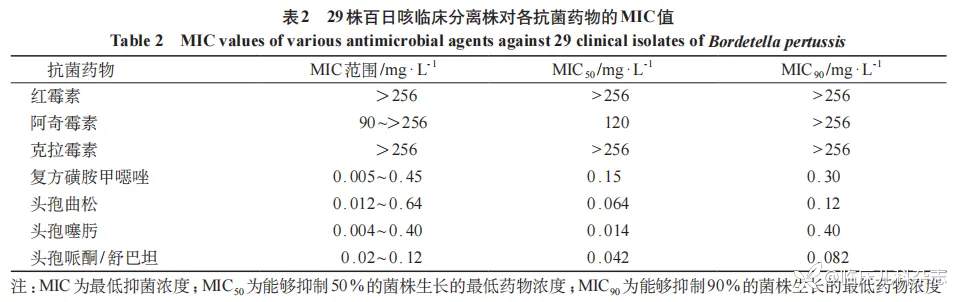
2.4 抗菌药物敏感性分析
E-test 结果显示,29 株 BP 分离株对大环内酯类药物的 MIC90 均超过 256 mg/L。相比之下,分离株对其他抗菌药物 MIC 值处于较低水平,MIC90 分别为:TMP-SMX 0.30 mg/L、头孢曲松 0.12 mg/L、头孢噻肟 0.40 mg/L、头孢哌酮/舒巴坦 0.082 mg/L,见表 2。参考 CLSI M100-Ed33(2023 年)[15] 中流感嗜血杆菌和大肠埃希菌的判定标准,所有菌株对 TMP-SMX 及β-内酰胺类药物(头孢曲松、头孢噻肟、头孢哌酮/舒巴坦 2∶1)的 MIC 值均低于该标准中定义的耐药折点。
3 讨论
百日咳作为一种高传染性急性呼吸道疾病,疫苗接种始终是防控的核心策略。我国全面推行百日咳疫苗接种后,发病率与病死率显著下降。然而,随着疫苗的大规模应用,BP 逐渐面临由疫苗诱导的免疫选择压力,促使其通过抗原基因变异来逃逸宿主免疫系统的识别与清除,导致疫苗保护效果受到挑战,这被认为是近年来百日咳发病率回升的重要原因之一 [16]。因此,开展 BP 抗原基因型监测对揭示区域百日咳流行病学变化规律具有重要意义。
全球范围内,BP 流行株呈现明显的基因型更替特征,逐渐从疫苗相关型(ptxP1/prn1/ptxA2)向非疫苗型(ptxP3/prn2/ptxA1)转变 [17-23],这种转变被认为与疫苗施加的选择压力密切相关。疫苗诱导的免疫应答主要针对 PT、PRN 等关键抗原,PT 的表达水平受其启动子基因 ptxP 调控,研究表明,携带 ptxP3 型菌株 PT 分泌量显著高于 ptxP1 型,从而表现出更强的毒力 [24]。同时 prn2 等位基因的变异则可能影响抗原表位暴露 [25],协同增强菌株的免疫逃逸能力。本研究中 BP 分离株以 ptxP3/prn2/ptxA1 型为主(72.4%,21/29),这一分布模式与我国近年多地监测数据高度吻合,如北京(88.3%)[26]、上海(72.7%)[27]、深圳(62.0%)[8],均显示 ptxP3/prn2 型的绝对优势。提示我国 BP 流行株的抗原漂移可能已形成跨地域的协同进化格局。PRN 作为百日咳疫苗中的关键保护性抗原,其缺失可能削弱疫苗保护效力,且动物模型证实 prn 阴性菌株呼吸道定植能力增强 [28],因此受到广泛关注。近年来多个国家陆续报道了 prn 阴性菌株的出现 [29-31],然而我国此类变异株仍较罕见 [27,32],本研究中亦未检出。值得注意的是,本研究发现 4 株(13.8%)prn150 菌株(基因型 ptxP3/prn150/ptxA1),这些菌株均携带 23S rRNA A2047 G 突变。已有研究表明,此类耐药菌株可能与 COVID-19 之后国内百日咳发病率上升直接相关 [33],需警惕 prn150 变异株可能成为新的疫苗逃逸分支。本研究中以 ptxP3/prn2 基因型菌株为主导,一方面因该型菌株高 PT 分泌引发典型痉咳症状,增加就医与检出概率 ;另一方面,疫苗诱导的群体免疫屏障可能对低毒力菌株形成生态位挤压,最终导致高毒力基因型在传播链中占据主导地位。
我国 BP 临床分离株对大环内酯类药物的耐药率高达 70% 至 100%,显著高于国际水平 [34],本研究进一步证实上述现象:福建地区分离株对大环内酯类的 MIC50 及 MIC90 均大于 256 mg/L,且所有菌株均检出 23S rRNA 基因 A2047 G 点突变,该突变是 BP 耐药的主要分子机制 [34]。本研究中高耐药率的出现,一方面是由于研究样本量有限,且部分纳入对象是经前期抗菌药物治疗无效后转诊的病例,可能导致耐药菌株的入选比例偏高。另一方面,国内抗菌药物使用模式的差异性 [35],可能使 BP 流行株长期暴露于较强的药物选择压力,进而促进耐药克隆的传播与优势化 [36]。鉴于大环内酯类耐药的高流行率,探索有效的替代治疗方案至关重要。国内现行指南推荐 TMP-SMX 作为大环内酯类耐药百日咳的替代药物 [10],本研究显示,TMP-SMX 对 BP 的 MIC 较低(MIC90 = 0.30 mg/L),体外抗菌活性良好,这与 Li 等 [37] 报道的国内其他地区数据一致。然而,需警惕 TMP-SMX 耐药发生的潜在风险,如 Hua 等 [38] 已报道耐药株的出现,提示未来需加强监测。β-内酰胺类抗菌药物是另一类潜在的替代治疗选择。本研究中,头孢曲松、头孢噻肟及头孢哌酮/舒巴坦对分离株的 MIC90 值分别为 0.12 mg/L、0.40 mg/L 和 0.082 mg/L,表明这些药物在体外对 BP 具有较强的抑制活性。然而,评估β-内酰胺类抗菌药物的临床价值需考虑其在呼吸道的药代动力学特性。既往研究显示,部分β-内酰胺类抗菌药物(如氨苄西林)在呼吸道黏膜的浓度较低,可能导致临床疗效受限 [39]。但是根据 Mi 等 [40] 报道,使用哌拉西林/他唑巴坦治疗的患儿,其鼻咽部 BP 清除率在治疗 14 天后显著高于接受大环内酯类药物治疗的患儿。现有证据提示β-内酰胺类药物可能对治疗大环内酯类耐药 BP 感染具有潜力 [41]。但其临床应用仍面临关键问题,如不同β-内酰胺类药物在呼吸道的分布存在显著差异,需具体药物具体分析;现有临床疗效数据多来源于观察性研究或小样本报告,亟需开展设计严谨的前瞻性、多中心随机对照试验,以系统评估β-内酰胺类药物在百日咳治疗中的有效性及安全性。
综上,福建省 BP 流行株已呈现向 ptxP3/prn2 基因型演化的趋势,并表现出对大环内酯类药物高度耐药,本研究为优化疫苗策略、加强耐药监测提供了依据,有助于应对百日咳再现的公共卫生挑战。同时也存在一定局限性:首先,样本来源局限于福州及尤溪两地区,是否能够代表整个福建省的百日咳流行情况尚未获得验证,可能存在选择偏倚;其次,本研究采用被动监测方式收集数据,样本量相对有限,且未涵盖无症状感染者及全年龄段人群,可能影响基因型分布和药物敏感性评估的代表性与全面性。后续研究将拓展样本来源区域,增加样本量,纳入更多年龄群体,以提升基因型分布评估的代表性与可靠性。
好文章,需要你的鼓励















