


科研速递│免疫疗法不起效?可能是这种氨基酸在「帮倒忙」!浙大四院王凯教授团队《Advanced Science》带来最新发现
肺癌,长期盘踞我国癌症死亡率的首位。虽然免疫检查点抑制剂(如 PD-1/PD-L1 抗体)带来了革命性的治疗希望,但一个残酷的现实是:仅有约 20%-30% 的患者能从中显著获益。如何突破瓶颈,找到更有效的联合疗法,让更多患者受益?
7 月 10 日,浙江大学医学院附属第四医院王凯教授团队在国际期刊《Advanced Science》在线发表题为"Targeting Cystine Metabolism in the Lung Cancer Environment Enhances the Efficacy of Immune Checkpoint Inhibition"的研究论文。
团队深入探索肺癌微环境中的代谢奥秘,聚焦于肿瘤相关巨噬细胞(TAMs,肿瘤内部的「帮凶」免疫细胞)中异常活跃的胱氨酸代谢,并带来了一项令人振奋的发现——
调节肺癌患者体内一种名为「胱氨酸」的氨基酸代谢,可能成为激活免疫疗法潜力的关键钥匙!

研究揭示:
1. 「饿死」胱氨酸,唤醒免疫「战士」:
当研究人员在实验(体外细胞培养和小鼠模型)中限制巨噬细胞的胱氨酸摄入,或者直接给小鼠喂食无胱氨酸饲料时,神奇的事情发生了——
这些巨噬细胞开始从促癌的「M2」型向抗癌的「M1」型转变!它们大量分泌 TNF-α、CXCL9、CXCL10 等抗肿瘤因子,有效抑制了肺癌的生长。
2. 意外发现:狡猾肿瘤的「免疫刹车」:
然而,研究也发现了一个「副作用」。在胱氨酸缺乏的情况下,被「唤醒」的 M1 型巨噬细胞会显著上调表达 PD-L1 蛋白。PD-L1 正是癌细胞用来抑制免疫细胞攻击的关键分子。
这意味着,单纯限制胱氨酸虽然能激活部分免疫攻击,但肿瘤微环境会同时启动「刹车」机制,削弱治疗效果。
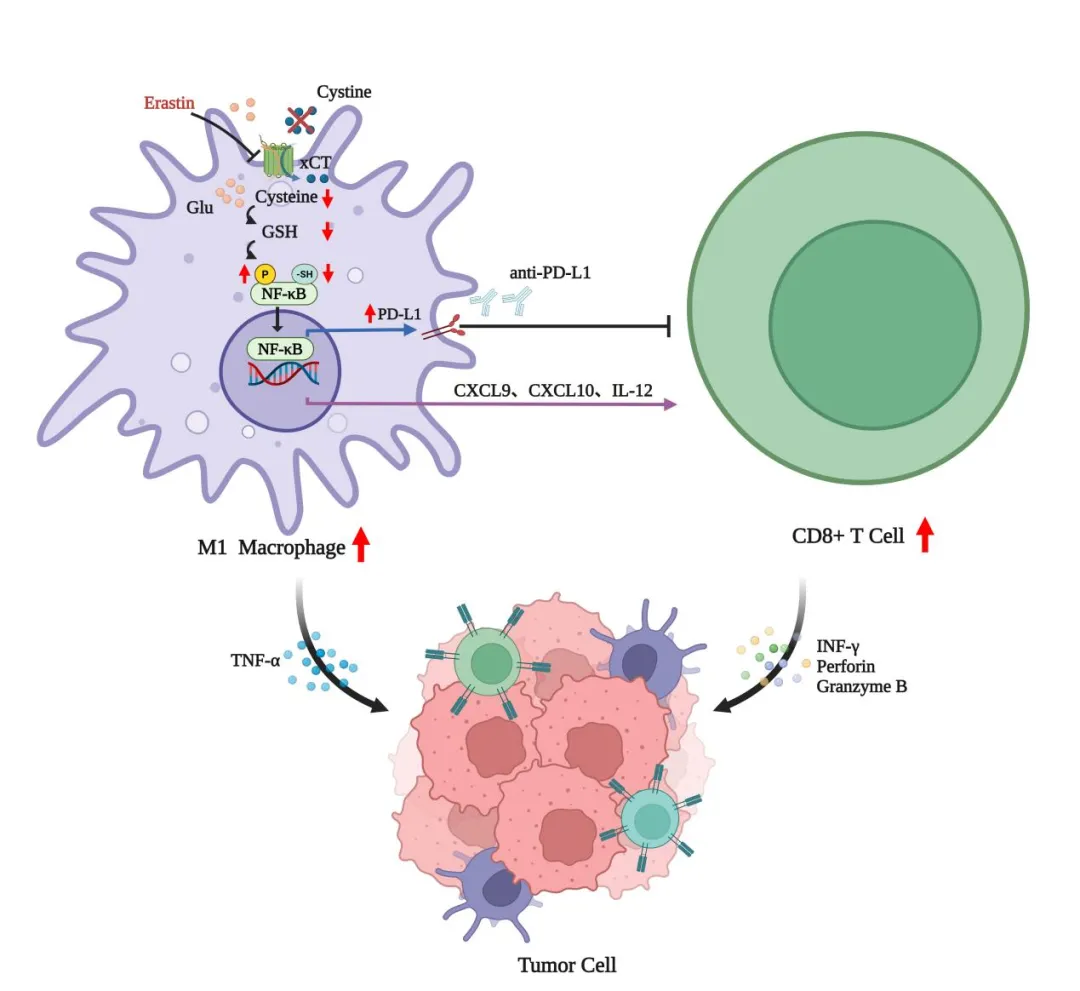
关键破局:「双管齐下」,协同增效
既然限制胱氨酸能激活巨噬细胞(增强「油门」),但同时也会诱发 PD-L1 升高(踩了「刹车」),那么,如果同时踩下「油门」并解除「刹车」会怎样?
研究团队给出了激动人心的答案:将限制胱氨酸与 PD-L1 抗体联合使用,产生了强大的协同抗肿瘤效果!
在小鼠模型中,这种组合疗法显著抑制了肺癌的生长和转移,效果远优于单用任何一种方法。联合治疗组肿瘤内冲锋陷阵的 CD8+ T 细胞数量大增,其释放的「武器」(如 IFN-γ、颗粒酶 B、穿孔素)也显著增多。
王凯教授团队的这项突破性研究,不仅揭示了肺癌微环境中胱氨酸代谢调控免疫反应的全新机制(谷胱甘肽 GSH 耗竭→NF-κB 去谷胱甘肽化→激活),更重要的是,为克服免疫治疗耐药性提供了极具前景的联合策略:靶向胱氨酸代谢 + PD-1/PD-L1 抑制剂。
这意味着,未来通过特定的饮食干预(精确调控氨基酸摄入)或开发靶向药物,结合现有的免疫疗法,有望大幅提升肺癌患者的治疗效果,让更多患者从免疫治疗中获益。
科学的力量,正在将「精准营养」与「精准免疫治疗」紧密结合,为抗击肺癌开辟充满希望的新战场。

研究团队介绍
浙江大学医学院附属第四医院,浙江省肺癌精准诊疗重点实验室主任王凯教授为论文通讯作者,浙江大学医学院附属邵逸夫医院肖鹏研究员为共同通讯作者。浙江大学医学院附属第四医院许云研究员为论文第一作者。本研究受到国家重点研发计划、国家自然科学基金区域重点等项目资助。

通讯作者:王凯
教授、主任医师 博士生导师
浙大四院和「一带一路」国际医学院党委书记
全省肺癌精准诊疗重点实验室主任
浙江大学求是特聘教授
国家重点研发计划首席科学家
享受国务院特殊津贴专家
浙江省医学会呼吸病学分会候任主任委员,浙江省抗癌协会肺癌专业委员会候任主任委员,中国抗癌协会低氧肿瘤学专业委员会副主任委员,中华医学会呼吸病学分会肺癌学组委员,Cancer Letters (IF 9.1) 杂志编委。国家科学技术进步二等奖、教育部科学技术进步奖一等奖、浙江省科学技术进步一等奖、浙江省十大杰出青年。
研究方向为肺干细胞调控慢性肺病相关机制解析及干预新技术,肺癌靶向和免疫治疗疗效相关机制,肺癌微环境调控机制及新型抗癌药物研发等。

论文第一作者:许云
研究员 硕士研究生导师
浙大四院临床研究中心主任助理
研究方向:肿瘤免疫及慢性肺病治疗
浙大四院呼吸医学中心
浙江省肺癌精准诊疗重点实验室
浙大四院呼吸医学中心由呼吸与危重症医学科、心胸外科、放射科、病理科共同组成,中心现有医生 85 名,高级职称医师 27 名,其中博士生导师 2 名,硕士生导师 6 名,特聘研究员 9 名。2023 年,年门诊量达 13 万余人次,年手术量 2000 余台次,支气管镜介入治疗稳居全省前列。
浙江省肺癌精准诊疗重点实验室于 2024 年 7 月批准成立,为浙江省唯一认定的肺癌领域省级重点实验室,依托于浙江大学医学院附属第四医院,充分发挥本院、国科大杭州高等研究院及华东医药有限公司联合共建优势,集成三家单位丰富的临床资源、完善的基础平台、雄厚的研发能力的优势力量。

好文章,需要你的鼓励













