EHA 2024 丨张弦主任:CD7 CAR-T 治疗复发/难治急性 T 淋巴细胞白血病/T 淋巴母细胞淋巴瘤后的免疫重建
以下文章来源于血液时讯 ,作者血液时讯

2024 年 6 月 13 日~16 日, 第 29 届欧洲血液协会(EHA)年会在西班牙的首府马德里隆重举行,作为欧洲血液学领域规模最大的国际会议,每年都吸引着来自世界各地的专家学者,一起分享并探讨有关血液学的创新理念及最新的科学和临床研究成果。在本届 EHA 会议上,陆道培医院张弦主任
的一项研究(S119)入选了大会 Oral,该研究探讨了 R/R T-ALL/LBL 患者在接受 CD7 CAR-T 治疗后的免疫重建情况,《肿瘤瞭望-血液时讯》特邀采访了张弦教授围绕该研究的内容和 R/R T-ALL/LBL 治疗的话题进行了介绍和解读。
研究简介
难治或复发急性 T 淋巴细胞白血病/T 淋巴母细胞淋巴瘤(R/R T-ALL/LBL)在接受 CD7 CAR-T 治疗后的免疫重建情况的探索
背景
CD19 CAR-T 在难治/复发急性 B 淋巴细胞白血病(R/R B-ALL)的治疗中展现出卓越的疗效,完全缓解率(CR)可达 90% 左右。最近的研究表明,CD7 CAR-T 在难治或复发急性 T 淋巴细胞白血病/T 淋巴母细胞淋巴瘤(R/R T-ALL/LBL)中也显示出优秀的治疗作用。CD19 CAR-T 的副作用已被证实对于患者的免疫功能无显著影响,但关于 CD7 CAR-T 的毒副作用,尤其是对于 T 细胞的细胞毒性效应仍不确定。
目的
旨在探讨 R/R T-ALL/LBL 患者接受 CD7 CAR-T 治疗后的免疫重建情况。
方法
该研究入组了 2020 年 12 月~2022 年 6 月间的 60 例 R/R T-ALL/LBL 患者,并接受自然选择的抗 CD7 CAR-T(NS7CAR-T)治疗,与此同时,另有 60 例 R/R B-ALL 患者接受了 CD19 CAR-T 治疗,将其作为 CD7 CAR-T 组的对比,数据提取自两个独立的临床试验。患者在输注 CAR-T 前接受淋巴细胞清除治疗,在 CAR-T 输注后,通常桥接异基因造血干细胞移植(allo-HSCT)巩固治疗。我们分析了从 CD7 CAR-T 或 CD19 CAR-T 细胞输注到 allo-HSCT 期间的感染发生情况(感染诊断包括病因学和影像学诊断)。
40 例输注 CD7 CAR-T 细胞治疗的患者在第 0、4、8、11、14、21 和 28 天时采用流式细胞术对总 CD3+ T 细胞绝对值进行检测,然后分别测定 CD7+ CD3 + T 细胞、CD7- CD3+ T 细胞、CAR-T 细胞/CD7-CD3+ T 细胞中的比例和绝对值。
结果
在疗效方面,经 CD7 CAR-T 治疗后,94.4%(51/54)的 R/R T-ALL/LBL 患者达到了骨髓的完全缓解(CR)。
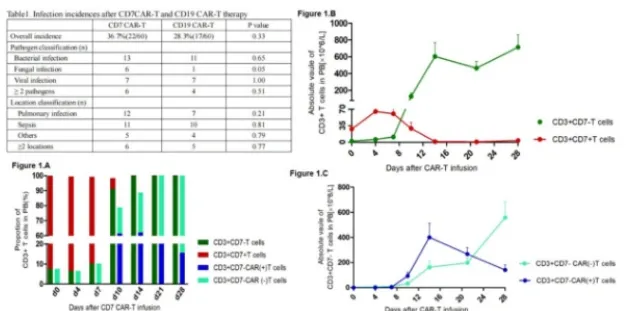
安全性方面:①53/60(88.3%)例 CD7 CART 患者出现了轻度的细胞因子释放综合征 (CRS,≤ II 级), 另有 6 例 CRS 为 III 级,1 例为 IV 级。神经毒性事件方面,仅有 2 例为 I 级,1 例为 IV 级。②在感染发生率上,CD19 CAR-T 治疗组和 CD7 CAR-T 治疗组的总体感染发生率无统计学差异,分别为 28.3% vs 36.7%(p = 0.33)(表 1)。但需要指出的是,CD7 CAR-T 组的真菌感染率明似乎要高于 CD19 CAR-T 组,分别为 10% vs. 1.7%(P= 0.05)。
另外,我们分析了 40 例接受 CD7 CAR-T 治疗的患者中 CD3+ T 细胞中的 CD7+/CD7- T 细胞的比例和绝对值,以及 CAR-T 和非 CAR-T 细胞在 CD7- CD3+T 细胞中的比例和绝对值。 结果发现: 在 CAR-T 输注前,外周血中已有较低水平的 CD7-细胞(平均约占 7.5%),而在 CAR-T 输注后,随着时间的推移,CD7+T 细胞数量明显减少,CD7-T 细胞的数量却逐渐增加。在 CD7-T 细胞中,除了 CAR-T 细胞外,非 CAR-T 的 CD7-T 细胞却表现出显著的增加,并保持在一个高水平(图 1)。
结论
这项研究表明,在接受 CD7 CAR-T 治疗后,R/R T-ALL/LBL 患者并未发生严重的副作用,总体感染率没有显著的增加,但 CD7 CAR-T 组的真菌感染率较之于 CD19 CAR-T 组要相对更高。此外,我们发现,在 CD7 CAR-T 输注后 CD7+ T 细胞显著减少,非 CAR-T CD7- T 细胞却明显增加,这可能是其在 CAR-T 治疗后能够维持免疫功能的原因,故 CD7 CAR-T 对免疫功能并没有产生实质性的影响。但是,在超过 2 个月的观察期之后,allo-HSCT 巩固治疗和 CD7 CAR-T 对免疫重建的长期影响仍不确定。
《肿瘤瞭望-血液时讯》
张教授,恭喜您的研究在 EHA 大会上入选口头报告。能否简要介绍一下您团队这项研究的背景和主要目标?
张弦主任:首先,这是一项非常有意义的临床研究,主要针对的患者群体为难治/复发急性 T 淋巴母细胞白血病/淋巴瘤(R/R T-ALL/LBL),在 CD7 CAR-T 出现之前,此类患者的治疗可谓非常棘手,治疗选择乏善可陈,死亡率相当高。从 2020 年 9 月开始,我们团队开始探索 CD7 CAR-T 在 R/R T-ALL/LBL 中的治疗应用,截至目前,已经入组了超过 200 例患者,结果显示,其具有非常不俗的疗效,完全缓解率(CR)可达 90% 以上。但值得关注的一个问题是,R/R T-ALL/LBL 患者在接受 CD7 CAR-T 治疗后的免疫重建和感染情况如何,目前国内外尚无明确的数据来阐明,因此该研究旨在提供一个详实的临床数据支持来阐明该问题,尝试得出一些相对可靠的结论,为临床医生带来一定的指导。
《肿瘤瞭望-血液时讯》
该研究探讨了使用 CD7 CAR-T 治疗对 R/R T-ALL/LBL 患者免疫重建的影响。请您介绍下研究有哪些主要发现?这些发现对于推进 CD7 CAR-T 疗法的进一步研究或临床应用有何重要意义?
张弦主任:近十余年,CD19 CAR-T 在难治/复发急性 B 淋巴细胞白血病(R/R B-ALL)的治疗中取得了令人瞩目的疗效成果,完全缓解率达到了 90% 以上,并且研究已经证实 CD19 CAR-T 对于患者的免疫功能并没有明显影响。但是,CD7 CAR-T 的治疗标靶为 T 细胞,而 T 细胞是人体非常重要的免疫细胞,那么将 T 细胞清除后患者的免疫功能是否会受到严重的影响?这无疑令人疑惑和担忧。事实上,我们团队已经开展 CD7 CAR-T 的临床研究达 3 年之久,临床上似乎并未观测到明显的免疫功能破坏,为了进一步探究其中的机制,我们团队开展了这项研究,旨在阐明 CD7 CAR-T 后 R/R T-ALL/LBL 患者免疫重建的情况,本研究纳入了 60 例接受 CD7 CAR-T 治疗的 R/R T-ALL/LBL 患者,并且与同期接受 CD19 CAR-T 治疗的 60 例 R/R B-ALL 患者进行对比分析,结果显示,两组患者在总体感染发生率未见明显的差异,CD7 CAR-T 组的真菌感染率较之于 CD19 CAR-T 组确实要相对更高,但尚不能排除是因为样本量不够所带来的结果偏差。总体而言,CD7 CAR-T 与 CD19 CAR-T 治疗后的总体感染发生率基本相似。
为了深入挖掘原因,该研究对 CD7 CAR-T 治疗后的 T 细胞功能进行了详细的亚组分析,着重测定和分析了 CD3+ T 细胞中的 CD7+/CD7- T 细胞的比例和绝对值,以及 CAR-T 和非 CAR-T 细胞在 CD7-CD3+T 细胞中的比例和绝对值。我们惊奇地发现,在 CD7 CAR-T 输注后,随着时间的推移,CD7+细胞数量明显减少,CD7-细胞的数量逐渐增加。值得特别指出的是,在 CD7-细胞中,当 CAR-T 细胞随着时间推移开始下降时,非 CAR-T 的 CD7-T 细胞却仍然保持上升趋势,并且保持在相对稳定的高水平,而查阅文献也指出,CD7- T 细胞也能提供正常的免疫功能。因此,我们得出一个结论:在 CD7 CAR-T 治疗 R/R T-ALL/LBL 后并未出现令人担忧的免疫功能问题,其原因在于 CD7- T 细胞替代 CD7+ T 细胞为人体提供和保持了基本的免疫功能。
《肿瘤瞭望-血液时讯》
鉴于 CD7 CAR-T 治疗在 R/R T-ALL/LBL 中已展现出令人瞩目的疗效,您和团队对于深入研究其长期影响有哪些规划与展望?
张弦主任:目前 CD7 CAR-T 在 R/R T-ALL/LBL 治疗中的疗效非常好,完全缓解率高达 90%,对于髓外的病灶也有很好的清除作用。除了疗效之外,在研究的观察期间,患者在治疗后的免疫功能未受到明显的影响。至于真菌感染率略高的问题,我们认为需要通过扩大患者的样本量和延长随访时间来进一步明确。另外,CD7 CAR-T 中位缓解持续时间(mDOR)大约为 3 个月之间,我们中心通常在 CART 细胞输注后 2~3 个月内需要桥接 allo-HSCT,我们对于桥接 allo-HSCT 后的患者免疫功能情况有较大的研究兴趣,下一步我们将在该方面开展深入的研究挖掘,以期带来更多的数据信息。
《肿瘤瞭望-血液时讯》
最后,在 R/R T-ALL/LBL 治疗方面,您认为还有哪些有前景的治疗手段或研究方向值得进一步探索?
张弦主任:首先,上述我们探讨了 CD7 CAR-T 在 R/R T-ALL/LBL 治疗中的可喜进展,其 CR 达到了 90% 以上,然而仍有少部分患者对该治疗无效,因此新型靶点的挖掘依然是未来的研究方向之一,例如 CD5 靶点。其次,R/R T-ALL/LBL 在 CD7 CAR-T 治疗后需桥接 allo-HSCT,然而有些患者在 CAR-T 后无法进行 allo-HSCT(无法耐受或已经是移植后),如何维持这些患者的无病生存(DFS),是我们后续需要进一步探讨的问题,例如增加新型小分子药物的应用和 CD5 CAR-T 巩固等,这些目前还停留于临床研究的思路阶段,尚未在临床中应用。然后,CD7 CAR-T 能否拓展至其他恶性肿瘤疾病的治疗中,也是当前需要探索的方向,目前已有一定的研究数据,例如在外周 T 细胞淋巴瘤(PTCL)、CD7 阳性急性髓系白血病中的应用,这是目前潜在可应用 CD7 CAR-T 的病种。最后,新型靶向药、抗体药物偶联物(ADC)及双特异性抗体等也是 R/R T-ALL/LBL 治疗中能够进一步展望前景的药物。

专家简介
张弦 主任
陆道培医院普通血液科主任 (副院长级),血液学博士,主任医师
中国抗癌协会第五届血液肿瘤专业委员会造血干细胞移植与细胞治疗学组委员
中国医师协会血液科医师分会委员
中国研究型医院学会细胞研究与治疗学专业委员会委员
中国输血协会人类组织抗原专业会专家组委员
北京市抗癌协会血液淋巴血液肿瘤专业委员会委员
北京市癌症防治学会红细胞疾病专业委员会委员
河北省血液学会淋巴瘤专业委员会委员
廊坊市门诊特殊疾病鉴定专家
廊坊市抗癌协会药物临床试验安全性评价专业委员会常务委员
来源:《肿瘤瞭望–血液时讯》编辑部
好文章,需要你的鼓励