近日,普通外科孙学军教授团队在 Nature Press(自然出版集团)旗下细胞死亡领域权威期刊 Cell Death & Differentiation(2022 IF: 12.4)在线发表题为「USP51 facilitates colorectal cancer stemness and chemoresistance by forming a positive feed-forward loop with HIF1A」的研究论文。该研究阐明了 USP51 在结直肠癌细胞耐药中的作用和机制,为预防和逆转结直肠癌耐药提供新思路,为疾病的治疗提供潜在的新靶点,为制定更优的临床治疗策略提供理论依据。

化疗目前仍是结直肠癌治疗的重要方法之一,尤其对于转移性结直肠癌。但几乎所有接受化疗的患者最终会发展为化疗耐药。化疗耐药极大地限制了化疗药物的有效性。研究结直肠癌化疗耐药机制有助于制定更有效的策略来预防或逆转耐药,提高化疗药物的有效性,从而提高患者的生存率。近年来的研究表明,USP51 参与调节了 DNA 损伤修复和肿瘤的侵袭性。然而,USP51 如何参与结直肠癌的耐药却知之甚少。该研究揭示了结直肠癌化疗耐药中的一个重要分子机制,即 USP51 和 HIF1A 之间形成了一个正反馈环路。
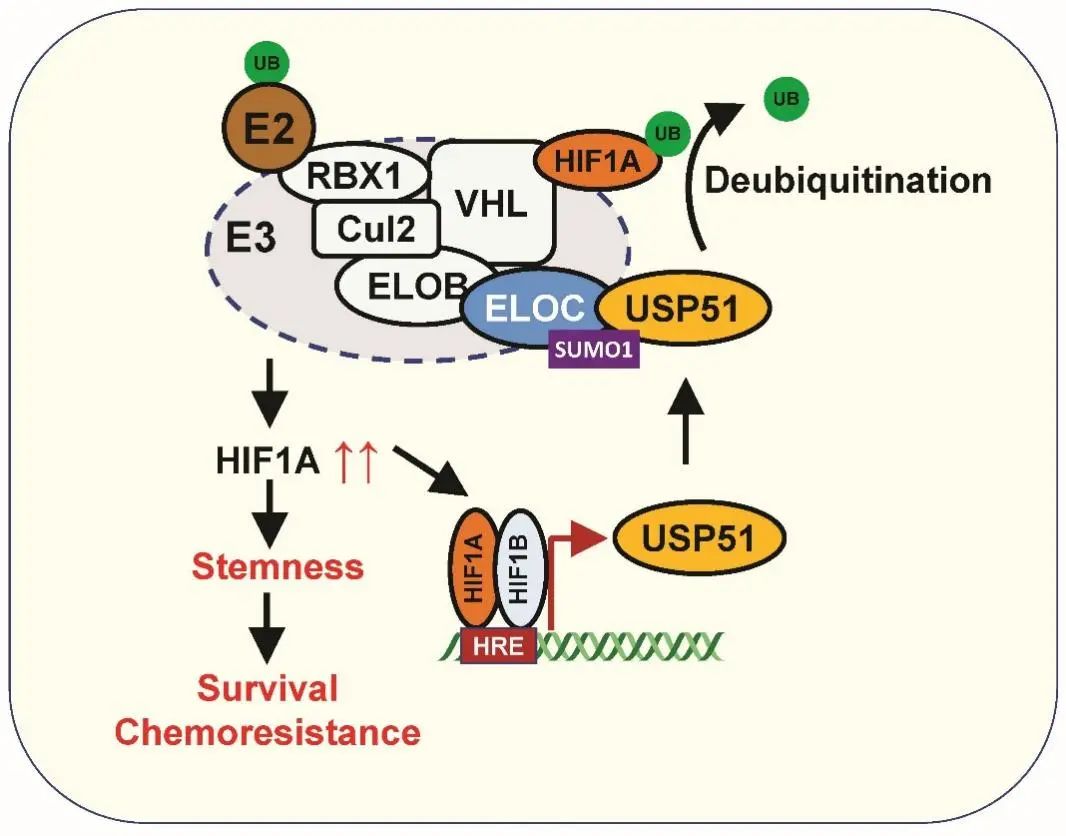
在缺氧条件下,HIF1A 结合在 USP51 的启动子区域,激活 USP51 的转录,导致 USP51 蛋白水平增加。USP51 蛋白通过与 ELOC 的直接互作而与 VHL E3 连接酶形成复合物。USP51 去泛素化并稳定 HIF1A 蛋白,阻止 HIF1A 通过泛素-蛋白酶体途径降解。HIF1A 蛋白在细胞内累积,激活包括 USP51 在内的下游基因的转录。HIF1A-USP51 正反馈环路导致 USP51 和 HIF1A 蛋白在细胞内均增加。细胞内 HIF1A 累积促进了细胞的生存、干性和耐药。
在这个正反馈环路中,ELOC 的苏木化修饰也发挥了调节作用。ELOC K32 位点的 SUMO1 修饰抑制了 ELOC 与 USP51 的结合,抑制了 USP51 对 HIF1A 的去泛素化作用。SENP1 介导的 ELOC 去苏木化促进了 ELOC 和 USP51 的结合,促进了 USP51 对 HIF1A 的去泛素化作用,上调了细胞中 HIF1A 的蛋白水平。
研究癌症治疗中的化疗耐药有助于开发更有效的治疗策略,提高患者的生存率。同时,深入了解缺氧环境对肿瘤细胞的影响可以揭示新的治疗靶点和策略。事实上,该研究揭示了 USP51 在肿瘤干性和耐药性中的潜在作用,为研发特异性抑制剂提供了潜在的治疗靶点,为未来的治疗方法开辟了新的方向。
该研究对于改善结直肠癌患者的治疗效果具有重要的临床意义。西安交通大学第一附属医院普通外科牟明超博士为本文的第一作者,孙学军教授和余钧辉副研究员为论文共同通讯作者,西安交通大学第一附院医院为第一完成单位。孙学军教授团队长期致力于胃肠道肿瘤发病机制研究。近几年团队得到了国家自然科学基金(81972720、82002547)、陕西省重点研究计划(2022ZDLSF03-02;2022SF-309;2021SF-311;2019SF-065)、中央高校基本科研业务费(xzy012022102)和交大一附院科学基金(2022MS-17;2019QN-12)等项目资助。
好文章,需要你的鼓励















