近日,高博医疗集团「博医同行,情暖重阳」大型科普系列活动——「淋巴瘤&骨髓瘤科普专场」特别邀请到高博医学(血液病)北京研究中心北京博仁医院克晓燕教授、胡凯主任、郑培浩医生、郭玥潞医生围绕淋巴瘤/骨髓瘤进行专题科普。克晓燕教授围绕「老年淋巴瘤患者的治疗之路」进行了系统性解读,帮助大家进一步了解老年淋巴瘤的治疗。
淋巴瘤是一种常见的恶性血液肿瘤,在免疫与化疗时代,复发难治淋巴瘤的预后往往比较差。以弥漫大 B 细胞淋巴瘤(DLBCL)为例,在所有 DLBCL 中,约有 60%~65% 的患者可以通过一线 R-CHOP 方案达到治愈,而有 10%~15% 的患者会出现原发耐药,并且在被治愈的患者当中,也有 20%~30% 的患者会出现复发;在难治复发的这部分患者中,约 50% 的患者可以进行移植治疗,但最终仅有 30%~40% 经过自体造血干细胞移植的患者可以达到治愈,60%~70% 的患者仍然会复发。最终,约有 30% 的患者会发展为化疗和自体干细胞移植失败的复发难治性 DLBCL 病例。
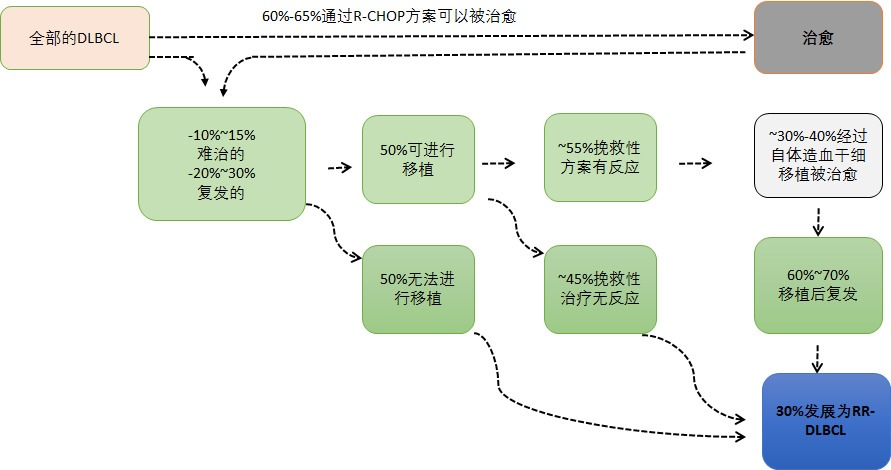
而 SCHOLAB-1 研究对纳入的这些一线化疗和自体干细胞移植后失败的 636 例复发 DLBCL 患者进行了回顾性分析,结果显示这些患者在采用二线方案再治疗后客观缓解率(ORR)仅为 26%,完全缓解(CR)率仅为 7%,中位总生存期(OS)仅 6.3 个月。因此,对于这些复发难治性 DLBCL 来说,传统化疗难以满足患者的治疗需要。
初诊识高危,治疗需分层
近年来,随着对 DLBCL 研究的不断深入,DLBCL 的诊疗策略也在不断发生变化,其中一个重要认识即——初诊时就应识别具有高危复发风险的患者,从而进行分层治疗,降低复发风险。在治疗用药方面,很多患者都有一个认识误区,认为初治时先用低级别的药物治疗,把好药留给复发后再用。但实际上,复发后的治疗难度陡然增大,治疗效果也显著下降。因此,淋巴瘤患者应该在初诊一线治疗时即给予最佳的治疗方案,尽量减少复发。
要想提高一线治疗的有效性,首先需要明确病理诊断。目前,DLBCL 的病理分型可以根据细胞起源分为 GCB 型和非 GCB 型,还可以分为双表达、双打击、高级别 B 等不同类型,不同病理分型的预后也有所不同。另外一些特殊因素如 CD5、P53、CD79B、EBV+也可以提示预后不良。
除病理分型外,随着分子生物学的研究深入,DLBCL 还可以进行基因分型,而不同基因分型的疾病预后也有所不同。
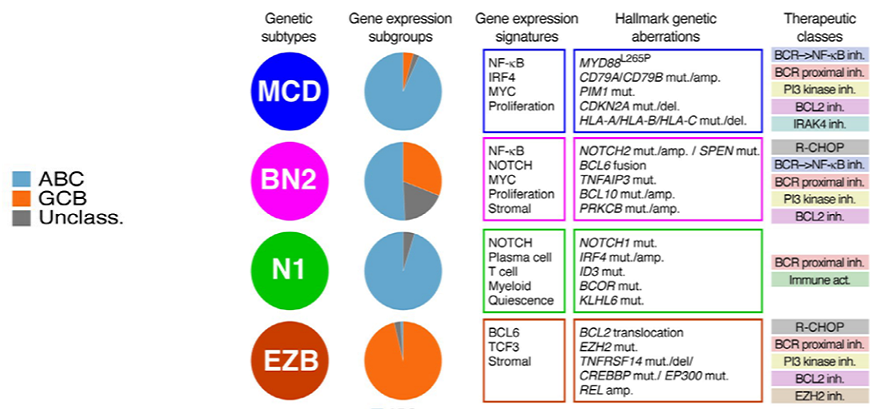
一项研究显示,与 EZB 亚型和 BN2 亚型相比,MCD 亚型和 N1 亚型的无进展生存和总生存明显更差。
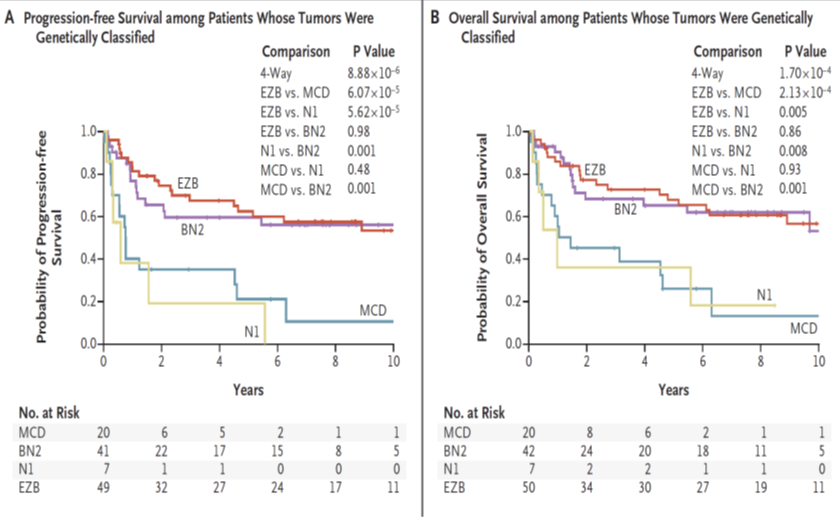
根据不同的病理分型和基因分型,对不同患者进行分层治疗,就可以尽可能减少复发难治淋巴瘤的发生:
1. 对于无不良预后因素的 DLBCL,可采取常规 R-CHOP 方案进行治疗;
2. 对于原发性纵膈 B 细胞淋巴瘤(PMBCL),应采用 R-EPOCH 方案进行治疗;
3. 对于中枢神经系统淋巴瘤(PCNS),应采用 HDMTX 方案进行治疗;
4. 对于高级别 B 细胞淋巴瘤(HGBCL),应采用 R-EPOCH+APBSCT 方案进行治疗;
5. 对于具有不良预后因素和基因的患者,应采用调高治疗如 R-EPOCH 方案或 APBSCT 方案进行治疗。
而对于难治复发患者来说,即便调高治疗级别,也有部分患者难以获得治愈,因而需要借助靶向治疗、免疫治疗等新武器。对于无法耐受高剂量化疗的老年患者,也可以选择以靶向治疗为主的治疗方案。
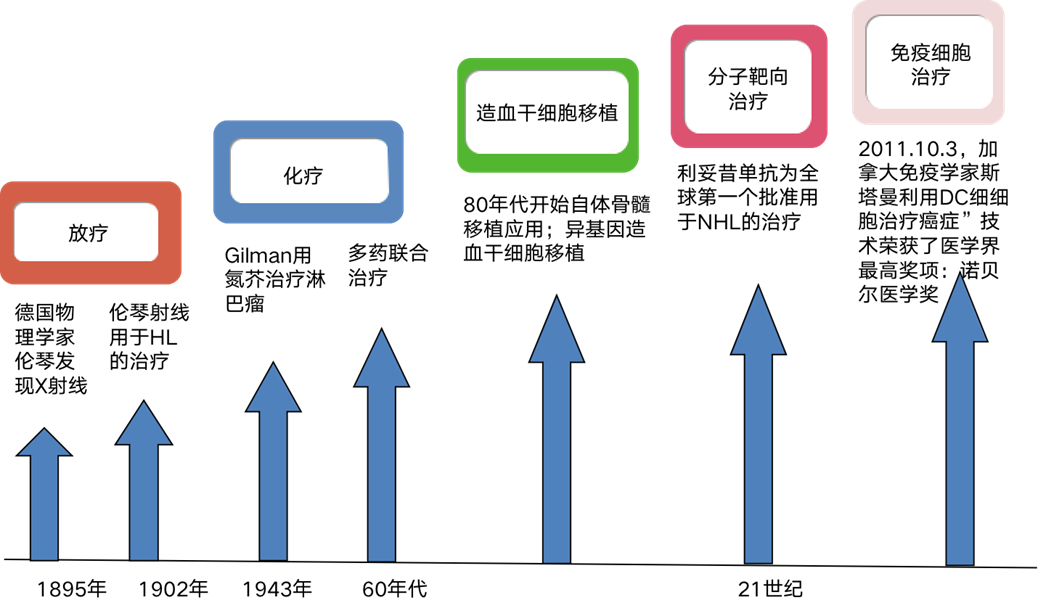
1. 靶向药物的选择需要在二代测序(NGS)指导下,根据不同基因型进行个体化用药。
2. 免疫治疗中的 CAR-T 细胞治疗也在如火如荼的开展当中,目前针对 CD19、CD20、CD22 等靶点的 CAR-T 细胞治疗已经日趋成熟,取得了较好的临床疗效。
3. 另外,CAR-T 治疗联合自体造血干细胞移植治疗也取得了令人鼓舞的疗效,目前对于 80 岁以上老年人群也可以进行尝试。
典型病例
病例介绍
患者男,95 岁确诊淋巴瘤,退休前长期从事放射工作。既往患高血压 20 余年;2 型糖尿病 20 余年。30 余年粒细胞减少的病史(白细胞长期在 2.5~3,Neu 1.2 左右),未予特殊诊治。
2014 年发现三系进行性下降,完善骨髓检查,提示 MDS/AA 可能性大。
2018 年 8 月,患者因发热伴左下颌肿痛就诊,全血细胞减少进一步加重。血常规:白细胞 1.44*10^9/L,血红蛋白 63 g/L,血小板 61*10^9/L
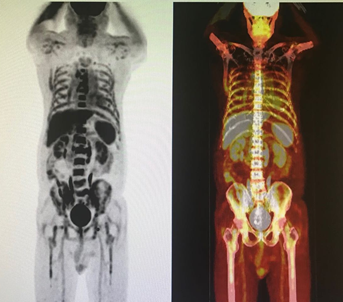
2018 年 9 月,骨髓 0.36% 为可疑异常成熟 B 细胞,表达 CD19,CD20,CD22,CD103,CD11c。B 淋巴瘤克隆性基因重排检测:阳性。FISH:未发现 IgH/CCND1 融合基因,发现 IgH 基因扩增占 20% 骨髓活检:小 B 细胞类淋巴瘤。PET-CT:左侧锁骨下 、纵隔 、双肺门、胸骨旁、前肋膈窦、心膈角、腹腔、肠系膜、腹膜后、双侧腹股沟多发淋巴结,部分肿大,代谢明显增高,符合淋巴瘤表现(纵膈最大淋巴结 2.4*1 cm,腹膜后最大 2.0*1.4 cm,浅表最大 1.3*0.6 cm)。
2018 年 12 月,患者自行触及左侧腹股沟淋巴结肿大,约 4.0*2.5 cm。超声提示:左侧腹股沟区可见一低回声包块,大小约 3.3*2.1 cm,边界不清,形态不规则,周围软组织回声增强,内可见较丰富血流信号。
2018 年 12 月 6 日,左腹股沟淋巴结穿刺。弥漫性大 B 细胞淋巴瘤,非特指型,生发中心;双重打击淋巴瘤。病理免疫组化结果:CD19+,CD20+,CD22+;BCL-2(+>90%),C-MYC(+>70%),Ki-67(+70%),P53 阳性++(野生型)。
注:本次活检肿瘤细胞体积明显大于骨髓活检,增殖活性明显增加。FISH:MYC:60% 断裂;BCL-2:40% 断裂;BCL-6:35% 扩增。基因测序:SOCS1、IRF8、BCL-2、FOXO1、BTG1、MYC、CREBBP、DTX1、GNA13。经基因同源性测定,证明患者骨髓和淋巴结非同源,有复合淋巴瘤,即骨髓有惰性小 B 细胞淋巴瘤,而淋巴结为弥漫性大 B 细胞淋巴瘤。
诊断
1. 淋巴结:高级别 B 细胞淋巴瘤,伴有 C-MYC 和 Bcl-2 重排
2. 骨髓:小 B 细胞淋巴瘤
治疗
1.R 500 mg*2 周期,HGB 72 g/L,腹股沟淋巴结 3.0*2.1 cm
2.R 500 mg*2 周期,HGB 76 g/L,腹股沟淋巴结 3.7*1.8 cm
3.R 500 mg*4 周期+伊布替尼 280 mg/日,HGB 76 g/L,HGB 无变化,及淋巴结稍缩小 3.5*0.9 cm(BP 升高)
4. 换用 BCL-2 抑制剂 12.5 mg/日维持治疗至今,淋巴结逐渐缩小
2021 年 9 月,(98 岁)复查
1. 全身浅表淋巴结及腹腔淋巴结未见肿大;
2.WBC 3.09*10^9/L,HGB 79 g/L,PLT 130*10^9/L;
3. 外周血免疫分型未见异常。
总的来说,弥漫大 B 细胞淋巴瘤的治疗关键在于精准诊断、精准分层、精准初治、减少复发。而对于复发难治患者来说,通过二线化疗并有机结合靶向治疗、免疫治疗等手段,也可以获得生存获益。
好文章,需要你的鼓励
















