来源:首都医学科学创新中心
撰文|张峙轩(2023 级博士研究生)
编辑|梁笑濛(副研究员)
审核|李国民
2026 年 3 月 25 日,应首都医学科学创新中心特聘研究员、肿瘤研究所所长李国民教授的邀请,纽约纪念斯隆-凯特琳癌症中心(Memory Sloan Kettering Cancer Center, MSKCC)的 Dinshaw J. Patel 教授来访并带来一场题为「Antiphage defense by CARF-effector and protective deity systems」的学术报告。
Dinshaw J. Patel 教授现任 MSKCC 结构生物学教授,美国国家科学院院士、美国艺术与科学院院士,长期致力于核酸与蛋白复合物结构生物学研究。其团队运用 X 射线晶体学和冷冻电镜技术,系统解析了 RNA 干扰、DNA 修复以及原核生物抗噬菌体防御系统(包括 Lamassu、PUA-Cal-HAD、CRISPR-Cas 等)的分子机制。
Type III CRISPR-Cas surveillance complex 是原核生物(细菌和古菌)免疫系统中的关键效应复合物,其功能机制较 I 型与 II 型(如 Cas9)系统更为复杂。后者主要通过切割 DNA 发挥功能,而 Type III 系统具备双重靶向能力:一方面直接切割病毒 RNA 与 DNA,另一方面在识别入侵 RNA 后合成信号分子,激活下游辅助蛋白,引发协同性免疫应答。具体而言,当复合物通过 crRNA 识别入侵 RNA 转录本时,其内部的 Cas7 亚基(Csm3)切割目标 RNA,同时 Cas10 亚基(Csm1)激活 DNA 切割活性,降解单链 DNA。被激活的 Cas10 进一步以 ATP 为底物合成环状寡腺苷酸(cOA)作为第二信使,该信号分子随后激活具备 CARF 结构域的辅助核酸酶(如 Csm6),后者无差别降解细胞内 RNA 与 DNA,最终通过诱导流产感染阻止病毒扩散 [1]。
Cat1(cA4-TIR-CARF)是 III 型 CRISPR-Cas 系统中新鉴定的 CARF 效应蛋白,通过消耗宿主细胞内的核心代谢物 NAD⁺来诱导生长停滞,从而阻止噬菌体增殖。Dinshaw J. Patel 教授团队在体外通过孵育 cA₄分子(10s,冰上)成功诱导 Cat1 丝状结构(filament)形成。TIR-CARF 复合物在形成 cA₄复合物时组装成丝状结构。该丝状结构的基本二聚体单元中,CARF 结构域朝向内侧,而 TIR 结构域朝向外侧。在丝状结构中,TIR-CARF 二聚体单元相互堆叠,cA₄分子被夹在 CARF 二聚体之间。该丝状结构进一步形成高阶的三聚体和五聚体排列。NAD⁺被定位在丝状结构中堆叠的 TIR 单体之间;当丝状结构的形成被破坏时,NAD⁺的切割过程也随之被阻断。CARF 结构域作为 cA₄的传感器,cA₄的结合诱导构象变化,从而触发 TIR 结构域的激活;活化的 TIR 结构域消耗 NAD⁺,这种辅酶的耗竭导致流产感染。
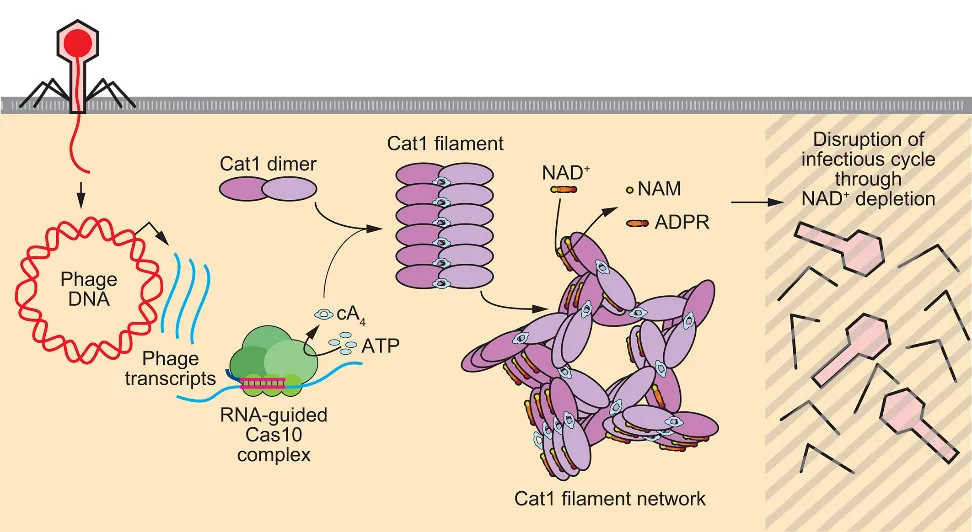
Cat1 丝网(filament network)提供对噬菌体感染的免疫力 [2]
丝状化(filamentation)是细菌抗噬菌体防御中一种广泛存在的激活机制。Pycsar(Pyrimidine cyclase system for antiphage resistance)系统的研究显示,3',5'-cGMP 可作为抗噬菌体免疫的第二信使,拓展了已知的细菌免疫信号分子谱系。此前,III 型 CRISPR 系统利用环状寡腺苷酸(如 cA₄、cA₆)传递感染信号,而 cGMP 的加入表明细菌可利用多种环状核苷酸启动防御。该系统的核心是传感器蛋白 PucTIR。在静息状态下,它组装成四聚体,处于自抑制状态,确保效应器「绝对安全」。一旦感染发生,嘧啶代谢异常触发环化酶产生 cGMP,cGMP 结合会打破四聚体平衡,释放出 PucTIR 二聚体,进一步的 cGMP 结合,使复合物首尾相连,形成反向平行丝状体。当丝状体形成后,相邻亚基间的界面才能共同构成完整的活性口袋,激活 TIR 结构域。最终,NAD⁺被大量消耗,细胞代谢崩溃,触发流产感染。
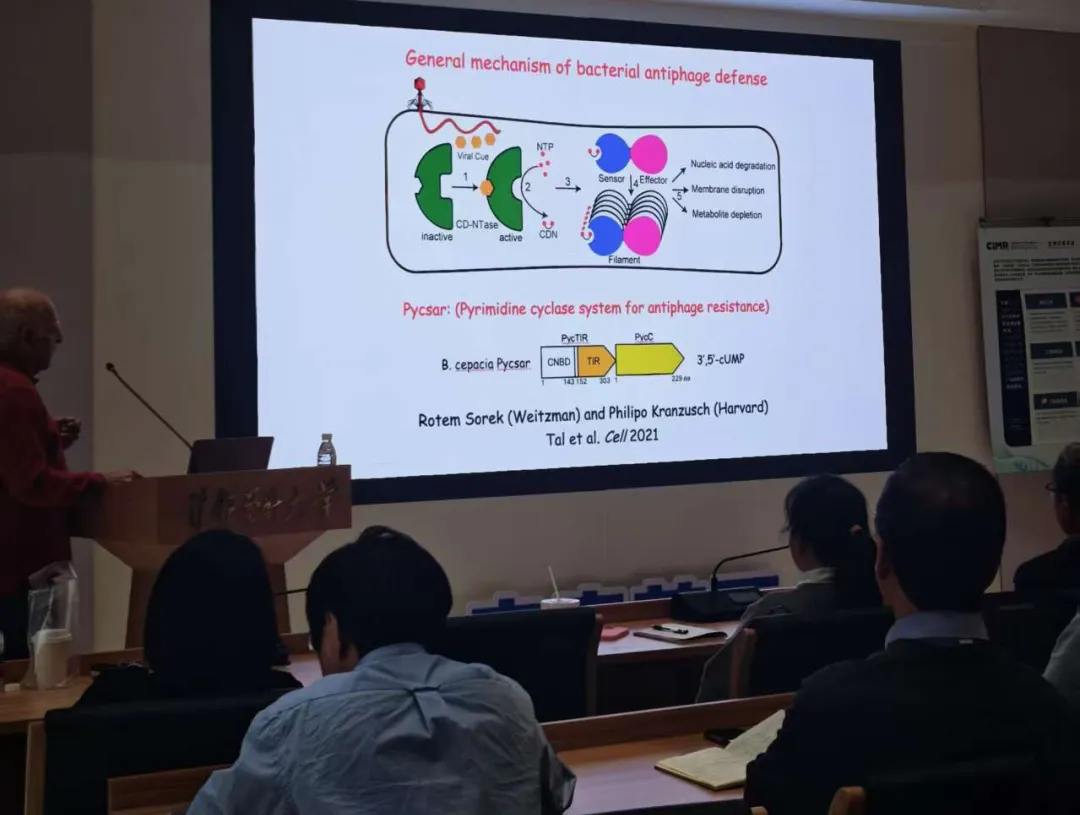
Dinshaw J. Patel 教授介绍 Pycsar(Pyrimidine cyclase system for antiphage resistance)系统
Dinshaw J. Patel 教授介绍了其实验室近年发现的三种抗噬菌体系统:Pucsar、Lamassu 和 PUA-Cal-HAD。其中,Pucsar(Purine cyclase system for antiphage resistance)的相关数据尚未发表,因此在此不作介绍。
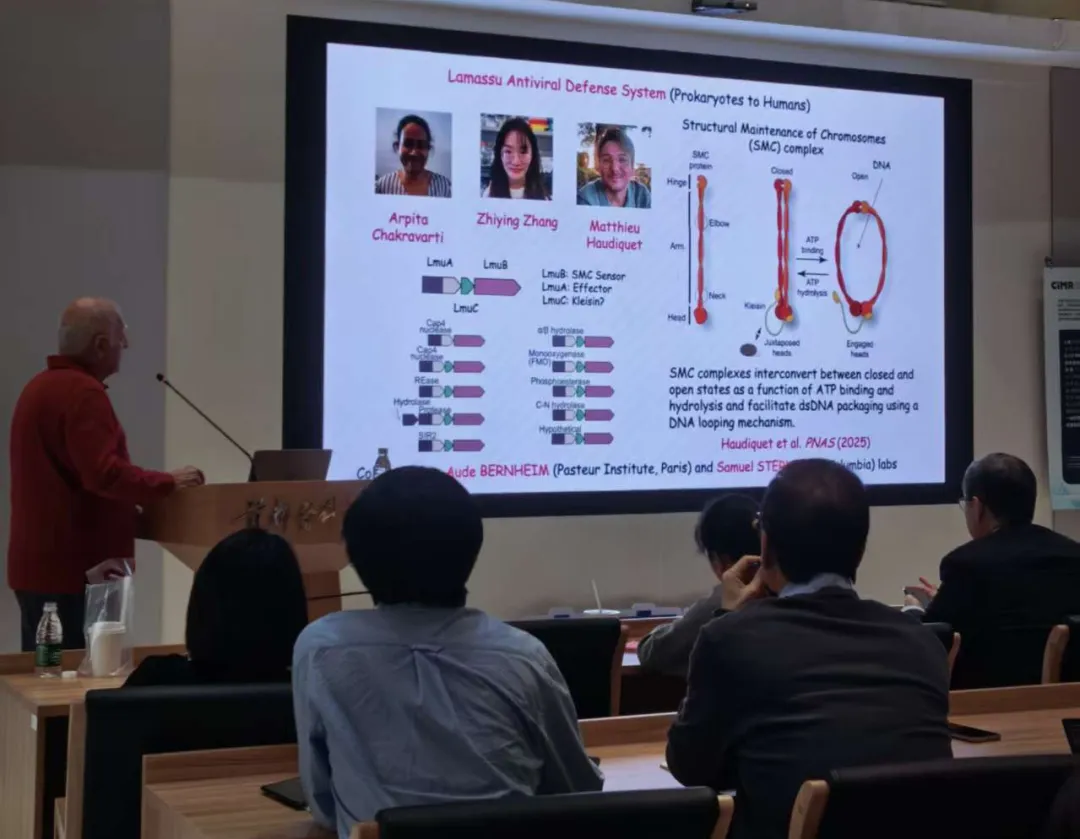
Dinshaw J. Patel 教授介绍 Lamassu 系统
1. Lamassu(3-component system containing an SMC sensor):含 SMC 传感器的三组分系统——从 DNA 修复到免疫防御的功能跃迁
Lamassu 系统通过利用 DNA 修复相关的 SMC 蛋白框架,演化出基于 dsDNA 末端识别的抗噬菌体防御机制。静息状态下,效应蛋白 LmuA 以无活性单体形式被传感器亚基 LmuB 和 LmuC 包裹,形成 LmuA·B₂C 三元复合物。噬菌体感染产生的游离 dsDNA 末端被 LmuB/C 识别后,触发复合物内部 ATP 水解,导致复合物解体并释放单体 LmuA。脱离束缚的 LmuA 发生构象重排并组装为四聚体,在四聚化界面处形成完整的 dsDNA 切割催化口袋,最终通过降解 DNA 引发流产感染。该过程遵循「单体隔离 → 信号释放 → 四聚化成酶」的构象控制逻辑。
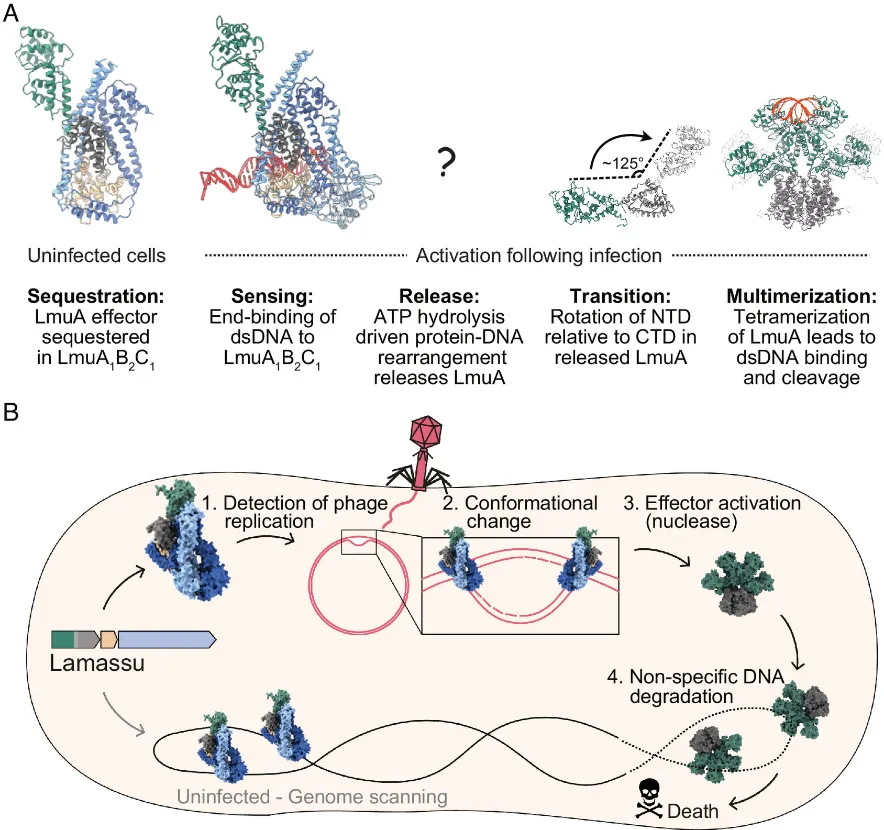
Lamassu 介导抗病毒防御的细胞模型 [3]
2. PUA-Cal-HAD(Epigenetic nucleotide triggers filament formation):表观遗传触发器-从预装复合物到免疫丝状体
PUA-Cal-HAD 系统代表了抗噬菌体触发机制的一个全新范式。该系统由三个特征性结构域组成:PUA(假尿苷合酶样结构域,常结合 RNA 或核苷酸)、Cal(钙结合蛋白样结构域)和 HAD(卤代酸脱卤酶样结构域,通常具有磷酸酶或核苷酸酶活性)。PUA-Cal-HAD 首次揭示了基于宿主表观遗传甲基化图谱的抗噬菌体感应机制,其利用细菌 Dam 甲基化酶维持的 DNA 甲基化图谱(如 m⁶A)作为免疫监控基础。噬菌体感染时,为掠夺核苷酸原料而降解宿主染色体,释放出带有甲基化修饰的游离 mt-dAMP(甲基化脱氧腺苷一磷酸),该分子作为「危险信号」被系统识别。PUA-Cal-HAD 在静息时已预组装为六聚体复合物,处于「待发」状态。mt-dAMP 作为配体结合后,通过配体门控机制引发构象重排,促使多个六聚体首尾相连形成多聚丝状体,将瞬时化学信号转化为持久的结构激活状态。形成巨型丝状体后,复合物可能通过暴露大量 HAD 结构域的催化口袋消耗细胞内 dNTP 池,阻断噬菌体基因组复制,引发流产感染。作为反制,部分噬菌体演化出编码 DNA 模拟蛋白的能力,通过物理性阻断丝状体组装界面来破坏该防御系统,体现了「抗聚合」策略在细菌-噬菌体军备竞赛中的微观博弈。
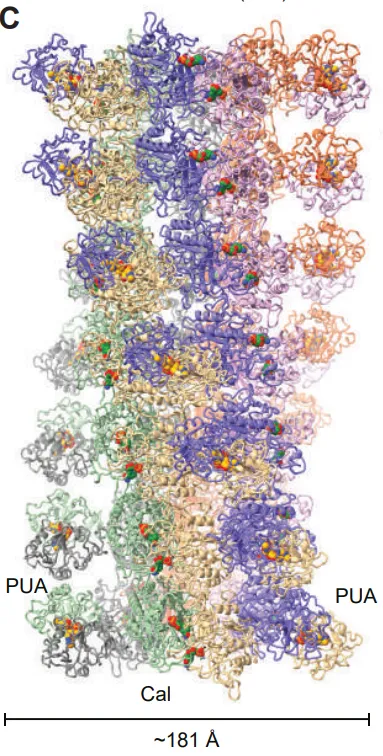
m6-dAMP 结合 PUA-Cal 形成 filament 的结构模型 [4]
这三个系统共同诠释了细菌免疫系统的进化智慧。在触发信号的多样性上,Pucsar 监控代谢失衡(嘌呤水平),Lamassu 监控细胞器损伤(DNA 结构破坏),PUA-Cal-HAD 监控化学副产物(表观遗传核苷酸 mt-dAMP 的释放)。在结构激活的共性上,三者均依赖构象变化介导的寡聚化或丝状化,通过从「点状蛋白」到「线状/网状聚合物」的转变,实现酶活性的放大并引发不可逆的细胞死亡。在终极目标上,三者均通过敏锐的特异性检测,在噬菌体复制的早期阶段按下「自毁按钮」(耗竭 NAD⁺、dNTP、ATP 等),以局部牺牲换取全局生存的群体免疫。
参考文献
[1] Jia N, Jones R, Yang G, Ouerfelli O, Patel DJ. Mol Cell. 2019.
[2] Baca CF, Majumder P, Hickling JH, Patel DJ, Marraffini LA. Science. 2025.
[3] Haudiquet M, Chakravarti A, Zhang Z, Patel DJ. PNAS. 2025.
[4] Zhang Z, Wu Y, Lee YJ, Patel DJ, Nobrega FL. bioRxiv [Preprint]. 2026.
好文章,需要你的鼓励
















