想象一位生活在三万年前冰河时期的母亲,采集与狩猎时代不稳定的食物供给使得身为孕妇的她经常处于食不果腹的状态。但就在此刻,在她温暖的子宫里,一个新的生命正在悄然生长。
令人惊叹的是,这个胎儿并没有因为母亲「饿肚子」而放缓构建自己小小身躯的速度——他的肝脏,正像一个沉着的工程师,无视外界的「能源供应波动」,坚定地执行着原定的生长计划。
巧妇难为无米之炊,还未出生的胎儿是怎么打破这一困境的呢?
2026 年 3 月 13 日, 浙江大学医学院附属第四医院和「一带一路」国际医学院 生殖医学中心黄荷凤院士联合厦门大学生命科学学院林圣彩院士团队在 Vita 期刊发表了题为 TRPV4 acetylation in prenatal liver prevents low glucose-induced inhibition of mTORC1 and safeguards fetal development 的研究论文。本文第一作者是浙大四院生殖医学中心医生张辰颉博
研究发现,哺乳动物胎儿在相对低糖的宫内环境中,通过一种独特的蛋白质化学修饰——「乙酰化」,阻断了肝脏细胞对低糖的应激反应通路,从而保障了合成代谢的持续进行与胎儿的正常发育。这一机制不仅是胎儿应对宫内资源限制的生理适应,更可能是人类漫长演化历史中,为应对母体间歇性食物匮乏而锤炼出的深层生存策略。它从分子层面诠释了生命起源的坚韧,并引发了关于生存环境压力如何塑造生命基本程序的哲学思考。
研究背景与科学问题
哺乳动物细胞中存在两个核心代谢调控节点:促进合成代谢的 mTORC1 和响应能量匮乏、促进分解代谢的 AMPK。在成体细胞中,低糖环境会同时导致 mTORC1 活性抑制与 AMPK 活化,构成经典的营养匮乏应答。既往主要认为该应答是低糖引起细胞内能量水平下降,继而通过 LKB1 激活 AMPK。
近年来研究发现,餐前餐后正常的血糖波动更多是依赖葡萄糖溶酶体感应通路来实现对葡萄糖的感知,即溶酶体通路:低糖环境下,代谢中间产物果糖-1,6-二磷酸(FBP)水平下降,未能与 FBP 结合的醛缩酶会发生构象改变,转而与内质网上的 TRPV 通道结合,使其关闭。这一信号进一步传递至溶酶体表面的 v-ATPase,最终导致 mTORC1 从溶酶体表面脱落,失去活性。这套精密的感应机制,确保了细胞在营养短缺时及时按下「暂停键」。
然而,一个令人困惑的问题由此浮现:胎儿长期处于相对低糖的宫内环境,其肝脏作为合成代谢最为旺盛的器官之一,为何能够「无视」这条经典的营养感应通路,依然维持高水平的建设活动,以支撑快速生长发育?这一有趣的生理学悖论,正是本研究的切入点。
核心发现:胎肝中 mTORC1 与 AMPK 的非偶联激活
研究团队通过模拟母胎之间的葡萄糖浓度差异,对不同细胞系进行了梯度葡萄糖浓度的培养实验,发现了令人兴奋的实验结果:尽管在生理状态下胎儿的葡萄糖供给相对匮乏,但胎肝来源的细胞系即使在完全无葡萄糖的培养基中,其增殖速率依然维持在较高水平。这一现象提示,胎肝细胞可能具备独特的代谢适应机制。
值得注意的是,这一独特现象在成年小鼠肝脏细胞以及经典的对糖敏感、用于研究 mTORC1 和 AMPK 信号通路的模式细胞系 HEK293T 细胞和 MEF 细胞中均未观察到,具有很强的组织与发育阶段特异性。这提示,胎肝细胞这种「无视」低糖信号、坚持合成代谢的能力,可能是胎儿期特有的一种适应性机制,为其在宫内相对低糖环境中的快速生长提供了代谢保障。
机制解析:葡萄糖溶酶体感应通路在 TRPV 水平受阻
为揭示胎肝细胞抵抗低糖信号、维持 mTORC1 活性的分子机制,研究团队进一步深入合作,对葡萄糖溶酶体感应通路的各个环节进行了系统解析:
(1)信号源头感知正常:
通过代谢组学检测发现,低糖处理同样导致胎肝细胞内果糖-1,6-二磷酸(FBP)水平显著下降。这表明,信号通路的起始端——代谢物的变化——在胎肝细胞中依然正常发生,问题可能出在后续的信号传递环节。
(2)阻断点位于通路下游:
进一步检测发现,在胎肝细胞中,低糖并未引起 v-ATP 酶活性下降,mTORC1 依然稳固地结合于溶酶体表面。直接应用 v-ATPase 抑制剂氯化铵,则可迅速导致 mTORC1 失活并脱离溶酶体,提示阻断点位于通路下游的 v-ATP 酶或其调控上游路径。
(3)关键节点锁定 TRPV4:
鉴于 TRPV 家族在葡萄糖感应通路中的关键地位,研究团队对胎肝细胞中 TRPV 家族成员的表达谱进行了分析,发现 TRPV4 的表达量最高,进一步将 TRPV4 作为 TRPV 家族的代表加以研究。为实时监测 TRPV4 通道的活性,团队构建了 TRPV4-GCaMP6s 融合蛋白——利用钙离子浓度敏感的 GCaMP6s 荧光强度变化,来反映 TRPV4 通道的开放状态。结果显示,在成体肝脏细胞和 293T 细胞中,低糖处理可显著抑制 TRPV4 通道活性;然而在胎肝细胞中,即使处于低糖环境,TRPV4 通道依然保持开放状态。应用 TRPV 通道抑制剂 BCTC,则可显著抑制胎肝细胞的 mTORC1 活性,由此鉴定 TRPV4 的低糖不敏感性是维持 mTORC1 活性的关键环节。
一个有趣的旁注:AMPK 的另类激活
值得注意的是,胎肝细胞在低糖环境下虽然维持了 mTORC1 活性,但 AMPK 依然被有效激活。进一步研究发现,这种激活并非通过溶酶体感知途径实现,而是依赖于传统的能量感知机制——即由 AMP/ADP 水平升高所触发。这意味着,在胎肝细胞中,两条通路发生了「解耦联」:溶酶体感应通路被屏蔽以维持合成代谢,而能量应激通路依然正常工作以保障细胞生存。值得注意的是,胎肝细胞中保持着高水平的 AMP、ADP 即能量应激状态,这种状态的成因和所代表的生物学意义,尤其是在发育过程中的意义,值得深思。
分子基础:TRPV4 K608 位点乙酰化为胎肝 mTORC1 戴上「低糖护身符」
为探究胎肝细胞 TRPV4 通道对低糖不敏感性的分子基础,研究团队聚焦于蛋白质翻译后修饰,通过质谱分析以及大量分子实验筛选,鉴定出 TRPV4 上一个在胎肝中特异性高乙酰化的位点——第 608 位赖氨酸(K608)。与成年肝脏相比,胎肝中 TRPV4 K608 位点的乙酰化水平显著升高,提示这一修饰可能与胎儿期的独特代谢状态密切相关。
为验证该位点的功能意义,研究团队构建了模拟去乙酰化状态的 TRPV4-K608R 点突变体。将该突变体导入胎肝细胞后,细胞对低糖环境的抵抗表型被完全逆转:在葡萄糖缺乏条件下,表达 K608R 突变体的胎肝细胞中,v-ATPase 活性受到显著抑制,AXIN 向溶酶体膜的转位增加,mTORC1 从溶酶体表面解离——这一系列分子事件与成体肝细胞在低糖刺激下的经典应答完全一致。结果表明,单一氨基酸位点的修饰状态转换,即足以使胎肝细胞丧失其特有的代谢抵抗特征,转而呈现成体细胞典型的营养感应模式。这进一步证实,TRPV4 K608 位点的高乙酰化是维持胎肝细胞在低糖环境中 mTORC1 持续活化的核心分子基础。
调控机制:乙酰基转移酶 p300 介导 TRPV4 K608 乙酰化
为明确催化 TRPV4 K608 乙酰化的关键酶,研究团队进行了系统的筛选与验证,发现敲低乙酰基转移酶 p300 可显著削弱胎肝细胞对低糖的抵抗能力,使 mTORC1 在低糖环境下受到抑制;而过表达去乙酰化酶 SIRT2 或 SIRT7 则产生类似效应,表明该乙酰化修饰处于动态调控之中。进一步的体外乙酰化实验证实,p300 能够直接作用于 TRPV4,催化 K608 位点的乙酰化修饰。
值得注意的是,p300 在肝脏组织中的表达水平在出生后急剧下降,这一时间节点与胎肝特有的代谢适应状态在出生后消失的现象高度吻合,表明 p300 介导的 TRPV4 K608 乙酰化是胎儿时期特有的调控事件,构成胎肝细胞在宫内低糖环境中维持合成代谢的分子基础。
生理意义:TRPV4 乙酰化对胎儿发育至关重要
为探究上述机制的生理意义,研究团队构建了肝脏特异性敲入去乙酰化模拟突变体 TRPV4-K608R 的转基因小鼠模型。结果显示,在宫内发育阶段,突变体胎鼠肝脏呈现显著的 mTORC1 活性下降,伴随肝脏重量减轻、外观形态异常、细胞增殖率降低以及蛋白质合成减少等表型。更为严重的是,部分突变胚胎在宫内期即发生死亡,提示 TRPV4 乙酰化所维持的合成代谢对胎肝发育乃至个体存活具有不可或缺的作用。在出生后存活方面,所有携带该肝脏特异性突变的子代小鼠均未存活至离乳期,表现出完全的出生前/后致死表型。
为验证这一致死效应是否直接源于宫内 mTORC1 活性抑制,研究团队用雷帕霉素(mTORC1 特异性抑制剂)处理野生型胎鼠,结果显示可有效模拟 TRPV4-K608R 突变体的致死表型,进一步证实宫内 mTORC1 活性的维持是胎鼠正常发育和出生后存活的关键保障。
总结与展望
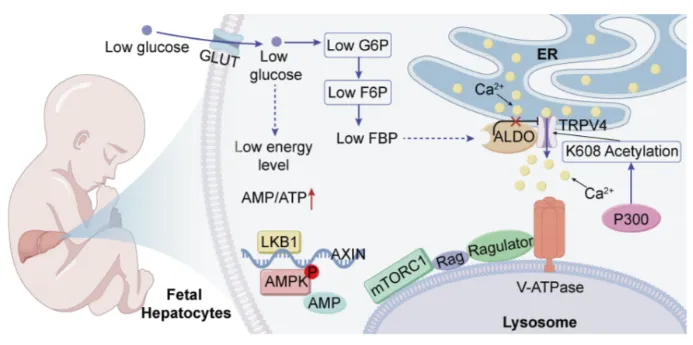
物竞天择,适者生存。这一发现
揭示了胎儿通过 TRPV4 乙酰化将低糖环境转化为生长保障的生存智慧,体现了生命的「反脆弱性」
——并非被动承受环境限制,而是主动将其重构为持续发育的稳定基础,在压力中激发更深层的韧性。然而,这种演化的精巧妥协也暗藏风险:胎儿期为保障生长速度而牺牲的部分营养应激调控能力,可能在个体脱离宫内环境后留下深远的代谢「印记」,与成年后对高热量饮食的不适应、乃至糖尿病等代谢性疾病的易感性产生隐秘关联。
更深层看,这一机制映射了环境与基因之间持续而深刻的对话——母体营养状态可能通过表观遗传修饰微调 TRPV4 乙酰化程度,使胎儿的发育程序在遵循预设蓝图的同时,始终保留着与外部世界交互的窗口。每一个新生命的孕育,都携带着远古与饥饿抗争的艰苦记忆与应对策略;这份深植于细胞深处的「韧性」,既是演化馈赠的生存礼物,也埋下了健康与疾病交织的复杂伏笔。
黄荷凤院士、林圣彩院士、复旦大学附属妇产科医院丁国莲教授、厦门大学生命科学学院张宸崧教授为共同通讯作者,浙江大学医学院附属第四医院张辰颉医师、复旦大学附属妇产科医院余传金助理研究员为共同第一作者。该研究得到了国家自然科学基金、国家重点研发计划等项目资助。
好文章,需要你的鼓励
















