2022 年 11 月 8 日,同济大学附属同济医院消化内科杨长青教授团队在国际期刊发表论文,揭示了 Mas 信号在 DILI 进程中的关键地位及核心机制,为药物干预新靶点的开发提供了重要的数据支持。
肝损伤是众多肝脏疾病的起点,因此往往是肝脏领域突破性研究的发源地。药物性肝损伤(Drug-induced liver injury, DILI)是最常见的严重药物不良反应,也是全球目前导致急性肝衰竭的首要原因。近年来,随着中药、抗生素、抗肿瘤药物的广泛使用,中国大陆的 DILI 疾病负担逐年增加,明显高于其他国家。因此,阐明 DILI 的核心发病机制,以寻找关键药物干预靶点具有重要的临床意义。
2022 年 11 月 8 日,同济大学附属同济医院消化内科杨长青教授团队在国际期刊 Journal of Hepatology(中科院一区 Top,IF 30)以 Original Article 形式在线发表了题为「Hepatocyte-specific Mas activation enhances lipophagy and fatty acid oxidation to protect against acetaminophen-induced hepatotoxicity in mice」的论文,揭示了 Mas 信号在 DILI 进程中的关键地位及核心机制,为药物干预新靶点的开发提供了重要的数据支持。

Mas 是由新发现的原癌基因 Mas1 编码的 G 蛋白偶联受体,本身具备作为理想的药物干预靶点的属性。Mas 在人和小鼠的多种组织内广泛表达,其天然配体为血管紧张素 (1-7),后者是「抗炎型」肾素-血管紧张素系统的重要效应分子,因此理论上,激活 Mas 可能具有改善脂质代谢紊乱、抗炎、抗氧化等多重有益效应,但目前尚无研究涉及 Mas 在 DILI 进程中的作用。
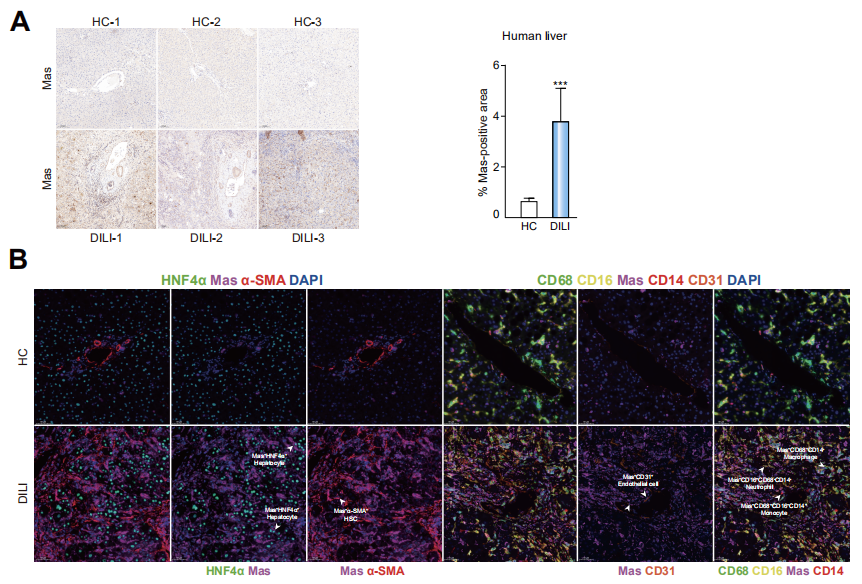
杨长青教授团队首先在 DILI 患者的肝脏局部检测到 Mas 表达水平的显著上调。多重荧光免疫组化染色显示,Mas 在肝细胞呈低水平表达,且在髓系来源单核-巨噬及中性粒细胞呈高水平表达。研究者紧接着开展了一系列的功能实验,证实了 DILI 进程中肝细胞的 Mas 表达上调是机体应对肝损伤的一种保护性反馈,但尚不足以完全对抗药物引起的肝损伤。
解热镇痛类药物——对乙酰氨基酚(acetaminophen, APAP)引起的 DILI(以下简称 AILI)是引起急性肝衰竭的主要致病药物之一。鉴于小鼠 AILI 模型可高度复刻人类 AILI 的病理生理机制,因此在 DILI 的研究领域中使用最为广泛。
在本研究中,研究人员首先发现全身性、肝组织局部、肝细胞特异性 Mas1 基因敲除所致的小鼠 AILI 表型(包括肝损伤程度及炎症水平)高度类似,有力证实了肝细胞 Mas 信号在小鼠 AILI 进程中的关键地位。此外,通过腹腔注射 Mas 受体特异性激动剂 AVE0991,实现 Mas 受体的体内系统性激活,可有效预防和治疗小鼠 AILI。
脂质自噬(简称脂噬)是一种特殊类型的自噬,可选择性地识别脂滴,并高效整合至自噬小体中,利用溶酶体的酶分解甘油三酯产生游离脂肪酸,为脂肪酸氧化(fatty acid oxidation, FAO)提供底物,后者是机体降低脂质毒性的重要代谢途径。
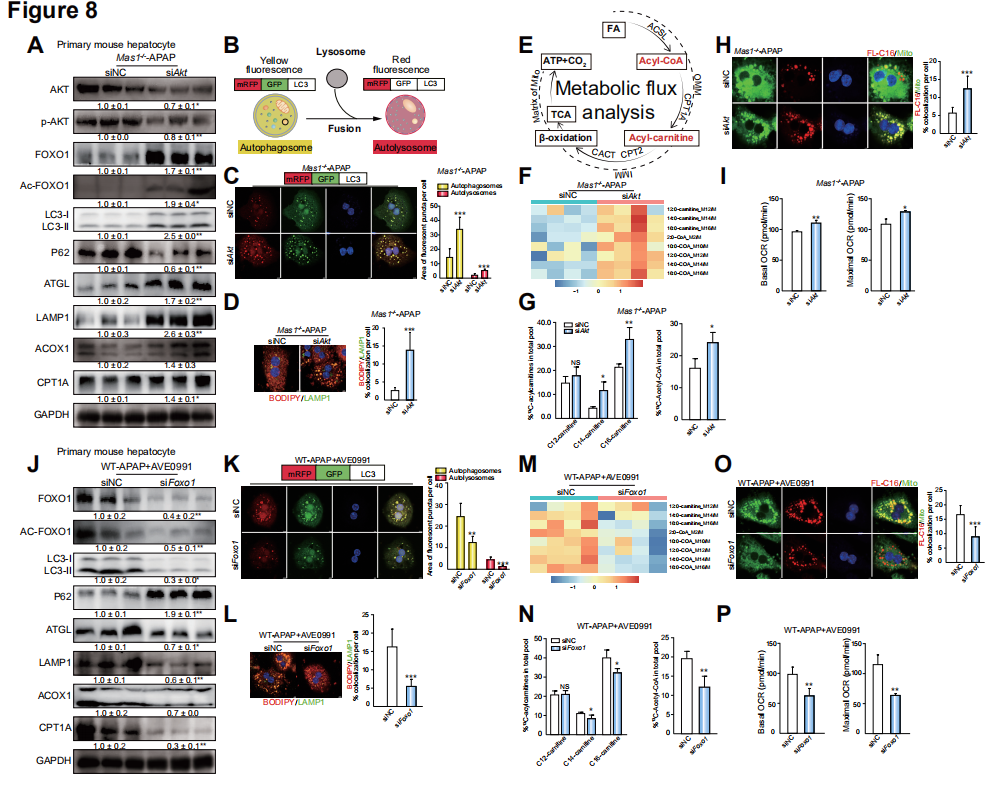
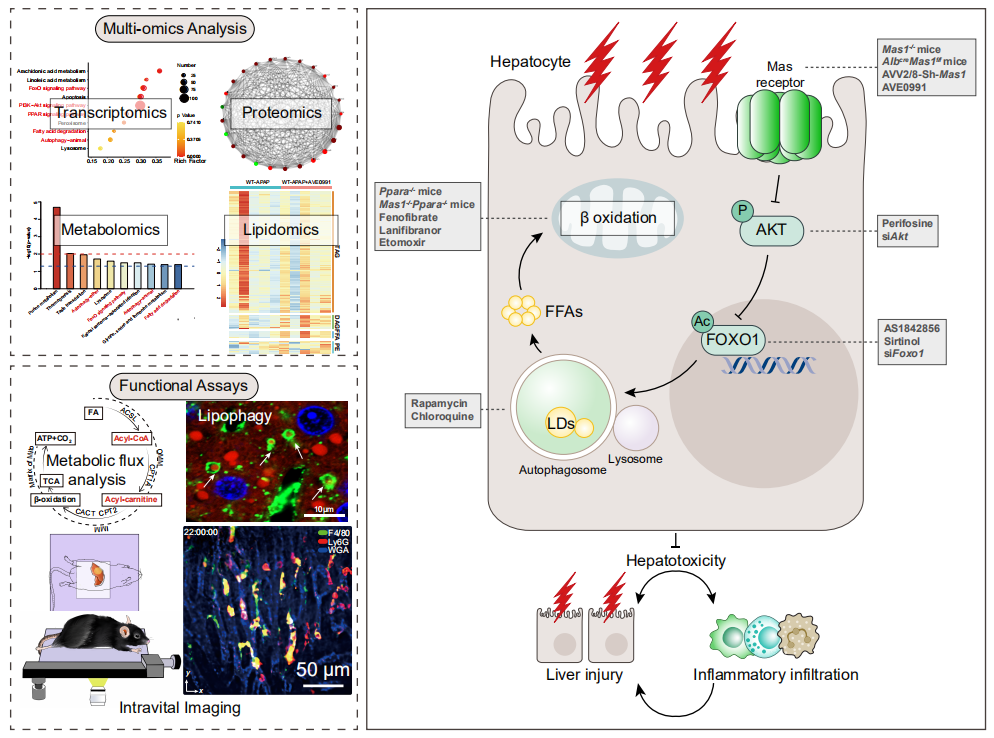
研究者发现,在 AILI 小鼠模型中,Mas 信号缺失往往伴随着脂噬和 FAO 两大效应通路的受损,而激活 Mas 则可显著上调脂噬和 FAO 的水平。通过转录组、蛋白质组、非靶向代谢组及靶向脂质组等多组学联合应用分析,研究者筛选出 AKT-FOXO1 信号分子通路是 Mas 调控 AILI 进程中脂噬和 FAO 变化的关键通路,并通过体内外实验严密论证。
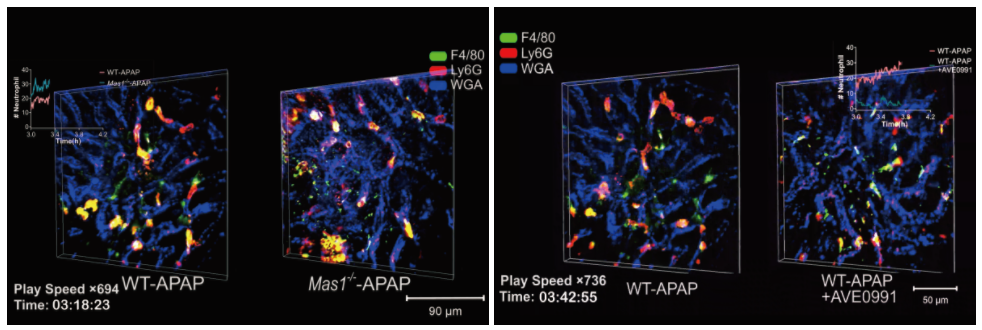
为了更直观地展示 Mas 对炎症细胞的调控作用,研究者还利用清华大学脑与认知科学研究院开发的自适应扫描光场显微镜(digital adaptive optics scanning lightfield mutual iterative tomography, DAOSLIMIT),以超高时空分辨率生动呈现了急性 AILI 进程中,小鼠肝内中性粒细胞及单核巨噬细胞的运动轨迹。
DAOSLIMIT 技术大幅提升了活体三维成像的观测时长及时空分辨率,显著降低了光毒性,在国际上首次实现了哺乳动物活体内连续数小时的毫秒级高速持续观测,为揭示哺乳动物活体多细胞间的相互作用提供了全新路径,于 2021 年发表于著名学术期刊《Cell》。本研究所展示的数据,也是 DAOSLIMIT 在肝脏疾病研究中的首次应用。
上述研究发现在审稿阶段受到审稿人的高度评价,认为是 AILI 进程中的重大突破,可为未来 AILI(对乙酰氨基酚导致的肝损伤)的治疗书写新愿景。(评价原文:The result has been magnificent and the results of transcendence in the field of acetaminophen poisoning. They add knowledge and propose a new path in its treatment.)
好文章,需要你的鼓励















