JMML 治疗选择化疗还是移植?化疗治疗能治愈吗?移植,还是不移植?……治疗路上,我们是否也有诸如此类的难题?又该如何解决?看看彭智勇医生怎么说~非移植案例分享患者,1 岁,男,血小板低(32 G/L
JMML 治疗选择化疗还是移植?化疗治疗能治愈吗?移植,还是不移植?
……
治疗路上,我们是否也有诸如此类的难题?又该如何解决?
看看彭智勇医生怎么说~
非移植案例分享
患者,1 岁,男,血小板低(32 G/L)、脾大,骨髓基因:Kras 突变;HbF 不高;2017 年 10 月确诊 JMML(Kras,低危)
治疗:1 个疗程 DAC 后,PLT 恢复;后续总计 8 个疗程 DAC,基因转阴 1 年,去年 6 月基因突变频率 1.19%;但目前患儿状态正常,继续观察。
彭智勇医生:
1. 患者 1 岁,男孩,主要是脾大,GS、Kras、HbF 不高,血小板也不是特别低,他是 2017 年 10 月份诊断的,我们给他进行地西他滨病治疗,一个疗程后,他血小板就上来了,后续一年的时间,总共打了 8 个疗程。2017 年至今已有三年多,孩子目前的状态比较好。2020 年 6 月,患者基因突变频率 1.19%,又冒了一点点,但是他的血象,肝脾脏都非常好,看不出他是个白血病的孩子,后续继续监测基因变化。
2. 患者,20 个月,确诊 JMML(Nras,低危),HbF:5.7%,PLT 87 G/L,2016 年开始 DAC 治疗,结疗后 3 年,基因阳性,病情稳定。
彭智勇医生:
患者是一个 Nras 突变的孩子,不到两岁时发病,他的 HbF 不高,血小板也不是特别低。我们给他进行地西他滨治疗之后,他的血象以及肝脾脏都很好,现在三年情况非常好。
3. 患者,出生时 3 个月发病,10 个月确诊,HbF:3.1%,2016 年确诊 JMML(Kras,低危)后,即开始 DAC 治疗,结疗后 3 年,稳定。
彭智勇医生:
患者是 Kras 突变的孩子,我们当时发布的是低危,我们给他进行 DAC 治疗,共计 8 个疗程,接近一年的时间,结疗后至今,接近 4 年的时间,病情非常稳定。
彭智勇医生说
这三个是非移植的案例,他们都属于 Nras、Kras 突变的孩子,可能提示这两种基因突变的 JMML 患儿,少部分不需要移植或不急于移植,尤其是通过评估后属于低危的患儿。当然,这个大前提是看孩子的病情是否稳定,能否让临床医生密切随访观察,同时家长也需要知情,愿意接受这种治疗与观察的策略。
哪些孩子可能不需要做移植呢?
彭智勇医生:首先,这没有一个非常明确的金标准。
对于 NRAS 突变的患儿,如果他属于低危的,比如他的血红蛋白 f 不高,血小板不低,没有合并染色体异常核型等因素,可以进行观察或者去甲基化治疗,不急于做移植。对于 CBL 突变的患儿,部分孩子如果病情稳定,我们也可以进行观察与等待,或者是去甲基化治疗的策略。对于 KRAS 突变的患儿,目前有学者认为去甲基化治疗效果较好,特别是低危的 KRAS 突变的患儿,可以不急于移植。
哪些孩子需要移植呢?
彭智勇医生:总的来讲,JMML 是造血干细胞移植的适应症,造血干细胞移植对 JMML 来讲,目前是最可能根治 JMML 的办法。
目前公认的,对于 PTPN11、NF1 突变和复合突变的患儿,目前认为预后较差,必须行造血干细胞移植治疗。除此之外,对于其他基因突变或伴有高危因素(年龄>4 岁,HBF>10%,血小板<40 G/L,肿瘤负荷高,染色体异常核型,高甲基化等)的患儿,我们认为需行造血干细胞移植治疗。
科普时间
近些年来随着检测手段的进步,我们逐渐了解了 JMML 分子基因特征,诊断也随之不断更新变化。
JMML 的诊断主要包括三个方面,临床表现、基因特征以及除五种主要基因突变外其他细胞遗传学特征等。近年来,关于 JMML 表观遗传学研究热点主要集中在 DNA 甲基化方面,有许多研究显示,DNA 甲基化程度与 JMML 进展、预后密切相关。
在 JMML 的治疗方面,目前的治疗手段十分有限,尚无标准化治疗方案,只有异基因造血干细胞移植被证实能够治愈,但其 EFS 仅为 55%。如果不进行治疗干预,大部分 JMML 患者生存时长不到 1 年;如果不进行移植,十年生存率仅 6%。另外,有 30-50% 的患者治疗后复发是治疗失败的主要原因,另外有 15% 左右会转化成为 AML。
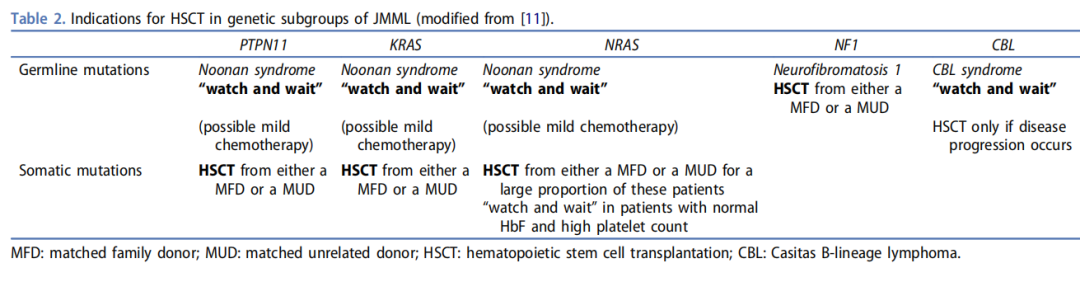
图. JMML 治疗策略
对于胚系突变与体细胞突变的患者,以及不同基因位点突变的患者,治疗建议也有所不同。从基因组学层面,对患者移植指征进行分层,分为低危、中危和高危。如胚系突变的 PTPN11、KRAS、NRAS 等就不需要进行移植,可以先等待和观察,随着时间的推移,可能会慢慢自我缓解。
而体细胞突变的 PTPN11、KRAS 就需要进行移植治疗,NRAS 仅少部分需要做移植,还有一部分会自愈;CBL 通常不建议做移植,但如果疾病仍然进展,也需要尽早考虑移植治疗。
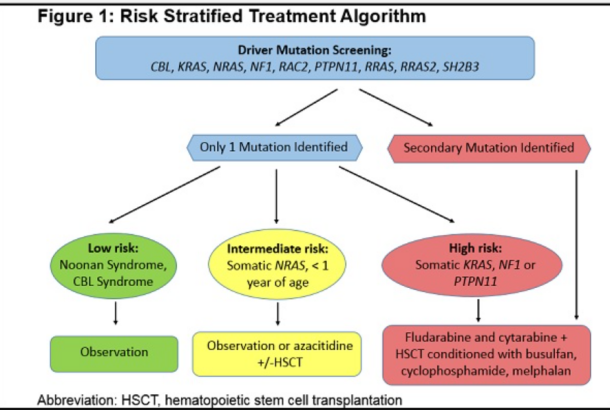
图.JMML 患者风险分层
一项早期研究数据显示,JMML 患者采取异基因造血干细胞移植治疗 EFS 仅为 52%,OS 为 64%,移植复发率高达 35%,移植死亡率是 13%。另一项来自国际多中心的脐血移植的回顾性研究显示,5 年生存率仅 22%,5 年 DFS 为 44%。
对年龄进行分层分析发现,小于 1.4 岁的患者 EFS 明显优于超过 1.4 岁的患者。2018 年来自土耳其一项回顾性研究显示,移植患者的生存优于非移植患者;非 PTPN11 突变患者的生存优于 PTPN11 突变患者。
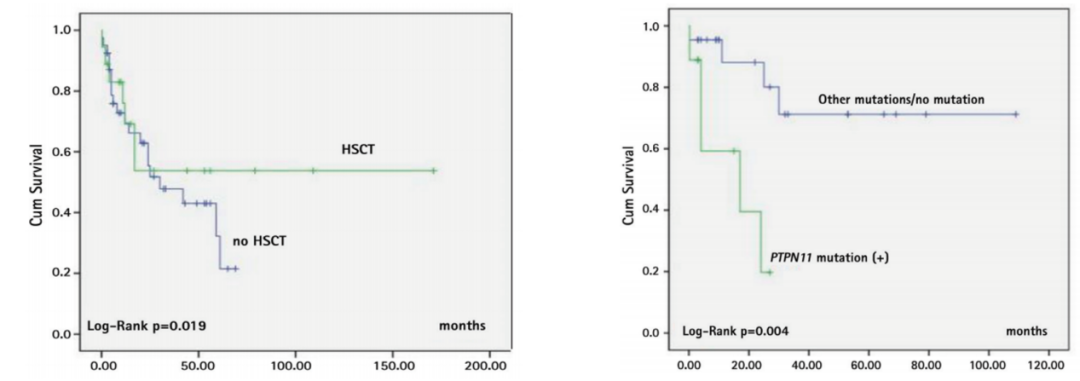
国内一家中心研究报道的数据显示,单倍体造血干细胞移植治疗幼年型单核细胞白血病的 2 年 OS 达 75%,2 年 DFS 达 67%,但 aGVHD 也高达 92%,3-4 度 aGVHD 达 42%;而且病例数也很少。
总结
异基因造血干细胞移植仍然是 JMML 的主要根治手段,但报道的治疗总体疗效并不是很理想。对于少部分患儿来说,是否进行移植仍然存在争议,可参考风险分层来进行指征的评判。
高博南方春富(儿童)血液病研究院彭智勇医生团队通过优化 JMML 移植方案获得良好效果,提示移植前化疗可能使患者获益,此外,移植前、后的去甲基化治疗可能发挥重要作用。
作者简介

彭智勇,高博医疗集团,南方春富(儿童)血液病研究院副主任医师。
2017 年「宋庆龄儿科医学奖」获得者。广东省地贫防治协会治疗专业委员会委员,广东省抗癌协会小儿肿瘤专业委员会第一届青年委员会常委,广东省抗癌协会神经肿瘤专业委员青年委员,广东省医学会罕见病学分会第一届委员会免疫病学组成员。
主持及参与发表论文 20 余篇,SCI 2 篇。主持省市级课题各一项,参与多项国家课题,参与广州市科技项目健康医疗协同创新二期重大专项课题,并完成国内首例基因修饰的造血干细胞移植治疗地中海贫血。
从事临床工作 16 年,主要研究方向为儿童血液病、造血干细胞移植,临床经验较丰富。目前主攻治疗幼年粒单核细胞白血病,JMML 移植治疗成功率在 90% 以上,临床治疗结果达到国际领先水平,成果 2 次在美国血液学会年会(ASH)作为壁报报道,并多次在全国性血液会议做口头报道。
*声明:本内容仅代表文章来源方观点,不代表本站立场。本内容仅供医学药学专业人士阅读,不构成实际治疗建议。
好文章,需要你的鼓励














